ГОСТ 30518-97/ГОСТ Р 50474-93
Группа Н09
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ
Методы выявления и определения количества бактерий группы
кишечных палочек (колиформных бактерий)
Food products. Methods for detection and quantity determination of coliformes
МКС 07.100.30
ОКСТУ 9109
Дата введения 1994-01-01
ИНФОРМАЦИОННЫЕ ДАННЫЕ
1 РАЗРАБОТАН И ВНЕСЕН Всероссийским научно-исследовательским институтом консервной и овощесушильной промышленности (ВНИИКОП) и Техническим комитетом по стандартизации ТК 93 "Продукты переработки плодов и овощей"
2 ПРИНЯТ Межгосударственным Советом по стандартизации, метрологии и сертификации (протокол N 11 от 23 апреля 1997 г.)
3 Настоящий стандарт соответствует ИСО 4831-78 "Микробиология. Общее руководство по подсчету колибактерий. Методика расчета наиболее вероятного значения после инкубации при 30 °С" и ИСО 4832-78 "Микробиология. Общее руководство по подсчету колиформ. Метод подсчета колоний при температуре 30 °С" в части сущности методов
4 Постановлением Госстандарта России от 16 апреля 1998 г. N 122 ГОСТ 30518-97 введен в действие в качестве государственного стандарта Российской Федерации с момента принятия указанного постановления и признан имеющим одинаковую силу с ГОСТ Р 50474-93 на территории Российской Федерации в связи с полной аутентичностью их содержания
За принятие проголосовали:
Наименование государства |
Наименование национального органа |
Республика Беларусь |
Госстандарт Республики Беларусь |
Республика Казахстан |
Госстандарт Республики Казахстан |
Кыргызская Республика |
Кыргызстандарт |
Республика Молдова |
Молдовастандарт |
Российская Федерация |
Госстандарт России |
Республика Таджикистан |
Таджикстандарт |
Туркменистан |
Главгосслужба "Туркменстандартлары" |
Республика Узбекистан |
Узгосстандарт |
5 ВВЕДЕН ВПЕРВЫЕ
6 ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Обозначение НТД, на который дана ссылка |
Номер пункта |
ГОСТ 9284-75 |
3.1 |
ГОСТ 10444.1-84 |
3.1, 5.3 |
ГОСТ 24104-88 |
3.1 |
2 | |
ГОСТ 26669-85 |
2, 5.1.1 |
ГОСТ 26670-91 |
5.1.2, 5.5, 6.3, 6.4, 6.5 |
5.7 |
7 ПЕРЕИЗДАНИЕ
Настоящий стандарт распространяется на пищевые продукты и устанавливает метод выявления в определенной навеске пищевого продукта колиформных бактерий и три метода определения их количества: метод наиболее вероятного числа (НВЧ) и методы посева в или на агаризованные селективно-диагностические среды.
Метод определения НВЧ колиформных бактерий предназначен для пищевых продуктов, содержащих в 1 г твердого продукта менее 150 или в 1 см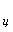 жидкого продукта менее 15 клеток колиформных бактерий.
жидкого продукта менее 15 клеток колиформных бактерий.
Метод определения количества колиформных бактерий посевом в агаризованные селективно-диагностические среды предназначен для пищевых продуктов, содержащих в 1 г твердого продукта более 150 или в 1 см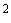 жидкого продукта более 15 колониеобразующих единиц (KОЕ) колиформных бактерий.
жидкого продукта более 15 колониеобразующих единиц (KОЕ) колиформных бактерий.
Метод определения количества колиформных бактерий посевом на агаризованные селективно-диагностические среды предназначен для пищевых продуктов, содержащих в 1 г твердого продукта более 1500 или в 1 см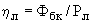 жидкого продукта более 150 KОЕ колиформных бактерий.
жидкого продукта более 150 KОЕ колиформных бактерий.
1 Сущность методов
Методы выявления и определения наиболее вероятного числа колиформных бактерий основаны на высеве определенного количества продукта и (или) разведений навески продукта в жидкую селективную среду с лактозой, инкубировании посевов, учете положительных пробирок (колб), пересеве, при необходимости, культуральной жидкости на поверхность агаризованной селективно-диагностической среды для подтверждения по биохимическим и культуральным признакам роста принадлежности выделенных колоний к колиформным бактериям.
Методы определения количества колиформных бактерий посевом в (на) агаризованные селективно-диагностические среды основаны на высеве определенного количества продукта или его разведений в или на агаризованную селективно-диагностическую среду с лактозой, инкубировании посевов, подсчете типичных колоний, подтверждении, при необходимости, по биохимическим признакам принадлежности выделенных колоний к колиформным бактериям.
2 Отбор и подготовка проб
Отбор и подготовка проб - по ГОСТ 26668, ГОСТ 26669.
3 Аппаратура, материалы, реактивы и питательные среды
3.1 Для проведения испытания применяют аппаратуру, материалы и реактивы по ГОСТ 10444.1 со следующими дополнениями:
весы лабораторные общего назначения с метрологическими характеристиками по ГОСТ 24104* с наибольшим пределом взвешивания 200 г, 2-го класса точности (для взвешивания реактивов);
весы лабораторные общего назначения с метрологическими характеристиками по ГОСТ 24104* с наибольшим пределом взвешивания 1 кг, 4-го класса точности (для взвешивания продукта);
_____________
* С 01.07.2002 г. вводится в действие ГОСТ 24104-2001.
микроскоп световой биологический с увеличением 900-1000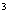 ;
;
петля бактериологическая;
поплавки (трубки Дархема);
стекла предметные по ГОСТ 9284;
термостат с диапазоном рабочих температур 28-55 °С, позволяющий поддерживать заданную температуру с допустимой погрешностью ±1 °С.
бриллиантовый зеленый;
генцианвиолет;
желчь говяжья сухая или натуральная;
метиловый фиолетовый;
феноловый красный.
3.2 Для проведения испытания применяют питательные среды:
агар лактозный с бриллиантовым зеленым и феноловым красным;
бульон лактозный с бриллиантовым зеленым и желчью;
бульон Мак-Конки;
бульон Кесслер;
среду Эндо.
4 Подготовка к испытанию
4.1 Приготовление растворов
4.1.1 Щелочной раствор бромкрезолового пурпурного концентрацией 10 г/дм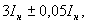 : 1 г бромкрезолового пурпурного переносят в фарфоровую ступку с 19 см
: 1 г бромкрезолового пурпурного переносят в фарфоровую ступку с 19 см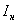 раствора гидроокиси натрия
раствора гидроокиси натрия 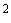 (NaOH)=0,1 моль/дм
(NaOH)=0,1 моль/дм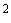 и после растворения добавляют 80 см
и после растворения добавляют 80 см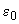 дистиллированной воды.
дистиллированной воды.
4.1.2 Раствор бриллиантового зеленого концентрации 5 г/дм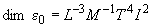 : 0,5 г бриллиантового зеленого переносят в фарфоровую ступку и постепенно растворяют в дистиллированной воде. Раствор переливают в мерную колбу вместимостью 100 см
: 0,5 г бриллиантового зеленого переносят в фарфоровую ступку и постепенно растворяют в дистиллированной воде. Раствор переливают в мерную колбу вместимостью 100 см и доводят дистиллированной водой до метки.
и доводят дистиллированной водой до метки.
4.1.3 Раствор генцианвиолета или кристаллического фиолетового, или метилового фиолетового концентрацией 10 г/дм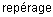 : 1 г одной из анилиновых красок переносят в фарфоровую ступку и постепенно растворяют в дистиллированной воде. Раствор переливают в мерную колбу вместимостью 100 см
: 1 г одной из анилиновых красок переносят в фарфоровую ступку и постепенно растворяют в дистиллированной воде. Раствор переливают в мерную колбу вместимостью 100 см и доводят дистиллированной водой до метки.
и доводят дистиллированной водой до метки.
4.1.4 Раствор фенолового красного концентрации 2 г/дм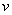 : 0,2 г фенолового красного переносят в фарфоровую ступку и постепенно растворяют в дистиллированной воде. Раствор переливают в мерную колбу вместимостью 100 см
: 0,2 г фенолового красного переносят в фарфоровую ступку и постепенно растворяют в дистиллированной воде. Раствор переливают в мерную колбу вместимостью 100 см и доводят дистиллированной водой до метки.
и доводят дистиллированной водой до метки.
4.1.5 Растворы, приготовленные по 4.1.1-4.1.4, хранят в закрытых сосудах из темного стекла при комнатной температуре не более 3 мес.
4.1.6. Растворы и реактивы для окраски по Граму готовят по ГОСТ 10444.1.
4.2 Приготовление питательных сред
4.2.1 Агар лактозный с бриллиантовым зеленым и феноловым красным: 3,0 г мясного экстракта, 10,0 г пептона, 10,0 г лактозы, 5,0 г хлористого натрия, 0,5 г фосфорнокислого двузамещенного калия, 15,0 г агара добавляют к 1000 см дистиллированной воды. При отсутствии мясного экстракта допускается использовать вместо мясного экстракта, пептона и дистиллированной воды мясопептонный бульон по ГОСТ 10444.1. Смесь нагревают до полного растворения компонентов, охлаждают до 45-55 °С, устанавливают рН так, чтобы после стерилизации она составляла при 25 °С (7,0±0,1). Среду стерилизуют в течение 20 мин при температуре (115±1) °С, затем охлаждают до 45-55° и прибавляют 40 см
дистиллированной воды. При отсутствии мясного экстракта допускается использовать вместо мясного экстракта, пептона и дистиллированной воды мясопептонный бульон по ГОСТ 10444.1. Смесь нагревают до полного растворения компонентов, охлаждают до 45-55 °С, устанавливают рН так, чтобы после стерилизации она составляла при 25 °С (7,0±0,1). Среду стерилизуют в течение 20 мин при температуре (115±1) °С, затем охлаждают до 45-55° и прибавляют 40 см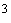 раствора фенолового красного, приготовленного по 4.1.4, и 2 см
раствора фенолового красного, приготовленного по 4.1.4, и 2 см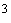 раствора бриллиантового зеленого, приготовленного по 4.1.2, тщательно перемешивают и разливают в стерильные чашки Петри, колбы или флаконы.
раствора бриллиантового зеленого, приготовленного по 4.1.2, тщательно перемешивают и разливают в стерильные чашки Петри, колбы или флаконы.
4.2.2 Бульон лактозный с бриллиантовым зеленым и желчью: 10,0 г пептона, 5,0 г лактозы, 6,45 г двузамещенного фосфорнокислого безводного натрия, 2,0 г однозамещенного фосфорнокислого безводного калия, 20,0 г сухой говяжьей желчи или 200 см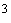 натуральной желчи, 3 см
натуральной желчи, 3 см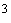 раствора бриллиантового зеленого, приготовленного по 4.1.2, добавляют к 1000 см
раствора бриллиантового зеленого, приготовленного по 4.1.2, добавляют к 1000 см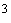 дистиллированной воды (в случае использования натуральной желчи к 800 см
дистиллированной воды (в случае использования натуральной желчи к 800 см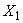 дистиллированной воды), тщательно перемешивают, нагревают на слабом огне до кипения, кипятят 1-2 мин, фильтруют через ватно-марлевый фильтр, охлаждают до 45-55 °С и устанавливают рН таким образом, чтобы она составляла при 25 °С (7,2±0,1), после чего среду вновь доводят до кипения. Среда не подлежит стерилизации в автоклаве, ее разливают с соблюдением правил асептики по 10 см
дистиллированной воды), тщательно перемешивают, нагревают на слабом огне до кипения, кипятят 1-2 мин, фильтруют через ватно-марлевый фильтр, охлаждают до 45-55 °С и устанавливают рН таким образом, чтобы она составляла при 25 °С (7,2±0,1), после чего среду вновь доводят до кипения. Среда не подлежит стерилизации в автоклаве, ее разливают с соблюдением правил асептики по 10 см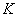 в стерильные пробирки с поплавками или по 100 см
в стерильные пробирки с поплавками или по 100 см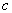 в колбы.
в колбы.
4.2.3 Бульон Мак-Конки: 20,0 г пептона, 10,0 г лактозы, 5,0 г хлористого натрия, 5,0 г сухой говяжей желчи или 50 см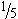 натуральной желчи, 1 см
натуральной желчи, 1 см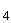 раствора бромкрезолового пурпурного, приготовленного по 4.1.1, добавляют к 1000 см
раствора бромкрезолового пурпурного, приготовленного по 4.1.1, добавляют к 1000 см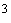 дистиллированной воды (в случае использования натуральной желчи к 950 см
дистиллированной воды (в случае использования натуральной желчи к 950 см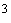 дистиллированной воды), нагревают на слабом огне до кипения, кипятят 1-2 мин, фильтруют через ватно-марлевый фильтр, охлаждают до 45-55 °С и устанавливают рН таким образом, чтобы после стерилизации она составляла при 25 °С (7,2±0,1). Среду разливают по 10 см
дистиллированной воды), нагревают на слабом огне до кипения, кипятят 1-2 мин, фильтруют через ватно-марлевый фильтр, охлаждают до 45-55 °С и устанавливают рН таким образом, чтобы после стерилизации она составляла при 25 °С (7,2±0,1). Среду разливают по 10 см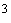 в пробирки с поплавками или в колбы по 100 см
в пробирки с поплавками или в колбы по 100 см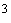 и стерилизуют 15 мин при температуре (121±1) °С.
и стерилизуют 15 мин при температуре (121±1) °С.
4.2.4 Среда Кесслер: 10,0 г пептона, 2,5 г лактозы, 5,0 г сухой говяжьей желчи или 50 см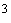 натуральной желчи, 2 см
натуральной желчи, 2 см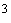 раствора генцианвиолета или кристаллического фиолетового, или метилового фиолетового, приготовленного по 4.1.3, добавляют к 1000 см
раствора генцианвиолета или кристаллического фиолетового, или метилового фиолетового, приготовленного по 4.1.3, добавляют к 1000 см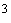 дистиллированной воды (в случае использования натуральной желчи к 950 см
дистиллированной воды (в случае использования натуральной желчи к 950 см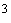 дистиллированной воды), тщательно перемешивают, нагревают на слабом огне до кипения, кипятят 1-2 мин, фильтруют через ватно-марлевый фильтр, охлаждают до 45-55 °С, устанавливают рН таким образом, чтобы после стерилизации она составляла при 25 °С (7,3±0,2). Среду разливают по 10 см
дистиллированной воды), тщательно перемешивают, нагревают на слабом огне до кипения, кипятят 1-2 мин, фильтруют через ватно-марлевый фильтр, охлаждают до 45-55 °С, устанавливают рН таким образом, чтобы после стерилизации она составляла при 25 °С (7,3±0,2). Среду разливают по 10 см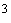 в пробирки с поплавками или в колбы по 100 см
в пробирки с поплавками или в колбы по 100 см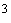 и стерилизуют 20 мин при температуре (115±1) °С,
и стерилизуют 20 мин при температуре (115±1) °С,
4.2.5 Среда Эндо: выпускается Дагестанским НПО "Питательные среды" и готовится по прописи, указанной на этикетке.
4.2.6 Жидкие среды двойной концентрации готовят по 4.2.2-4.2.4, но при приготовлении берут удвоенную массу (объем) ингредиентов, кроме дистиллированной воды, и разливают в посуду с учетом последующего количества добавляемого жидкого продукта.
5 Проведение испытания
5.1 Посевы для определения количества колиформных бактерий
5.1.1 Из навески продукта готовят исходное и ряд десятикратных разведений по ГОСТ 26669 так, чтобы можно было определить в 1 г (см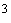 ) продукта предполагаемое количество колиформных бактерий или их количество, указанное в нормативном документе на конкретный продукт.
) продукта предполагаемое количество колиформных бактерий или их количество, указанное в нормативном документе на конкретный продукт.
5.1.2 При определении количества колиформных бактерий посевом на агазированные селективно-диагностические среды по 0,1 или 0,2 см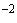 навески продукта или его разведения наносят на поверхность одной из сред, приготовленных по 4.2.1 или 4.2.5 и разлитых в две параллельные чашки Петри. Подготовку чашек Петри со средой к посеву и посев проводят по ГОСТ 26670.
навески продукта или его разведения наносят на поверхность одной из сред, приготовленных по 4.2.1 или 4.2.5 и разлитых в две параллельные чашки Петри. Подготовку чашек Петри со средой к посеву и посев проводят по ГОСТ 26670.
При применении метода мембранных фильтров по ГОСТ 26670 фильтры переносят на поверхность агаризованной селективно-диагностической среды, избегая образования пузырьков воздуха между средой и фильтром. Поверхность фильтра с осевшими на ней бактериями должна быть обращена вверх.
При определении количества колиформных бактерий посевом в агаризованные селективно-диагностические среды по 1 см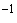 навески продукта или его разведения вносят в две параллельные чашки Петри. Посевы заливают по ГОСТ 26670 на поверхность одной из агаризованных сред, приготовленных по 4.2.1 или 4.2.5.
навески продукта или его разведения вносят в две параллельные чашки Петри. Посевы заливают по ГОСТ 26670 на поверхность одной из агаризованных сред, приготовленных по 4.2.1 или 4.2.5.
5.1.3 При определении количества колиформных бактерий по методу НВЧ высевают три последовательные навески продукта и (или) его разведения, отличающиеся по количеству продукта в них в 10 раз.
Каждую навеску продукта и (или) его разведение в трехкратной повторности высевают в колбы или пробирки с одной из питательных сред, приготовленной по одному из следующих пунктов: 4.2.2, 4.2.3, 4.2.4.
Соотношение между количеством высеваемого продукта или его разведения и питательной средой 1:9, а для сред двойной концентрации - 1:1.
5.2 Посев для выявления колиформных бактерий в определенной навеске продукта
При выявлении колиформных бактерий в определенной навеске продукта или его эквивалентном разведении эту навеску или разведение вносят в одну из питательных сред, приготовленную по одному из следующих пунктов 4.2.2, 4.2.3, 4.2.4. Соотношение между количеством высеваемого продукта или его эквивалентным разведением и питательной средой 1:9, а для сред двойной концентрации - 1:1.
5.3 При испытании высококислотных продуктов для предотвращения резкого снижения рН (на 0,5 и более) питательных сред при внесении в них продукта или его разведений рН питательных сред доводят до допустимых значений с помощью стерильного раствора гидроокиси натрия, приготовленного по ГОСТ 10444.1, или при приготовлении питательных сред рН устанавливают выше заданного с учетом ее последующего снижения при внесении продукта. Количество добавляемого раствора гидроокиси натрия или величину, на которую необходимо увеличить рН при приготовлении питательных сред, устанавливают опытным путем.
5.4 Посевы на агаризованных и жидких средах инкубируют при температуре (36±1) °С в течение 24-48 ч. Чашки Петри с посевами инкубируют дном вверх. Посевы просматривают через (24±3) ч, отмечают положительные посевы в жидкие среды, а окончательный учет проводят через (48+3) ч.
Положительными считают посевы в жидкие среды, в которых имеет место интенсивный рост микроорганизмов, проявляющийся в помутнении среды, образовании газа, подкислении среды (то есть изменении цвета среды).
5.5 При необходимости, для подтверждения принадлежности микроорганизмов, выросших на жидких средах, к колиформным бактериям делают пересевы по ГОСТ 26670 на поверхность одной из агаризованных селективно-диагностических сред, приготовленных по 4.2.1 или 4.2.5. Посевы инкубируют при температуре (36±1) °С в течение (24±3) ч.
5.6 Посевы на агаризованных средах по 5.1 и 5.5 после инкубирования просматривают и отмечают рост характерных колоний.
На агаре лактозном с бриллиантовым зеленым и феноловым красным колиформные бактерии образуют ярко-желтые колонии диаметром 2-4 мм с желтой прозрачной зоной диаметром 1-3 мм вокруг колонии.
На среде Эндо колиформные бактерии образуют колонии бледно-розового или красного цвета, часто с металлическим блеском.
В посевах по 5.1.2 отбирают чашки, на которых выросло от 15 до 150 характерных колоний. При посеве методом мембранных фильтров на них подсчитывают количество колоний и в том случае, если их менее 15.
5.7 При необходимости подтверждения принадлежности выросших микроорганизмов к колиформным бактериям из чашек Петри с посевами по 5.1 и 5.5 отбирают не менее чем по пять колоний. Из каждой отобранной колонии приготавливают мазки и окрашивают по Граму (по ГОСТ 30425).
Колиформные бактерии являются грамотрицательными палочками.
6 Обработка результатов
6.1 Результаты оценивают по каждой пробе отдельно.
6.2 К колиформным бактериям относят аэробные и факультативно-анаэробные не образующие спор грамотрицательные палочки, сбраживающие лактозу с образованием кислоты и газа.
6.3 При определении НВЧ или при выявлении колиформных бактерий в определенной навеске продукта посевы в жидких средах считают положительными, если при последующем пересеве и подтверждении характерных колоний хотя бы в одной колонии будут обнаружены колиформные бактерии.
НВЧ колиформных бактерий в 1 г (см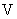 ) продукта определяют по количеству положительных колб (пробирок) по ГОСТ 26670.
) продукта определяют по количеству положительных колб (пробирок) по ГОСТ 26670.
6.4 Если при подтверждении характерных колоний в 80% случаев, то есть не менее чем в 4 из 5 колоний, подтвержден рост колиформных бактерий, то считают, что все характерные колонии, выросшие на чашке Петри (см. п.5.6), принадлежат к колиформным бактериям. В остальных случаях количество колиформных бактерий определяют, исходя из процентного отношения подтвержденных колоний к общему количеству характерных колоний, взятых для подтверждения.
Пересчет количества колиформных бактерий, определенного посевом в или на агаризованные среды, на 1 г (см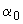 ) продукта проводят по ГОСТ 26670.
) продукта проводят по ГОСТ 26670.
6.5 Результаты определения количества колиформных бактерий и выявления их в определенной навеске продукта записывают по ГОСТ 26670.
Текст документа сверен по:
официальное издание
Консервы. Методы
микробиологического анализа:
Сб. ГОСТов. -
М.: ИПК Издательство стандартов, 2002