РД 34.50.503.2-93
МЕТОДИКА
ПО ОПРЕДЕЛЕНИЮ СОДЕРЖАНИЯ ХЛОРИДОВ
В ЭЛЕКТРОЛИТЕ ЭЛЕКТРОЛИЗНЫХ УСТАНОВОК
ТЭС ПОТЕНЦИОМЕТРИЧЕСКИМ МЕТОДОМ
Срок действия с 01.01.94
до 01.01.99*
_______________________
* См. ярлык "Примечания".
РАЗРАБОТАНА АО "Фирма по наладке, совершенствованию технологии и эксплуатации электростанций и сетей ОРГРЭС"
Исполнители Р.Л.Медведева, И.В.Никитина (ВХЦ); С.А.Спорыхин, Л.В.Соловьева (ЦИТМ)
УТВЕРЖДЕНА Департаментом науки и техники РАО "ЕЭС России" 27.12.93 г.
Первый заместитель начальника А.П.БЕРСЕНЕВ
Методика регламентирует порядок проведения количественного химического анализа проб электролита электролизных установок ТЭС потенциометрическим методом для определения в них содержания хлоридов, устанавливает требования к используемым средствам измерений, алгоритму проведения измерений и обработке результатов.
Методика обеспечивает получение достоверных характеристик погрешности определения содержания хлоридов в электролите при принятой доверительной вероятности и способы их выражения.
Результаты определения содержания хлоридов в электролите используют для контроля качества электролита электролизных установок ТЭС, которые регламентируются "Типовой инструкцией по эксплуатации электролизных установок для получения водорода и кислорода: ТИ 34-70-056-86*". (М.: СПО Союзтехэнерго, 1986).
_______________
* На территории Российской Федерации действует РД 34.50.501-96. - Примечание .
1. СВЕДЕНИЯ ОБ ОБЪЕКТЕ КОНТРОЛЯ
1.1. Электролит используют для получения водорода в электролизных установках ТЭС, применяемого в системах охлаждения генераторов и синхронных компенсаторов.
1.2. Электролит представляет собой раствор гидроксида калия с концентрацией основного вещества KOH 390-400 г/дм![]() .
.
1.3. В процессе эксплуатации происходит загрязнение электролита различными примесями и продуктами коррозии, что приводит к ухудшению технологических характеристик оборудования.
1.4. Для обеспечения экономичной и безопасной работы электролизера требуется контроль качества электролита с целью поддержания в нем соединений хлоридов в пределах нормы - не более 6 г/дм![]() (см. Типовую инструкцию по эксплуатации электролизных установок для получения водорода и кислорода).
(см. Типовую инструкцию по эксплуатации электролизных установок для получения водорода и кислорода).
2. СРЕДСТВА ИЗМЕРЕНИЙ, ВСПОМОГАТЕЛЬНЫЕ УСТРОЙСТВА,
ПОСУДА, РЕАКТИВЫ И РАСТВОРЫ
При определении содержания хлоридов следует применять средства измерений, вспомогательные устройства (ВУ), посуду, реактивы и растворы, перечень которых приведен в табл.1-4.
Таблица 1
Средства измерений
|
Наименование |
Тип |
Диапазон измерений |
Класс точности или предел допустимой погрешности |
Примечание |
|
1. Иономер |
ЭВ-74 |
-(100 |
±2,3 мВ |
|
|
2. Весы лабораторные аналитические |
ВЛР-200 |
(0 |
2,0 |
|
|
3. Термометр лабораторный |
ТЛ-2 |
(0 |
Цена деления 1 °С |
|
|
4. Хлор-селективный твердоконтактный электрод |
ЭК-041401 |
1·10 моль/дм |
|
КСРШ418422.037.TУ |
|
5. Вспомогательный хлор-серебряный электрод |
ЭВЛ-1М3.1 |
|
|
ТУ 25.05.2181-77 |
Примечание. Принцип работы хлор-селективного твердоконтактного электрода основан на селективном обмене между ионами мембраны и ионами хлора, содержащимися в анализируемом растворе.
Электрод селективен в присутствии бромид-ионов и иодид-ионов. Мешающие ионы: S![]() , CN
, CN![]() ; S
; S![]() O
O![]() .
.
Оптимальное значение рабочей области 2-11 ед. pH.
Крутизна хлоридной функции электрода при ![]() =25 °С составляет (54±4) мВ/pCl.
=25 °С составляет (54±4) мВ/pCl.
Электрод хранят в сухом виде.
Таблица 2
Вспомогательные устройства
|
Наименование ВУ |
Требования к ВУ |
|
1. Электролитический ключ |
См. примечание |
|
2. Шнур из асбестового волокна |
Шнур предварительно кипятят в дистиллированной воде (10-15 мин) |
Примечание. Электролитический ключ (рис.1) представляет собой стеклянную ячейку с капилляром, который заполнен асбестовым волокном. В ячейку наливают насыщенный раствор нитрата калия и помещают электрод сравнения.
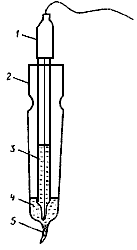
Рис.1. Электролитический ключ:
1 - электрод сравнения; 2 - стеклянная ячейка с капилляром;
3 - насыщенный раствор KCl; 4 - насыщенный раствор KNO![]() ; 5 - асбестовый шнур
; 5 - асбестовый шнур
Таблица 3
Посуда
|
Наименование |
Тип |
НТД |
|
1. Колбы мерные |
2-1000-2, |
ГОСТ 1770-74 |
|
|
2-100-2 |
ГОСТ 1770-74 |
|
2. Стакан мерный вместимостью 50 см |
Н-1-50 ТХС |
ГОСТ 25336-82 |
|
3. Пипетки |
6-2-10, |
ГОСТ 20292-74 |
|
|
6-2-5 |
ГОСТ 20292-74 |
Приведенные в табл.1 и 3 средства измерений и посуда могут быть заменены аналогичными с характеристиками не хуже указанных.
Таблица 4
Растворы и реактивы
|
Наименование |
Классификация |
НТД |
Примечание |
|
1. Вода дистиллированная Н |
|
ГОСТ 6709-72 |
Воду следует предохранять от попадания паров соляной кислоты и углекислоты из воздуха |
|
2. Уксусная кислота CH |
"х.ч." |
ГОСТ 61-75 |
|
|
3. Буферный раствор стандарт-титр натрий тетра-борнокислый Na |
|
ГОСТ 8.135-74* |
рН-9,18 |
|
4. Насыщенный раствор хлористого калия KCl |
"ч.д.а." |
ГОСТ 4234-77 |
|
|
5. Насыщенный раствор азотнокислого калия KNO |
"ч." |
ГОСТ 4217-77 |
|
________________
* Действует ГОСТ 8.135-2004. - Примечание .
Приготовление рабочих и стандартных растворов
1. Для приготовления стандартного раствора используют фиксанал 0,1 N NaCI "о.с.ч." (МРТУ 6-09-292-70), растворенный в 0,1 М растворе KNO![]() , массовая концентрация хлора в этом растворе составляет 3,55 г/дм
, массовая концентрация хлора в этом растворе составляет 3,55 г/дм![]() . (При отсутствии фиксанала используют хлорид натрия "х.ч." (ГОСТ 4233-77). Навеску 5,845 г хлористого натрия, предварительно высушенного в течение 1-2 ч при температуре 110 °С, растворяют в 0,1 М растворе KNO
. (При отсутствии фиксанала используют хлорид натрия "х.ч." (ГОСТ 4233-77). Навеску 5,845 г хлористого натрия, предварительно высушенного в течение 1-2 ч при температуре 110 °С, растворяют в 0,1 М растворе KNO![]() , переносят в мерную колбу на 1 дм
, переносят в мерную колбу на 1 дм![]() и доводят до метки. Этот раствор содержит 3,55 г/дм
и доводят до метки. Этот раствор содержит 3,55 г/дм![]() хлора.
хлора.
Из основного раствора последующим разбавлением в 0,1 М KNO![]() готовят растворы меньших концентраций.
готовят растворы меньших концентраций.
2. 0,1 М раствор KNO![]() . Навеску нитрата калия 10,1 г растворяют в дистиллированной воде, переносят в мерную колбу на 1 дм
. Навеску нитрата калия 10,1 г растворяют в дистиллированной воде, переносят в мерную колбу на 1 дм![]() и доводят до метки.
и доводят до метки.
3. МЕТОД ИЗМЕРЕНИЙ
3.1. Сущность метода
Метод основан на измерении электродвижущей силы (ЭДС) электродной системы, состоящей из измерительного электрода (Cl-селективного) и электрода сравнения. ЭДС, развиваемая электродной системой, прямо пропорциональна определяемому значению ![]() .
.
Зависимость потенциала электрода от активности потенциалообразующих ионов в растворе выражается уравнением Нернста
![]() , (1)
, (1)
где ![]() - активная концентрация потенциалообразующих ионов, г-ион/дм
- активная концентрация потенциалообразующих ионов, г-ион/дм![]() ;
;
![]() - нормальный или стандартный электродный потенциал, численно равный
- нормальный или стандартный электродный потенциал, численно равный ![]() при
при ![]() 1;
1;
![]() - универсальная газовая постоянная, равная 8,314 Дж/(град·моль);
- универсальная газовая постоянная, равная 8,314 Дж/(град·моль);
![]() - абсолютная температура, K;
- абсолютная температура, K;
![]() - число электронов, переносимых в процессе реакции, или заряд потенциалообразующего иона;
- число электронов, переносимых в процессе реакции, или заряд потенциалообразующего иона;
![]() - число Фарадея, равное 96500 Кл.
- число Фарадея, равное 96500 Кл.
Выразив постоянные величины ![]() и
и ![]() через их численные значения, а натуральные логарифмы через десятичные, получим упрощенное выражение уравнения Нернста
через их численные значения, а натуральные логарифмы через десятичные, получим упрощенное выражение уравнения Нернста
![]() , (2)
, (2)
где ![]() - концентрация потенциалообразующих ионов, т.е. хлора.
- концентрация потенциалообразующих ионов, т.е. хлора.
Таким образом, ЭДС электродной системы в анализируемом растворе связана с концентрацией ионов хлора логарифмической зависимостью
![]() , (3)
, (3)
где ![]() - концентрация ионов хлора, моль/дм
- концентрация ионов хлора, моль/дм![]() .
.
3.2. Диапазон измеряемых концентраций
Метод позволяет контролировать содержание ионов хлора в растворе в диапазоне концентраций от 3,55·10![]() мкг/дм
мкг/дм![]() до 3,55·10
до 3,55·10![]() мкг/дм
мкг/дм![]() .
.
3.3. Продолжительность определения
Продолжительность определения в единичной пробе при готовых калибровочных растворах и настроенной аппаратуре составляет около 1 мин.
4. ТРЕБОВАНИЯ БЕЗОПАСНОСТИ
4.1. Работа с иономером должна проводиться в соответствии с требованиями инструкции по эксплуатации.
4.2. При работе с уксусной кислотой следует выполнять требования безопасности в соответствии с "Правилами техники безопасности при эксплуатации тепломеханического оборудования электростанций и тепловых сетей*". (М.: Энергоатомиздат, 1985).
________________
* На территории Российской Федерации действует РД 34.03.201-97. - Примечание .
4.3. При приготовлении и использовании стандартных растворов следует выполнять требования безопасности в соответствии с ГОСТ 12.1.005-88 и ГОСТ 12.1.007-76.
5. ТРЕБОВАНИЯ К КВАЛИФИКАЦИИ ПЕРСОНАЛА
К выполнению анализа допускаются лица, имеющие среднее образование и практический опыт работы в химической лаборатории не менее 3 мес.
6. ПОДГОТОВКА К ВЫПОЛНЕНИЮ АНАЛИЗА
6.1. Собрать установку в соответствии с рис.2.
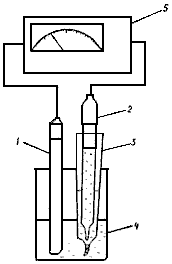
Рис.2. Установка для определения хлоридов потенциометрическим методом:
1 - хлор-селективный электрод; 2 - вспомогательный электрод;
3 - электролитический ключ; 4 - анализируемая проба; 5 - иономер
В стеклянный сосуд, заполненный анализируемым раствором или дистиллированной водой, поместить измерительный электрод и электрод сравнения. Подключить электроды к прибору.
6.2. Подготовить иономер к работе в соответствии с требованиями заводской инструкции.
6.3. Проверить работоспособность ион-селективного электрода.
Перед началом работы промыть электрод в течение 10-15 мин в дистиллированной воде. Произвести измерение потенциала в воде, а затем в 0,1 М растворе KNO![]() . Электрод готов к работе, если потенциал электрода, измеренный в дистиллированной воде, отличается от потенциала в 0,1 М растворе KNO
. Электрод готов к работе, если потенциал электрода, измеренный в дистиллированной воде, отличается от потенциала в 0,1 М растворе KNO![]() на 20-30 мВ. Если разность потенциалов отличается от указанного, необходимо повторить отмывку электрода с контролем потенциала.
на 20-30 мВ. Если разность потенциалов отличается от указанного, необходимо повторить отмывку электрода с контролем потенциала.
6.4. Определить крутизну электрода, для чего приготовить калибровочные растворы. Из исходного раствора (10![]() моль/дм
моль/дм![]() NaCl) последующим разбавлением в 0,1 М растворе KNO
NaCl) последующим разбавлением в 0,1 М растворе KNO![]() приготовить растворы следующих концентраций: 10
приготовить растворы следующих концентраций: 10![]() ; 10
; 10![]() ; 10
; 10![]() моль/дм
моль/дм![]() .
.
В стеклянный стакан поместить 25 см![]() каждого раствора и добавить по 10 см
каждого раствора и добавить по 10 см![]() буферного раствора.
буферного раствора.
Произвести измерение потенциалов ![]() калибровочных растворов и рассчитать крутизну электродной функции
калибровочных растворов и рассчитать крутизну электродной функции ![]() .
.
![]() ;
;
![]() ; (4)
; (4)
![]() .
.
За ![]() принимаем среднее значение из трех полученных данных
принимаем среднее значение из трех полученных данных
7. ВЫПОЛНЕНИЕ АНАЛИЗА
7.1. Подготовка пробы
При анализе электролита потенциометрическим методом для определения содержания хлоридов не требуется особой подготовки пробы. Однако, исходя из технических характеристик Cl-селективного электрода, необходимо щелочной раствор электролита нейтрализовать уксусной кислотой до рН 8-9 по индикаторной бумаге.
7.2. Анализ пробы
Определяемый объем электролита (10 см![]() ) поместить в мерный стакан вместимостью 50-100 см
) поместить в мерный стакан вместимостью 50-100 см![]() . Нейтрализовать 5-7 см
. Нейтрализовать 5-7 см![]() уксусной кислоты по каплям; проверить рН раствора, который должен быть в пределах 8-9.
уксусной кислоты по каплям; проверить рН раствора, который должен быть в пределах 8-9.
Объем анализируемого раствора довести до 25 см![]() дистиллированной водой или нитратом калия, прибавить 10 см
дистиллированной водой или нитратом калия, прибавить 10 см![]() боратно-буферного раствора и измерить потенциал в анализируемом растворе.
боратно-буферного раствора и измерить потенциал в анализируемом растворе.
8. РАСЧЕТ СОДЕРЖАНИЯ ХЛОРИДОВ В ПРОБЕ
8.1. Определить значение ![]() анализируемого раствора по формуле
анализируемого раствора по формуле
![]() , (6)
, (6)
где ![]() - потенциал электрода в 0,1 М KCl, мВ;
- потенциал электрода в 0,1 М KCl, мВ;
![]() - потенциал электрода в анализируемом растворе, мВ;
- потенциал электрода в анализируемом растворе, мВ;
![]() - крутизна электродной функции данного электрода, мВ/
- крутизна электродной функции данного электрода, мВ/![]() .
.
8.2. Получив значение ![]() , найти по табл.5 содержание хлоридов
, найти по табл.5 содержание хлоридов ![]() (мкг/дм
(мкг/дм![]() ) и с учетом разбавления определить концентрацию Cl в анализируемом растворе.
) и с учетом разбавления определить концентрацию Cl в анализируемом растворе.
В данном случае кратность разбавления (![]() ) равна 2,5. Объем добавляемого буферного раствора не принимается во внимание при учете разбавления, так как он и не учитывается при определении потенциала электрода стандартных растворов для определения электродной функции.
) равна 2,5. Объем добавляемого буферного раствора не принимается во внимание при учете разбавления, так как он и не учитывается при определении потенциала электрода стандартных растворов для определения электродной функции.
![]() , (7)
, (7)
где ![]() - концентрация хлоридов, найденная по табл.5, мкг/дм
- концентрация хлоридов, найденная по табл.5, мкг/дм![]() ;
;
![]() - кратность разбавления.
- кратность разбавления.
8.3. Для определения концентрации хлоридов вместо расчета по формуле можно пользоваться калибровочным графиком. Для этого необходимо определить потенциалы электрода в стандартных растворах с известной концентрацией хлоридов. По результатам измерений построить график ![]() .
.
Таблица 5
Пересчет ![]() в массовую концентрацию хлоридов
в массовую концентрацию хлоридов
|
|
C |
|
4,00 |
3550,00 |
|
3,99 |
3632,69 |
|
3,98 |
3717,31 |
|
3,97 |
3803,89 |
|
3,96 |
3892,50 |
|
3,95 |
3983,17 |
|
3,94 |
4075,95 |
|
3,93 |
4170,89 |
|
3,92 |
4268,04 |
|
3,91 |
4367,45 |
|
3,90 |
4469,19 |
|
3,89 |
4573,29 |
|
3,88 |
4679,81 |
|
3,87 |
4788,82 |
|
3,86 |
4900,36 |
|
3,85 |
5014,51 |
|
3,84 |
5131,31 |
|
3,83 |
5250,83 |
|
3,82 |
5373,14 |
|
3,81 |
5498,30 |
|
3,80 |
5626,37 |
|
3,79 |
5757,43 |
|
3,78 |
5891,53 |
|
3,77 |
6028,76 |
|
3,76 |
6169,19 |
|
3,75 |
6312,89 |
|
3,74 |
6459,94 |
|
3,73 |
6610,41 |
|
3,72 |
6764,39 |
|
3,71 |
6921,95 |
|
3,70 |
7083,18 |
|
3,69 |
7248,17 |
|
3,68 |
7417,04 |
|
3,67 |
7589,77 |
|
3,66 |
7766,55 |
|
3,65 |
7947,46 |
|
3,64 |
8132,58 |
|
3,63 |
8322,01 |
|
3,62 |
8515,86 |
|
3,61 |
8714,22 |
|
3,60 |
8917,20 |
|
3,59 |
9124,91 |
|
3,58 |
9337,45 |
|
3,57 |
9554,95 |
|
3,56 |
9777,51 |
|
3,55 |
10005,26 |
|
3,54 |
10238,31 |
|
3,53 |
10476,79 |
|
3,52 |
10720,83 |
|
3,51 |
10970,55 |
|
3,50 |
11226,09 |
|
3,49 |
11487,57 |
|
3,48 |
11755,15 |
|
3,47 |
12028,97 |
|
3,46 |
12309,16 |
|
3,45 |
12595,88 |
|
3,44 |
12889,27 |
|
3,43 |
13189,50 |
|
3,42 |
13496,72 |
|
3,41 |
13811,10 |
|
3,40 |
14132,80 |
|
3,39 |
14462,00 |
|
3,38 |
14798,86 |
|
3,37 |
15143,57 |
|
3,36 |
15496,31 |
|
3,35 |
15857,27 |
|
3,34 |
16226,63 |
|
3,33 |
16604,60 |
|
3,32 |
16991,37 |
|
3,31 |
17387,15 |
|
3,30 |
17792,15 |
|
3,29 |
18206,58 |
|
3,28 |
18630,66 |
|
3,27 |
19064,63 |
|
3,26 |
19508,70 |
|
3,25 |
19963,12 |
|
3,24 |
20428,12 |
|
3,23 |
20903,95 |
|
3,22 |
21390,87 |
|
3,21 |
21889,12 |
|
3,20 |
22398,99 |
|
3,19 |
22920,73 |
|
3,18 |
23454,62 |
|
3,17 |
24000,95 |
|
3,16 |
24560,00 |
|
3,15 |
25132,08 |
|
3,14 |
25717,48 |
|
3,13 |
26316,51 |
|
3,12 |
26929,50 |
|
3,11 |
27556,77 |
|
3,10 |
28198,65 |
|
3,09 |
28855,48 |
|
3,08 |
29527,61 |
|
3,07 |
30215,40 |
|
3,06 |
30919,21 |
|
3,05 |
31639,41 |
|
3,04 |
32376,38 |
|
3,03 |
33130,53 |
|
3,02 |
33902,24 |
|
3,01 |
34691,92 |
|
3,00 |
35500,00 |
|
2,99 |
36326,90 |
|
2,98 |
37173,06 |
|
2,97 |
38038,94 |
|
2,96 |
38924,98 |
|
2,95 |
39831,66 |
|
2,94 |
40759,45 |
|
2,93 |
41708,86 |
|
2,92 |
42680,39 |
|
2,91 |
43674,54 |
|
2,90 |
44691,85 |
|
2,89 |
45732,86 |
|
2,88 |
46798,11 |
|
2,87 |
47888,18 |
|
2,86 |
49003,64 |
|
2,85 |
50145,08 |
|
2,84 |
51313,11 |
|
2,83 |
52508,35 |
|
2,82 |
53731,42 |
|
2,81 |
54982,99 |
|
2,80 |
56263,71 |
|
2,79 |
57574,26 |
|
2,78 |
58915,34 |
|
2,77 |
60287,65 |
|
2,76 |
61691,93 |
|
2,75 |
63128,92 |
|
2,74 |
64599,38 |
|
2,73 |
66104,09 |
|
2,72 |
67643,86 |
|
2,71 |
69219,48 |
|
2,70 |
70831,81 |
|
2,69 |
72481,70 |
|
2,68 |
74170,01 |
|
2,67 |
75897,65 |
|
2,66 |
77665,54 |
|
2,65 |
79474,60 |
|
2,64 |
81325,80 |
|
2,63 |
83220,12 |
|
2,62 |
85158,57 |
|
2,61 |
87142,17 |
|
2,60 |
89171,97 |
|
2,59 |
91249,05 |
|
2,58 |
93374,51 |
|
2,57 |
95549,49 |
|
2,56 |
97775,12 |
|
2,55 |
100052,59 |
|
2,54 |
102383,12 |
|
2,53 |
104767,93 |
|
2,52 |
107208,29 |
|
2,51 |
109705,49 |
|
2,50 |
112260,86 |
|
2,49 |
114875,75 |
|
2,48 |
117551,55 |
|
2,47 |
120289,68 |
|
2,46 |
123091,50 |
|
2,45 |
125958,75 |
|
2,44 |
128892,71 |
|
2,43 |
131895,01 |
|
2,42 |
134967,24 |
|
2,41 |
138111,03 |
|
2,40 |
141328,05 |
|
2,39 |
144620,00 |
|
2,38 |
147988,63 |
|
2,37 |
151435,73 |
|
2,36 |
154963,12 |
|
2,35 |
158572,68 |
|
2,34 |
162266,31 |
|
2,33 |
166045,98 |
|
2,32 |
169913,68 |
|
2,31 |
173871,48 |
|
2,30 |
177921,47 |
|
2,29 |
182065,79 |
|
2,28 |
186306,65 |
|
2,27 |
190646,29 |
|
2,26 |
195087,01 |
|
2,25 |
199631,17 |
|
2,24 |
204281,18 |
|
2,23 |
209039,50 |
|
2,22 |
213908,65 |
|
2,21 |
218891,23 |
|
2,20 |
223989,86 |
|
2,19 |
229207,25 |
|
2,18 |
234546,17 |
|
2,17 |
240009,46 |
|
2,16 |
245599,99 |
|
2,15 |
251320,75 |
|
2,14 |
257174,77 |
|
2,13 |
263165,14 |
|
2,12 |
269295,04 |
|
2,11 |
275567,73 |
|
2,10 |
281986,52 |
|
2,09 |
288554,83 |
|
2,08 |
295276,14 |
|
2,07 |
302154,00 |
|
2,06 |
309192,07 |
|
2,05 |
316394,08 |
|
2,04 |
323763,85 |
|
2,03 |
331305,28 |
|
2,02 |
339022,37 |
|
2,01 |
346919,21 |
|
2,00 |
355000,00 |
|
1,99 |
363269,01 |
|
1,98 |
371730,63 |
|
1,97 |
380389,35 |
|
1,96 |
389249,76 |
|
1,95 |
398316,55 |
|
1,94 |
407594,54 |
|
1,93 |
417088,63 |
|
1,92 |
426803,87 |
|
1,91 |
436745,41 |
|
1,90 |
446918,52 |
|
1,89 |
457328,59 |
|
1,88 |
467981,14 |
|
1,87 |
478881,82 |
|
1,86 |
490036,41 |
|
1,85 |
501450,83 |
|
1,84 |
513131,12 |
|
1,83 |
525083,48 |
|
1,82 |
537314,24 |
|
1,81 |
549829,90 |
|
1,80 |
562637,08 |
|
1,79 |
575742,58 |
|
1,78 |
589153,35 |
|
1,77 |
602876,50 |
|
1,76 |
616919,29 |
|
1,75 |
631289,19 |
|
1,74 |
645993,80 |
|
1,73 |
661040,93 |
|
1,72 |
676438,55 |
|
1,71 |
692194,83 |
|
1,70 |
708318,12 |
|
1,69 |
724816,97 |
|
1,68 |
741700,13 |
|
1,67 |
758976,54 |
|
1,66 |
776655,38 |
|
1,65 |
794746,00 |
|
1,64 |
813258,02 |
|
1,63 |
832201,23 |
|
1,62 |
851585,69 |
|
1,61 |
871421,67 |
|
1,60 |
891719,68 |
|
1,59 |
912490,50 |
|
1,58 |
933745,14 |
|
1,57 |
955494,86 |
|
1,56 |
977751,19 |
|
1,55 |
1000525,94 |
|
1,54 |
1023831,18 |
|
1,53 |
1047679,28 |
|
1,52 |
1072082,86 |
|
1,51 |
1097054,88 |
|
1,50 |
1122608,57 |
|
1,49 |
1148757,48 |
|
1,48 |
1175515,48 |
|
1,47 |
1202896,75 |
|
1,46 |
1230915,82 |
|
1,45 |
1259587,53 |
|
1,44 |
1288927,09 |
|
1,43 |
1318950,06 |
|
1,42 |
1349672,36 |
|
1,41 |
1381110,26 |
|
1,40 |
1413280,46 |
|
1,39 |
1446199,99 |
|
1,38 |
1479886,31 |
|
1,37 |
1514357,29 |
|
1,36 |
1549631,20 |
|
1,35 |
1585726,75 |
|
1,34 |
1622663,07 |
|
1,33 |
1660459,75 |
|
1,32 |
1699136,83 |
|
1,31 |
1738714,81 |
|
1,30 |
1779214,68 |
|
1,29 |
1820657,91 |
|
1,28 |
1863066,48 |
|
1,27 |
1906462,88 |
|
1,26 |
1950870,10 |
|
1,25 |
1996311,70 |
|
1,24 |
2042811,78 |
|
1,23 |
2090394,98 |
|
1,22 |
2139086,53 |
|
1,21 |
2188912,26 |
|
1,20 |
2239898,57 |
|
1,19 |
2292072,51 |
|
1,18 |
2345461,74 |
|
1,17 |
2400094,56 |
|
1,16 |
2455999,95 |
|
1,15 |
2513207,53 |
|
1,14 |
2571747,66 |
|
1,13 |
2631651,36 |
|
1,12 |
2692950,39 |
|
1,11 |
2755677,26 |
|
1,10 |
2819865,23 |
|
1,09 |
2885548,33 |
|
1,08 |
2952761,39 |
|
1,07 |
3021540,04 |
|
1,06 |
3091920,74 |
|
1,05 |
3163940,83 |
|
1,04 |
3237638,48 |
|
1,03 |
3313052,77 |
|
1,02 |
3390223,68 |
|
1,01 |
3469192,13 |
|
1,00 |
3550000,00 |
9. ОБРАБОТКА РЕЗУЛЬТАТОВ ЭКСПЕРИМЕНТАЛЬНЫХ ИССЛЕДОВАНИЙ
ПРИ ОПРЕДЕЛЕНИИ СОДЕРЖАНИЯ ХЛОРИДОВ
9.1. Экспериментальные исследования проводятся для расчета погрешности определения содержания хлоридов в заданном диапазоне концентраций (3,55·10![]() -3,55·10
-3,55·10![]() ) мкг/дм
) мкг/дм![]() .
.
9.2. Доверительную вероятность при проведении экспериментальных исследований принимаем равной 0,8 (![]() =0,8).
=0,8).
9.3. Количество наблюдений (определений) ![]() содержания хлоридов для каждой концентрации определяют по формуле
содержания хлоридов для каждой концентрации определяют по формуле
![]() . (8)
. (8)
При ![]() =0,8
=0,8 ![]() 10.
10.
9.4. Оценку погрешности определения концентрации хлоридов проводят в такой последовательности:
9.4.1. Определяют систематическую составляющую погрешности по формуле
![]() мкг/дм
мкг/дм![]() , (9)
, (9)
где ![]() - значения концентрации хлоридов при
- значения концентрации хлоридов при ![]() -м определении;
-м определении;
![]() - действительное значение концентрации хлоридов.
- действительное значение концентрации хлоридов.
9.4.2. Определяют среднеквадратическое отклонение случайной составляющей погрешности по формуле
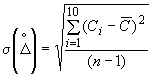 мкг/дм
мкг/дм![]() , (10)
, (10)
где ![]() - среднее значение результатов наблюдений (концентрации) содержания хлоридов, определяемое по формуле
- среднее значение результатов наблюдений (концентрации) содержания хлоридов, определяемое по формуле
![]() мкг/дм
мкг/дм![]() . (11)
. (11)
9.4.3. Определяют границы, в которых с вероятностью ![]() =0,8 находится погрешность определения концентрации по формуле
=0,8 находится погрешность определения концентрации по формуле
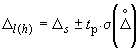 мкг/дм
мкг/дм![]() , (12)
, (12)
где ![]() - нижняя (верхняя) граница погрешности;
- нижняя (верхняя) граница погрешности;
![]() - коэффициент, зависящий от заданной вероятности и числа наблюдений: при
- коэффициент, зависящий от заданной вероятности и числа наблюдений: при ![]() =0,8 и
=0,8 и ![]() 10
10 ![]() 1,372.
1,372.
9.4.4. Находят границы, в которых с вероятностью ![]() =0,8 находится результат определения концентрации по формулам:
=0,8 находится результат определения концентрации по формулам:
![]() мкг/дм
мкг/дм![]() ;
;
(13)![]() мкг/дм
мкг/дм![]() ,
,
где ![]() - нижняя граница;
- нижняя граница;
![]() - верхняя граница.
- верхняя граница.
10. НОРМЫ ПОГРЕШНОСТИ.
ФОРМЫ ПРЕДСТАВЛЕНИЯ РЕЗУЛЬТАТОВ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ХЛОРИДОВ
10.1. В нормативно-технической документации не установлены нормы погрешности определения содержания хлоридов в электролите электролизных установок.
10.2. Результаты, согласно "Методическим указаниям. Государственная система обеспечения единства измерений. Результаты и характеристики погрешности измерений. Формы представления. Способы использования при испытаниях образцов продукции и контроле их параметров: МИ 1317-86". (М.: Издательство стандартов, 1986), представлены в следующей форме:
![]() ,
, ![]() ,
, ![]() .
.
10.3. Результаты определения содержания хлоридов для различных концентраций с доверительной вероятностью ![]() =0,8 находятся по табл.6.
=0,8 находятся по табл.6.
Таблица 6
Результаты определения содержания хлоридов для различных концентраций
|
Диапазон измерений, мкг/дм |
Результат определения, мкг/дм | |
|
|
Нижняя граница |
Верхняя граница |
|
3,55·10 |
|
|
|
Примечание. | ||
10.4. Пример определения концентрации хлоридов.
10.4.1. Показания иономера в анализируемом растворе ![]() =-218 мВ.
=-218 мВ.
10.4.2. По формуле (6) при ![]() =57 и
=57 и ![]() =-100 мВ получим
=-100 мВ получим ![]() =3,07.
=3,07.
10.4.3. По табл.5 находим ![]() =30215,4 мкг/дм
=30215,4 мкг/дм![]() .
.
10.4.4. Определяем нижнюю и верхнюю границы концентрации хлоридов по табл.6:
![]() =-83+0,95·30215,4=28621,6;
=-83+0,95·30215,4=28621,6;![]() =1,01·30215,4=30517,6.
=1,01·30215,4=30517,6.
Таким образом, результат определения концентрации хлоридов находится в границах от 28621,6 до 30517,6 мкг/дм![]() .
.
Текст документа сверен по:
Сборник методик по определению качества
электролита электролизных установок ТЭС
/ РАО "ЕЭС России". -
М.: СПО ОРГРЭС,1997