МУ 1.2.1105-02
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
1.2. ОБЩИЕ ВОПРОСЫ. ГИГИЕНА, ТОКСИКОЛОГИЯ, САНИТАРИЯ
Оценка токсичности и опасности дезинфицирующих средств
Дата введения: с момента утверждения
1. РАЗРАБОТАНЫ в НИИ дезинфектологии Министерства здравоохранения РФ авторским коллективом в составе: Шандала М.Г., Панкратова Г.П., Мальцева М.М., Заева Г.Н.
2. РЕКОМЕНДОВАНЫ к утверждению Бюро Комиссии по госсанэпиднормированию Минздрава России (протокол N 7 от 28 апреля 2001 г.).
3. УТВЕРЖДЕНЫ Главным государственным санитарным врачом Российской Федерации, Первым заместителем Министра здравоохранения Российской Федерации Г.Г.Онищенко 10 февраля 2002 г.
4. ВВЕДЕНЫ ВПЕРВЫЕ.
1. Область применения
1.1. Настоящие методические указания предназначены для токсикологов и гигиенистов, проводящих исследования дезинфицирующих средств (далее - ДС) разного назначения на степень токсичности и безопасности при их использовании с учетом назначения и условий применения.
1.2. На основании полученных результатов исследования на каждое ДС составляют методические указания по использованию их в практике лечебно-профилактических учреждений (далее - ЛПУ), организаций коммунального хозяйства, общественного питания, а также текст этикетки для ДС бытового назначения и разделы в инструкцию по применению ДС на предприятиях пищевой промышленности.
2. Общие требования к изучению токсичности
и опасности действующих веществ (ДВ)
2.1. Токсикологическая характеристика действующих веществ (далее - ДВ) или субстанций должна включать сведения по параметрам токсикометрии при различных путях поступления в организм с оценкой общетоксических, специфических и отдаленных эффектов:
- острой токсичности при введении в желудок (мыши, крысы) - ЛД![]() ;
;
- острой токсичности при нанесении на кожу - ЛД![]() ;
;
- острой токсичности при ингаляционном воздействии - ЛС![]() и порог острого действия (для субстанции, производящейся в России);
и порог острого действия (для субстанции, производящейся в России);
- клинических проявлений интоксикации;
- местно-раздражающего действия на кожу и слизистые оболочки глаз;
- подострой токсичности (кумулятивных свойств) для субстанций, производящихся в России;
- сенсибилизирующих свойств;
- хронической токсичности (с определением действующих, пороговых и неэффективных доз по лимитирующим показателям вредности);
- мутагенного эффекта по системе тестов;
- эмбриотропного действия;
- гонадотоксического действия и репродуктивной функции;
- онкогенности;
- метаболизма в организме млекопитающих;
- гигиенических нормативов - ПДК или ОБУВ в воздухе рабочей зоны, обеспечивающих безопасность работающих при производстве дезинфицирующих субстанций или самих ДС в России;
- гигиенических нормативов - ПДК (максимальная разовая и средне-суточная) или ОБУВ в атмосферном воздухе, обеспечивающих безопасность окружающей среды для субстанций и ДС, производимых в России [1, 2].
В полном объеме исследования должны проводиться для новых ДВ (субстанций), а для уже известных ДВ проводится сбор информации по вышеуказанным параметрам по данным литературы [3].
3. Общие требования к оценке токсичности и опасности
дезинфицирующих средств (ДС)
3.1. ДС имеют широкую сферу контакта с организмом как здорового, так и больного человека разного возраста, т.к. используются для неспецифической профилактики инфекционных заболеваний в лечебно-профилактических, детских, коммунальных учреждениях, на предприятиях общественного питания, в очагах инфекционных заболеваний, населением в быту, на предприятиях пищевой промышленности (пивобезалкогольной и винодельческой, мясомолочной, рыбоперерабатывающей, хлебопекарной и кондитерской), при обработке транспортных средств (санитарного транспорта, для перевозки пищевых продуктов).
3.2. Дезинфекционные мероприятия (профилактическая, текущая и заключительная дезинфекция) осуществляет профессиональная дезинфекционная служба, медицинский персонал ЛПУ, специально обученный персонал в других областях народного хозяйства и население в быту.
Профилактическая дезинфекция проводится постоянно, независимо от наличия инфекционного заболевания и имеет целью предупреждение возникновения и распространения инфекционных заболеваний на всех вышеуказанных объектах.
Текущая дезинфекция проводится постоянно в непосредственном окружении больного человека с целью предупреждения рассеивания возбудителей инфекционных заболеваний в окружающей среде. Основным способом обработки при этом виде дезинфекции является протирание различных поверхностей, а также погружение в дезинфицирующий раствор посуды, белья, игрушек, предметов по уходу за больными и т. д.
Заключительная дезинфекция проводится в инфекционном очаге однократно с целью предупреждения распространения возбудителей инфекционных заболеваний. В этом случае основными способами обработки являются - орошение и протирание различных поверхностей, погружение в дезинфицирующий раствор посуды, игрушек, замачивание белья и прочих предметов по уходу за больными.
Дезинфицирующие средства, сочетающие чистящие и моющие свойства, широко используются в быту населением и персоналом лечебно-профилактических учреждений для обработки и обеззараживания посуды и поверхностей санитарно-технического оборудования, предметов ухода за больными, а также для предстерилизационной очистки изделий медицинского назначения (далее - ИМН).
3.3. Для ДС используются в качестве ДВ химические вещества, принадлежащие к различным классам и группам химических соединений (хлорсодержащие, гуанидины, перекиси, поверхностно-активные вещества, йодсодержащие, надкислоты, альдегиды, фенолсодержащие и др.). Они характеризуются разнообразным действием на организм. Для придания ДС дополнительных свойств (моющих, чистящих, отбеливающих и др.) и усиления антимикробного действия создаются композиционные составы, включающие одно или несколько ДВ и вспомогательные ингредиенты (растворители, наполнители, синергисты, пеногасители, стабилизаторы, отдушки, красители и пр.).
3.4. Исходя из сказанного, следует, что изучение токсичности ДС будет определяться видом дезинфекции и вытекающими отсюда условиями их воздействия на человека (персонал или пациентов, в т.ч. больных в ЛПУ) с дифференцированными подходами к их изучению и требованиями по безопасности, принятыми в профессиональной и коммунальной сфере. В первом случае с возможностью использовать средства индивидуальной защиты (СИЗ), а для пациентов - регламентацией безопасных условий применения.
Безопасность должна быть обеспечена также установлением допустимых остаточных количеств ДС на обрабатываемых объектах (ИМН, посуде, белье, поверхностях) за счет отработки режимов их удаления.
Программа изучения ДС определяется конкретным его назначением, составом, видом и свойствами действующих веществ, режимами применения (нормой расхода, рабочими концентрациями, способами обработки), видами обрабатываемых объектов.
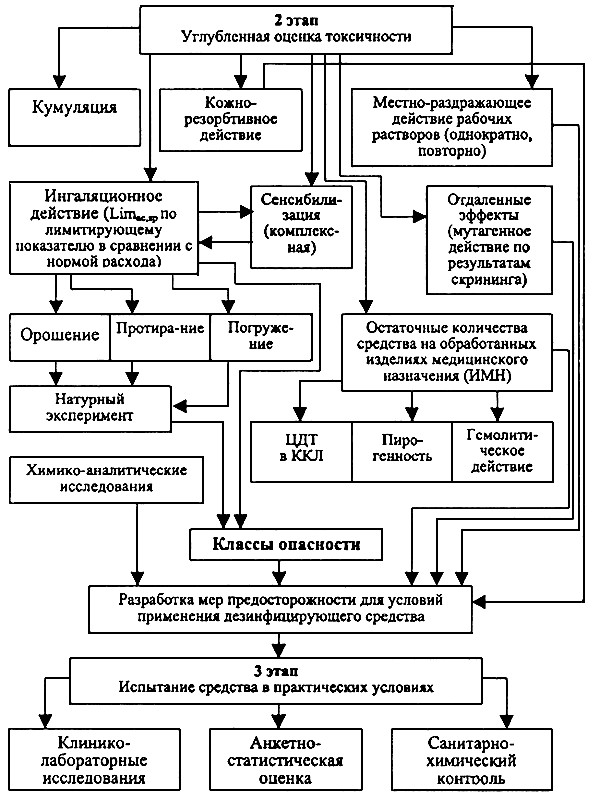
3.5. Изучение токсичности и опасности для всех регистрируемых ДС проводится по 3-этапной схеме (см. прилож.1):
1 этап включает первичную оценку токсичности и опасности ДС с определением лимитирующих параметров токсичности при потенциально опасных путях поступления в организм (в желудок, на кожу, на слизистые оболочки, через органы дыхания, парентерально) ускоренными методами в целях отбора ДС;
2 этап - это углубленные исследования токсичности ДС в острых и подострых экспериментах, исходя из режимов применения (нормы расхода, рабочих концентраций, способов обработки - протирание, орошение, погружение, замачивание, их кратности и экспозиции), с целью определения степени опасности.
3 этап - не обязателен и проводится для новых ДС, не имеющих аналогов, или для средств, требующих особых условий применения. Этот этап включает испытания ДС в практических условиях (в ЛПУ, очагах инфекционных заболеваний, на предприятиях и т.д.) с проверкой надежности и безопасности рекомендованных режимов применения и средств индивидуальной защиты (СИЗ) по анкетным данным о побочном действии, при необходимости проведение санитарно-химического анализа воздуха в помещениях по ведущим летучим компонентам средства. В пищевой промышленности проводится оценка смывов с оборудования на установление допустимых остаточных количеств дезинфицирующих средств.
3.6. Экспериментальные токсикологические исследования в зависимости от задач проводят на 3-4 видах лабораторных животных (крысы, мыши, кролики, морские свинки) обоего пола. Статистическая группа должна включать 6-8 особей мелких животных и не менее 3 для более крупных (кролики). Подопытные животные должны быть одной линии, вида, возраста, пола и весовых характеристик (масса мышей 18-22 г, крыс 180-200 г, морских свинок 200-300 г, кроликов 1,5-3 кг).
При отборе животных в эксперимент должен соблюдаться метод случайной выборки с отбраковкой больных и некондиционных животных.
Условия содержания и пищевой рацион животных должны быть стандартными и состоять из всех необходимых компонентов для нормальной жизнедеятельности (Приказ N 1179 от 10.10.83 "Об утверждении нормативов затрат кормов для лабораторных животных в учреждениях здравоохранения").
Перед экспериментом у животных необходимо снять фоновые данные по массе тела, показателям нервной системы (поведенческие реакции), и периферической крови (содержание лейкоцитов, эритроцитов и гемоглобин).
3.7. Полученные результаты экспериментов обрабатываются с применением статистических методов. Используют критерий "t" - Стьюдента, критерий "х![]() ", метод Кербера и пробит-анализа.
", метод Кербера и пробит-анализа.
3.8. Санитарно-химические исследования в токсикологических экспериментах проводят при анализе:
- воздуха на содержание ДВ дезинфектантов в затравочных камерах при моделировании условий и способов обработки (протирание, погружение, замачивание, орошение) или при проведении натурного эксперимента, соблюдая рекомендуемые условия, способы и нормы расхода;
- смывов с посуды, ИМН и других обработанных объектов.
При этом, соблюдается правило, когда химико-аналитические методы определения содержания ДВ в воздухе или смывах с обрабатываемых объектов должны отвечать требованиям соответствующих ГОСТ и утвержденным в установленном порядке методическим указаниям.
4. Первый этап изучения токсичности и опасности дезинфицирующих средств
4.1. Сбор информации по токсичности и опасности по данным литературы согласно вышеуказанным параметрам токсичности проводится по каждому ДВ и по всем компонентам, входящим в ДС (состав средства), с учетом физико-химических свойств (молекулярной массы, летучести, рН, растворимости, степени чистоты) и существующих гигиенических нормативов в различных средах. Пути поступления в организм ДС определяются его назначением (обработка поверхностей, предметов ухода за больными, изделий медицинского назначения, посуды, белья, игрушек, санитарно-технического оборудования и т.д.).
4.2. Определение средне-смертельной дозы (ЛД![]() ) проводят при разных путях поступления в организм ДС в острых опытах [4].
) проводят при разных путях поступления в организм ДС в острых опытах [4].
- При внутрижелудочном пути используют 4-6 доз в геометрической прогрессии, но не менее 3. Максимально вводимый объем мышам - 1 мл, крысам и морским свинкам - 5 мл.
- При введении в брюшную полость, под кожу или в кровеносные сосуды интервал между дозами составляет 10-20 мг/кг или в геометрической прогрессии от минимальной дозы. Максимальный объем для мышей составляет - 0,5 мл, для крыс - 1-1,5 мл, для кроликов - 10 мл на килограмм массы тела.
- При нанесении на кожу используют нативный ДС и в разведении. Исследуемое ДС наносят в строго дозированных количествах из расчета на 1 кг массы тела и 1 см![]() поверхности кожи (у мышей площадь на спине составляет 2х2 см, для крыс - 4х4 см, время экспозиции 2 и 4 ч соответственно). Животных помещают в специальные домики.
поверхности кожи (у мышей площадь на спине составляет 2х2 см, для крыс - 4х4 см, время экспозиции 2 и 4 ч соответственно). Животных помещают в специальные домики.
Срок наблюдения за животными - до 3 недель.
Допускается определение ЛД![]() ускоренным методом "одной точки" по Ван Дер Вардену при условии экспертной оценки известных соединений или композиций.
ускоренным методом "одной точки" по Ван Дер Вардену при условии экспертной оценки известных соединений или композиций.
В ходе опыта регистрируются клинические признаки отравления животных, сроки гибели и макроморфологические изменения в органах при вскрытии погибших животных.
Результаты изучения острой токсичности оценивают по 4 классам опасности согласно классификации по ГОСТ 12.1.007-76 для внутрижелудочного введения и нанесении на кожу (см. прилож.2).
Для парентерального введения (под кожу или в брюшную полость) полученные результаты оценивают по классификации К.К.Сидорова (см. прилож.3).
4.3. Местно-раздражающее действие на кожу оценивают на кроликах или морских свинках с однократным и многократным (повторным) воздействием (10-12 аппликаций). Животные отбираются со светлой кожей. Шерсть стригут накануне нанесения, избегая порезов и ссадин. Площадь нанесения для кроликов 8х9 см, для морских свинок 4х5 см. Дезинфицирующее средство наносят как в нативном виде, так и в разведениях с определением порога острого раздражающего действия (Lim![]() ). Время экспозиции составляет до 2 ч. В конце эксперимента ДС смывается (см. прилож.4 и 4-а - форма протоколов опытов). Реакция кожи регистрируется сразу после окончания экспозиции и далее ежедневно в течение 14 дней наблюдений (см. прилож.5). Отмечают функционально-морфологические нарушения кожи (эритема, отек, трещины, изъязвления, некроз, сухость, шелушение и др.).
). Время экспозиции составляет до 2 ч. В конце эксперимента ДС смывается (см. прилож.4 и 4-а - форма протоколов опытов). Реакция кожи регистрируется сразу после окончания экспозиции и далее ежедневно в течение 14 дней наблюдений (см. прилож.5). Отмечают функционально-морфологические нарушения кожи (эритема, отек, трещины, изъязвления, некроз, сухость, шелушение и др.).
Оценка эритемы проводится в баллах согласно общепринятой классификации С.В.Суворова.
Объективным методом оценки отека кожи служит измерение толщины кожной складки (в мм) при помощи инженерного микрометра и переводится в баллы. Баллы суммируются для каждого подопытного животного, после чего вычисляется средний суммарный балл для данной группы экспериментальных животных [5].
Выраженность местно-раздражающего действия испытуемого ДС при однократной аппликации на кожу оценивается в соответствии с классификацией, разработанной для ДС (табл.1).
Таблица 1
Классификация опасности по выраженности местно-раздражающих свойств дезинфицирующих средств на коже
|
Выраженность раздражающего действия |
Средний суммарный балл выраженности эритемы и величины отека |
Классы опасности |
|
Резко выраженное |
более 6 |
1 |
|
Выраженное |
4,1-6,0 |
2 |
|
Умеренное |
2,1-4,0 |
3 |
|
Слабое или отсутствие |
0-2,0 |
4 |
За порог раздражающего действия ДС на кожу принимается его минимальное разбавление, вызывающее минимальный эффект у животных (определяют для веществ, относящихся к 1-3 классам по степени выраженности раздражающего действия на кожу). Регистрируется также минимальное разбавление вещества, не вызывающее раздражения кожи.
4.4. Местно-раздражающее действие на глаза ДС оценивают на кроликах (статистическая группа 3) или морских свинках (статистическая группа 6). Отмечают выраженность гиперемии и отека конъюнктивы, инъекцию сосудов склеры, состояние роговицы и радужной оболочки, количество и качество выделений из глаза (см. прилож.6 и табл.2).
Таблица 2
Оценка интенсивности местно-раздражающего действия средства на глаза
|
|
Покраснение (века) и бульбарная конъюнктива (не затрагивающая роговицу и радужную оболочку) |
Оценка (баллы) |
|
|
Состояние сосудов нормальное |
0 |
|
А |
Сосуды явно расширены больше нормы |
1 |
|
|
Разлитая гиперемия, отдельные сосуды трудноразличимы |
2 |
|
|
Дуффузная, ярко красного цвета гиперемия |
3 |
|
|
Отек век |
|
|
|
Отека нет |
0 |
|
|
Слабый отек (включая мигательную перепонку) |
1 |
|
Б |
Явный отек и частичное выворачивание века |
2 |
|
|
Отек, веки наполовину закрылись |
3 |
|
|
Отек, веки закрыты более чем наполовину или полностью закрылись |
4 |
|
|
Выделения |
|
|
|
Выделений нет |
0 |
|
|
Минимальное количество в углу глазной щели |
1 |
|
В |
Количество выделений с увлажнением век и шерсти, прилегающей к векам |
2 |
|
|
Количество выделений с увлажнением век и шерсти и значительной площади вокруг глаз |
3 |
|
|
Сумма баллов (А+Б+В) | |
|
Роговица | ||
|
|
Помутнение - степень плотности (участок наибольшей плотности) |
Оценка (баллы) |
|
|
Помутнения нет |
0 |
|
А |
Рассеянное или диффузное, детали радужной оболочки хорошо видны |
1 |
|
|
Хорошо различимые полупрозрачные участки, детали радужной оболочки слегка замутнены |
2 |
|
|
Участок с замутнением, детали радужной оболочки не видны, размер зрачка едва различим |
3 |
|
|
Непрозрачная, радужная оболочка не видна |
4 |
|
|
Площадь поражения роговицы |
|
|
|
Одна четверть (или менее), но более нуля |
1 |
|
Б |
Более одной четверти, но менее половины |
2 |
|
|
Более половины, но менее трех четвертей |
3 |
|
|
Более трек четвертей, но менее всей площади |
4 |
|
|
Сумма баллов (А+Б) | |
Результаты обследования каждого животного суммируются, и выносится заключение о степени и характере поражения глаз при действии на него изучаемого соединения или средства. Указывается характер конъюнктивита (поверхностный, глубокий), наличие кератита. Класс по раздражающему действию ДС оценивается по классификации выраженности раздражающих свойств (табл.3).
Таблица 3
Классификация по выраженности раздражающих свойств дезинфицирующих средств на глаза
|
Выраженность раздражающего действия |
Средний суммарный балл (конъюнктива (А+Б+В) + роговица (А+Б) |
Классы |
|
Резко выраженное |
более 11 |
1 |
|
Выраженное |
7-10 |
2 |
|
Умеренное |
4-6 |
3 |
|
Слабое |
1-3 |
4 |
|
Отсутствие |
0 |
5 |
4.5. Оценка ингаляционной опасности ДС проводится в насыщающих концентрациях в герметичных емкостях (типа эксикатора), в котором создаются условия свободного испарения летучих компонентов средства при комнатной температуре в течение суток или более, в зависимости от их свойств. Опыты ставят на мышах или на крысах статическим методом из расчета объема воздуха на одно животное в час: для мышей - 2 л, для крыс - 5-7 л. Экспозиция составляет 2-4 ч. В ходе эксперимента регистрируются клинические признаки отравления и время их появления, а также гибель животных. После окончания воздействия животных целесообразно обследовать по показателям общетоксического или специфического действия. Опасность ингаляционного отравления характеризуется степенью проявления интоксикации (табл.4).
Таблица 4
Классификация химических веществ по степени летучести (С![]() )
)
|
Класс опасности |
Степень опасности и выраженность действия |
|
1 - чрезвычайно опасное вещество |
Насыщающая концентрация вызывает гибель |
|
2 - высоко опасное |
Насыщающая концентрация вызывает отчетливые проявления интоксикации, гибель отсутствует |
|
3 - умеренно опасное |
Насыщающая концентрация вызывает минимальные изменения интегральных показателей при обследовании животных (пороговый уровень) |
|
4 - малоопасное |
Насыщающая концентрация не оказывает токсического действия |
4.6. Сенсибилизирующие свойства ДС определяют комплексом методов.
- Методом Алексеевой-Петкевич на морских свинках при внутрикожном введении 50-200 мкг ДС с последующими (через 10 дней) накожными аппликациями и постановкой проб (кожной и конъюнктивальной) и аллергологических тестов с клетками крови по выбору согласно методическим указаниям, 1993-1997 гг. [6, 7].
- По реакции гиперчувствительности "замедленного" типа (ГЗТ) на мышах массой 20 ± 0,5 г при внутрикожной сенсибилизации ДС в ПАФ (полном адъюванте Фрейнда) проводят согласно методическим указаниям, 1992 г. [4]. Индекс реакции (ИР) вычисляют по формуле:
![]() , где
, где
![]() и
и ![]() - объем (масса) стопы в опыте и контроле соответственно, мм (мг).
- объем (масса) стопы в опыте и контроле соответственно, мм (мг).
Достоверным считают значения ИР более 5%.
Силу аллергенной активности оценивают по классификации для химических веществ (см. прилож.7) [6, 7].
4.7. Мутагенный эффект ДС оценивают по показаниям ускоренными методами: микроядерным на ретикулоцитах костного мозга, в тесте Эймса или на дрозофиле согласно методическим рекомендациям [8, 9].
5. Критерии отбора дезинфицирующих средств после первичной оценки токсичности и опасности
5.1. В состав ДС не должны входить действующие субстанции, обладающие отдаленными эффектами (мутагенный, канцерогенный, эмбриотропный, гонадотоксический и тератогенный) и относящиеся по гигиенической классификации пестицидов к 1 и 2 классу опасности [10].
5.2. Не подлежат дальнейшему изучению ДС, по параметрам острой токсичности относящиеся к 1 классу опасности по ГОСТ 12.1.007-76 (при введении в желудок и нанесении на кожу), к 1 и 2 классам токсичности по классификации К.К.Сидорова (при введении под кожу или в брюшную полость), к 1 классу опасности по классификации химических веществ по степени летучести (С![]() ) (при ингаляции в насыщающих концентрациях (пары) [11-13].
) (при ингаляции в насыщающих концентрациях (пары) [11-13].
5.3. Не рекомендуются для дальнейшего изучения ДС, обладающие выраженным кожно-резорбтивным действием и сильным аллергенным эффектом (1 класс опасности) [6].
5.4. Остальные ДС могут быть рассмотрены дифференцированно для использования в разных областях и сферах применения (для использования в медицинской дезинфекции, на объектах коммунального хозяйства, общественного питания, в детских учреждениях, на объектах пищевой промышленности, в быту населением) и могут быть рекомендованы для углубленного изучения с учетом рабочих концентраций, условий и режимов применения.
6. Второй этап оценки токсичности и опасности
дезинфицирующих средств с учетом сферы применения
6.1. Цель этих исследований - дать токсикологическую характеристику ДС и оценить реальную степень опасности в соответствии с режимами использования и рекомендовать безопасные условия его применения в практике.
6.2. В зависимости от способа обработки ДС оказывают на персонал, проводящий дезинфекцию, ингаляционное воздействие в виде аэрозолей или аэрозолей и паров или только паров.
Аэрозольная форма создается при орошении поверхностей растворами ДС. При этом используется различная разрешенная для этих целей аппаратура (гидропульт, дезинфаль, автомакс, распылители типа "Росинка" и др.). Необходимо учитывать дисперсность аэрозольных частиц, величину орошаемого факела.
Пары средства в воздухе образуются при использовании способа "протирания", "погружения" или "замачивания".
6.3. Оценку ингаляционной опасности рабочих концентраций ДС или готового к употреблению ДС проводят в затравочных камерах, моделируя в статических условиях способы применения (орошение, протирание, замачивание или погружение) с учетом режимов применения (нормы расхода, экспозиции).
Как показал опыт работы с дезинфектантами, лимитирующими эффектами для них являются - раздражающий, состояние нервной системы, аллергические реакции. На основании проведенных исследований определяют пороги острого и подострого действия (Lim![]() и Lim
и Lim![]() ) по лимитирующему показателю и рассчитывают зону острого токсического действия по отношению порога острого действия к норме расхода (Lim
) по лимитирующему показателю и рассчитывают зону острого токсического действия по отношению порога острого действия к норме расхода (Lim![]() /норма расхода) или зону подострого - по отношению порога подострого действия к норме расхода (Lim
/норма расхода) или зону подострого - по отношению порога подострого действия к норме расхода (Lim![]() / норма расхода).
/ норма расхода).
6.4. При моделировании способа протирания или орошения в затравочной камере обрабатывают все боковые поверхности и пол в рекомендуемой рабочей концентрации с учетом нормы расхода. В острых опытах обработки проводятся однократно, а в подострых опытах - ежедневно 5 раз в неделю, на протяжении всего эксперимента (от 2 до 4 недель).
При моделировании способа погружения или замачивания в затравочную камеру объемом 1 м![]() помещают открытую емкость с площадью открытой поверхности 0,1 м
помещают открытую емкость с площадью открытой поверхности 0,1 м![]() (что составляет 10% от площади затравочной камеры) с налитым в нее рабочим раствором ДС.
(что составляет 10% от площади затравочной камеры) с налитым в нее рабочим раствором ДС.
В затравочных камерах контролируют температуру и влажность воздуха, определяют содержание летучих действующих веществ ДС.
6.5. В зависимости от вида дезинфекционных мероприятий проводится дифференцированная оценка безопасности для персонала и пациентов:
- при заключительной дезинфекции, дезинфекции в очагах инфекционных заболеваний, на предприятиях пищевой промышленности - безопасность для персонала обеспечивается соблюдением гигиенических нормативов летучих ДВ дезинфицирующих средств в воздухе рабочей зоны (ПДК или ОБУВ);
- при текущей и профилактической дезинфекции - безопасность для пациентов и персонала обеспечивается соблюдением общего гигиенического норматива летучего ДВ в атмосферном воздухе (ПДК, ОБУВ - максимальная разовая).
6.6. После проведенных лабораторных исследований по оценке опасности при ингаляционном воздействии (аэрозоль + пары или пары) проводят натурный эксперимент в помещении, моделирующим больничные палаты или другие помещения (например, туалетные и ванные комнаты). Обработка проводится в соответствии с рекомендуемыми режимами (протирание или орошение) и нормами расхода. Воздух контролируют по содержанию индикаторного летучего ДВ средства в сравнении с его гигиеническим нормативом в воздухе рабочей зоны и максимально разовой концентрацией в атмосферном воздухе. После окончания воздействия проводится проветривание (естественное) до достижения гигиенического норматива в атмосферном воздухе и рекомендуется режим проветривания.
При проведении натурного эксперимента по отработке режима проветривания можно привлекать добровольцев с регистрацией в анкете субъективных ощущений или жалоб.
6.7. Оценку ингаляционной опасности при однократном воздействии проводят по зоне острого токсического действия согласно степени ингаляционной опасности ДС (табл.5), разрабатывают меры предосторожности и рекомендуют соответствующие средства индивидуальной защиты.
Таблица 5
Классификация степени ингаляционной опасности дезинфицирующих средств
|
Класс опасности |
Зона острого токсического действия: отношение порога острого действия (Lim |
Рекомендуемые условия применения |
|
1 - высокоопасно |
менее 1 |
Использовать в экстремальных ситуациях (по эпидемиологическим показаниям) в специальных костюмах и противогазах |
|
2 - опасно |
1-3 |
Использовать в ЛПУ со средствами защиты органов дыхания, глаз, кожи, в отсутствие больных и пациентов |
|
3 - умеренно опасно |
3,1-10 |
Использовать в ЛПУ без средств защиты органов дыхания и глаз, но в отсутствие больных и пациентов |
|
4 - малоопасно |
более 10 |
Использовать в присутствии больных, пациентов и в быту |
6.8. Оценку степени ингаляционной опасности ДС при подостром воздействии проводят по зоне подострого действия (при Z![]() менее 10 не рекомендуется использовать в присутствии больных. при Z
менее 10 не рекомендуется использовать в присутствии больных. при Z![]() более 10 можно использовать в присутствии больных).
более 10 можно использовать в присутствии больных).
6.9. Для ДС, в состав которых входят нелетучие соединения, не требуется проведение экспериментов с оценкой способов обработки протиранием, погружением и замачиванием. Для них достаточна оценка ингаляционной опасности в условиях насыщающих концентраций.
6.10. В том случае, когда средство рекомендуется использовать способом орошения, следует проводить исследования, как указано выше.
6.11. Исследование кумулятивных свойств необходимо для характеристики ДС при обработке посуды и игрушек. Используют метод Лима. Исследования проводят в течение 24±4 дней. В первые 4 дня вводят в желудок 0,1 ЛД![]() , увеличивая дозы каждые 4 дня в полтора раза. Коэффициент кумуляции рассчитывают по формуле: ЛД
, увеличивая дозы каждые 4 дня в полтора раза. Коэффициент кумуляции рассчитывают по формуле: ЛД![]() /ЛД
/ЛД![]() - Если К
- Если К![]() <1, это указывает на кумулятивные свойства средства, а если К
<1, это указывает на кумулятивные свойства средства, а если К![]() >1 - на повышение резистентности организма на это соединение. Для ДС, обладающих кумулятивными свойствами, необходимо определять остаточные количества ДС на обрабатываемых объектах и отрабатывать режим отмыва от данного ДС [1].
>1 - на повышение резистентности организма на это соединение. Для ДС, обладающих кумулятивными свойствами, необходимо определять остаточные количества ДС на обрабатываемых объектах и отрабатывать режим отмыва от данного ДС [1].
6.12. Местно-раздражающее действие рабочих концентраций ДС исследуют на кроликах или морских свинках при однократных и повторных аппликациях в течение 14 дней. Состояние кожи регистрируется ежедневно по наличию эритемы, отека, трещин, некроза, шелушения, сухости (см. п.4.3 и прилож.7). При появлении первых признаков аппликации прекращают. Кожно-резорбтивное действие в этом случае не изучается.
6.13. При отсутствии местно-раздражающего эффекта проводят изучение кожно-резорбтивного действия рабочих растворов ДС на мышах или крысах методом погружения хвостов в изучаемый раствор. Ежедневно животные, помещенные в специальные домики, подвергаются воздействию различных концентраций препарата, который налит в пробирки. Хвосты животных погружают на 2/3 длины в раствор на время от 2 до 4 ч (в зависимости от вида животных - соответственно мыши и крысы) на протяжении 14 дней. Животных обследуют каждые 7 дней по различным показателям, характеризующим состояние основных органов и систем (нервной системы, печени, почек, сердечно-сосудистой системы и периферической крови). Целесообразно использование дополнительных специфических показателей, характерных для данного ДС.
Если в этот срок не выявлено резорбтивного эффекта ДС, то дальнейшие исследования прекращают.
6.14. Местно-раздражающее действие рабочих концентраций ДС на глаза проводят и оценивают, как в п.4.4.
6.15. Для оценки безопасного использования столовой посуды после обработки ДС проводят исследования его остаточных количеств на поверхности. Для эксперимента используют комплект, состоящий из тарелок (глубокой и мелкой), стакана или чашки, ложки и вилки. Посуду погружают в дезинфицирующий раствор и выдерживают экспозицию согласно рекомендованному режиму по ее обеззараживанию. Затем ДС смывают и на посуде определяют остаточные количества ДС (по наиболее токсичному ДВ) химико-аналитическим методом. Отрабатывают режимы отмыва посуды от ДС (под проточной водой или путем кратного погружения в емкости с питьевой водой) [14].
Полученные результаты сопоставляют с ПДК для ДВ и воде водных объектов хозяйственно-питьевого и культурно-бытового водопользования. При этом учитывают, что только половина поверхности комплекта контактирует с потребляемой пищей. Смывы с посуды оценивают по местно-раздражающему действию на слизистые оболочки глаз и цитотоксическому действию в культуре клеток, МУ, 1990-1996 гг. (табл.6). На основании полученных данных разрабатывается режим отмыва посуды [15].
Таблица 6
Оценка цитотоксичности дезинфицирующих и стерилизующих средств в ККЛ (прямой контактный тест) на примере перекиси водорода
|
|
Реакция клеток в культуре** | |||
|
Концентрация раствора Н |
Степень ЦТД* |
по Фармакопее США |
| |
|
|
|
Степень ЦТД |
Реакция клеток |
|
|
0,3% |
++++ |
4 |
тяжелая |
100%-ная деструкция клеточного монослоя |
|
0,15% |
+++ |
3 |
умеренная |
70-75% клеточного монослоя содержат округлые и/или лизированные клетки |
|
0,03 % |
++ |
2 |
мягкая |
50% гибели клеток |
|
0,015% |
+ |
1 |
слабая |
20-25% лизированных клеток |
|
0,007% |
0 |
0 |
нет |
Отсутствие ЦТД |
|
Контроль наличия ЦТД - мертиолят - 1:10000 |
++++ |
4 |
тяжелая |
100%-ная деструкция клеточного монослоя |
|
Контроль отсутствия ЦТД - 0,9%-ный раствор хлористого натрия |
0 |
0 |
нет |
Отсутствие ЦТД |
|
Интактная ККЛ |
0 |
0 |
нет |
Отсутствие ЦТД |
|
_______________ | ||||
|
** Образец удовлетворяет требованиям безопасности, если ни одна из опытных клеточных культур не имеет степень более 1. | ||||
6.16. Безопасность остаточных количеств ДС на ИМН оценивают комплексом методов: пирогенность, цитотоксическое действие (далее - ЦТД) в культуре клеток (далее - ККЛ), гемолитическое действие. Проводится отработка режима отмыва ИМН от ДС [15-20].
Оценку смываемости ДС проводят с ИМН из разных материалов (металлов, стекла, резин натуральных и силиконовых, пластмасс). Режим отмыва ИМН осуществляют под проточной водой или при кратном погружении в дистиллированную воду. Остаточные количества (вытяжку или смывы) ДС с изделий получают дистиллированной водой при соотношении объема изделий к объему воды 1:1. Приготовление вытяжек или смывов проводится (в термостате) при температуре 37 °С в течение 24 ч. В полученные вытяжки или смывы добавляют хлористый натрий и используют при оценке пирогенности [17], гемолитического действия [18, 19] и ЦТД в культуре клеток (диплоидные клетки человека - ДКЧ и клетки почек зеленых мартышек - ПЗМ-4647) [15-17].
Вытяжки или смывы вносят в культуру клеток на 30 мин, затем раствор сливают и клетки промывают. В качестве отрицательного контроля берут клетки с питательной средой и клетки при воздействии физиологического раствора, приготовленного на воде, используемой для получения вытяжки. В качестве положительного контроля берут клетки после воздействия раствором мертиолята (1:10000). Результаты оценивают по ЦТД (см. табл.6).
6.17. Сенсибилизирующее действие (см. п.4.6).
При положительных результатах на первом этапе оценку аллергенного действия ДС проводят при комплексном поступлении аллергена в организм (через органы дыхания и кожу). Для этого используются эксперименты, описанные в п.6.4 при повторных ингаляционных воздействиях рабочих растворов ДС. Тестирование проводят на 14 и 28 сутки от начала воздействия, используя конъюнктивальную пробу как более чувствительную при ингаляционном пути поступления в организм и 2-3 иммунологических теста. Определяют Lim![]() , который учитывают при определении зоны подострого токсического действия.
, который учитывают при определении зоны подострого токсического действия.
При кожном пути поступления средств в организм, исследования проводят на морских свинках при повторных 4-недельных кожных аппликациях ДС в концентрации, не вызывающей местно-раздражающего действия. Тестирование проводят, как указано выше, добавляя кожную пробу. При оценке результатов учитывают развитие сенсибилизации даже у единичных животных в группе (см. прилож.6) [6, 7].
6.18. Для полной характеристики ДС на основе литературных данных дается токсикологическая характеристика компонентов состава средства (это вспомогательные компоненты-наполнители, стабилизаторы, антикоррозионные, отдушки, красители и т.д.).
6.19. На основании проведенных исследований разрабатываются рекомендации по мерам предосторожности при работе со средством и его хранении, а также меры первой помощи при случайном отравлении.
7. Критерии отбора дезинфицирующих средств, предназначенных для ЛПУ
7.1. Острое ингаляционное действие ДС (аэрозоли + пары или пары) оценивают по зоне острого токсического действия (табл.5).
- При зоне острого токсического действия менее 1, ДС следует отнести к 1 классу высоко опасных средств и использовать только в экстремальных чрезвычайных эпидемиологических ситуациях обученному персоналу с применением жестких средств индивидуальной защиты (противогаз, противочумный костюм).
- При зоне острого токсического действия, равной от 1 до 3, ДС следует отнести ко 2 классу опасных средств и использовать в ЛПУ при заключительной дезинфекции с обязательным применением индивидуальных средств защиты органов дыхания, кожных покровов и глаз в отсутствие пациентов.
- При зоне острого токсического действия, равной от 3 до 10, ДС следует отнести к 3 классу умеренно опасных и использовать в ЛПУ в отсутствие больных или пациентов. Персоналу рекомендуется работать без средств защиты органов дыхания и глаз, но избегать попадания средства в глаза и на кожные покровы.
- При зоне острого токсического действия более 10 ДС следует отнести к 4 классу малоопасных средств и рекомендовать для использования в присутствии пациентов.
7.2. Ингаляционную опасность при повторном воздействии ДС (аэрозоли + пары или пары) оценивают по зоне подострого токсического действия: при Z![]() менее 10 не рекомендуется использовать в присутствии пациентов, при Z
менее 10 не рекомендуется использовать в присутствии пациентов, при Z![]() более 10 можно использовать в присутствии пациентов.
более 10 можно использовать в присутствии пациентов.
7.3. Дезинфицирующие средства, обладающие кожно-резорбтивным и местно-раздражающим действием в рабочих концентрациях (2-3 класс опасности) должны использоваться строго с защитой кожи рук и глаз.
7.4. Дезинфицирующие средства с высокими кумулятивными свойствами контролируют химико-аналитическим методом при отмыве с посуды и игрушек, которые оценивают с учетом ПДК для ДВ в питьевой воде для изучаемого ДС.
7.5. Дезинфицирующие средства, обладающие умеренной сенсибилизацией (2 класс опасности) (прилож.6), рекомендуются для использования в ЛПУ обученным персоналом строго со средствами защиты в отсутствие людей (в очагах) и больных, с последующей уборкой и проветриванием помещений.
Дезинфицирующие средства, обладающие слабым сенсибилизирующим действием (3 класс опасности), рекомендуются для дезинфекции в ЛПУ с соблюдением мер предосторожности.
К работе с такими ДС не допускается персонал с аллергическими заболеваниями и повышенной чувствительностью к химическим веществам.
Дезинфицирующие средства, не обладающие сенсибилизирующим действием, могут широко использоваться в ЛПУ.
7.6. Режим отмыва ИМН от ДС удовлетворяет требованиям безопасного использования, если вытяжки или смывы:
- не оказывают ЦТД в ККЛ, и ни одна из опытных клеточных культур не имеет степень более 1;
- по пирогенности не вызывают эффекта;
- вызывают гемолитическое действие, не превышающее 2%.
7.7. На основании полученных данных составляют разделы в методические указания по применению ДС в ЛПУ с характеристикой его по токсичности и опасности, разработкой необходимых мер предосторожности с рекомендациями мер индивидуальной защиты, а также мер первой помощи при случайном отравлении. Меры предосторожности при работе и хранении средства, а также режимы удаления его с поверхности различных ИМН после обработки.
8. Параметры токсикометрии при оценке токсичности и опасности дезинфицирующих средств, предназначенных для дезинфекции в быту (обработка поверхностей, посуды, белья, санитарно-технического оборудования, предметов ухода за больными)
8.1. Токсикологическая характеристика по литературным данным всех компонентов состава средства (вспомогательные компоненты: наполнители, стабилизаторы, антикоррозионные, отдушки, красители и т.д.).
8.2. Острая токсичность при введении в желудок (мыши, крысы) - ЛД![]() , мг/кг (см. п.4.1).
, мг/кг (см. п.4.1).
8.3. Острая кожная токсичность - ЛД![]() , мг/кг (см. п.4.1).
, мг/кг (см. п.4.1).
8.4. Острая ингаляционная токсичность - СЛ![]() ингаляционная опасность в насыщающих концентрациях по степени летучести (см. п.4.5).
ингаляционная опасность в насыщающих концентрациях по степени летучести (см. п.4.5).
8.5. Клинические проявления острой интоксикации.
8.6. Местно-раздражающее действие на кожу рабочих концентраций (однократно) (см. п.4.3).
8.7. Подострая накожная токсичность (местно-раздражающее действие рабочих концентраций на кожу повторно) (см. п.6.10).
8.8. Местно-раздражающее действие на глаза (нативного средства и рабочих концентраций) (см. п.4.4).
8.9. Кожно-резорбтивное действие рабочих концентраций (см. п.6.11).
8.10. Кумулятивные свойства (см. п.6.9).
8.11. Сенсибилизирующее действие (см. п.4.6).
8.12. Ингаляционная опасность в режимах применения: протирание, погружение (см. пп.6.3-6.8).
8.13. Оценка безопасности остаточных количеств средства на посуде и игрушках (см. п.6.13).
8.14. Рекомендации по мерам предосторожности при работе и хранении средства, текст этикетки.
Критерии отбора дезинфицирующих средств,
используемых в быту
- Могут быть рекомендованы для использования в быту населением с соблюдением необходимых мер предосторожности ДС, относящиеся к 3 и 4 классу опасности при разных путях (в желудок, на кожу) поступления в организм, с отсутствием или слабо выраженными местно-раздражающим и сенсибилизирующими действиями.
- Ингаляционная опасность ДС (аэрозоль или аэрозоль + пары) оценивается по зоне острого и подострого токсического действия. Рекомендуются ДС с зоной токсического действия более 10 и относящиеся к 4 классу опасности.
- Рекомендуются ДС, не обладающие кумулятивными свойствами.
- Составляется этикетка по применению ДС с обоснованием необходимых мер предосторожности.
9. Параметры токсикометрии при оценке токсичности и опасности дезинфицирующих средств, предназначенных для обработки поверхностей помещений, технологического оборудования, тары на предприятиях в пищевой промышленности (пивобезалкогольная и винодельческая, мясомолочная, хлебопекарная, кондитерская, сыроварения, рыбоперерабатывающая)
9.1. Сбор данных литературы о токсичности изучаемого средства по общей токсичности, метаболизму в организме, отдаленным проявлениям, экологической безопасности.
9.2. ЛД![]() при введении:
при введении:
- в желудок, мг/кг;
- на кожу, мг/кг (см. п.4.1).
9.3. Ингаляция:
- в насыщающих концентрациях (пары) по степени летучести (см. п.4.5);
- в форме аэрозоля (см. пп.6 2-6.8).
9.4. Кумуляция (см. п.6.9).
9.5. Местно-раздражающее действие на кожу (см. п.4.3, 6.10):
- нативный препарат;
- рабочие растворы.
9.6. Местно-раздражающее действие на глаза (см. п.4.4, 6.12):
- нативный препарат;
- рабочие растворы.
9.7. Кожно-резорбтивное действие рабочих растворов (см. п.6.11).
9.8. Сенсибилизация:
- ГЗТ;
- кожные аппликации (см. п.4.6., 6.15).
9.9. Безопасность остаточных количеств ДС на оборудовании (п.6.13, 6.14).
9.10. Обоснование мер предосторожностей и средств индивидуальной защиты с учетом условий применения, меры первой помощи при случайном отравлении средством, условия хранения.
Критерии отбора дезинфицирующих средств,
предназначенных для предприятий пищевой промышленности
Не допускаются ДС:
- содержащие отдушки;
- относящиеся к 1 классу опасности при потенциально опасных путях поступления в организм (через рот, кожные покровы, ингаляционно);
- с выраженными отдаленными проявлениями действия;
- с выраженным кожно-резорбтивным действием;
- с выраженным сенсибилизирующим действием;
- обладающий выраженной кумуляцией в организме.
Для ДС отрабатывается режим отмыва до безопасных остаточных количеств средства.
Разрабатывается инструкция по применению ДС в практике предприятий пищевой промышленности с характеристикой токсичности и опасности средства, с разработкой необходимых мер предосторожности и рекомендациями по применению средств индивидуальной защиты, а также мер первой помощи при случайном отравлении.
10. Параметры токсикометрии и критерии отбора при оценке токсичности и опасности дезинфицирующих средств, предназначенных для предстерилизационной очистки изделий медицинского назначения (ИМН), включая эндоскопы, аналогичны для дезинфицирующих
средств, предназначенных для дезинфекции ИМН (см. пп.4-6)
11. Третий этап - испытания дезинфицирующих средств
в практических условиях
Дезинфицирующие средства, содержащие в своем составе новое ДВ, после токсикологического изучения и рассмотрения на Подкомиссии по дезинфекционным средствам при Минздраве России допускаются к практическим испытаниям в ЛПУ, очагах инфекционных заболеваний и на предприятиях пищевой промышленности.
В зависимости от назначения ДС проводятся исследования его эффективности, оцениваются потребительские свойства, анкетным методом собирается информация о побочных действиях дезинфектанта в процессе его испытаний в практике.
Проводится санитарно-химический контроль воздуха помещений на содержание ДВ ДС для проверки безопасности рекомендованных мер предосторожности.
Результаты практических испытаний оформляются в виде актов-заключений и приложенных анкет по учету побочного действия ДС (прилож.8) и представляются на рассмотрение Подкомиссии по дезинфекционным средствам при Минздраве России.
При положительных результатах испытаний в практических условиях ДС регистрируются в России и рекомендуются на промышленный выпуск (для отечественных средств) и на применение в практике.
Приложение 2
Классификация опасности веществ по степени воздействия на организм
(ГОСТ 12.1.007-76)
|
|
Класс опасности | |||
|
Показатели |
Чрезвычайно опасные |
Высоко опасные |
Умеренно опасные |
Мало опасные |
|
ПДК в воздухе рабочей зоны, мг/м |
менее 0,1 |
0,1-1,0 |
1,1-10,0 |
более 10,0 |
|
ЛД |
менее 15 |
15-150 |
151-5000 |
более 5000 |
|
ЛД |
менее 100 |
100-500 |
501-2500 |
более 2500 |
|
CЛ |
менее 500 |
500-5000 |
5001-50000 |
более 50000 |
Приложение 3
Классификация токсичности веществ при введении под кожу и в брюшную полость животного (по К.К.Сидорову) [12]
|
Класс токсичности |
Степень токсичности |
Средняя смертельная доза (мг/кг) при введении: | |
|
|
|
под кожу |
в брюшную полость |
|
1 |
Чрезвычайно токсично |
|
|
|
2 |
Высоко токсично |
0,4-15 |
0,3-10,0 |
|
3 |
Умеренно токсично |
16-150 |
11-100 |
|
4 |
Мало токсично |
151-1500 |
101-1000 |
|
5 |
Практически нетоксично |
1501-4500 |
1001-3000 |
|
6 |
Относительно безвредно |
>4500 |
>3000 |
Приложение 4
|
Протокол N __________ |
Дата __________ |
Оценка реакции кожи по интенсивности эритемы и отека в баллах при однократной обработке препаратом
|
Кролик |
Кожа неповрежденная |
Повреждение |
Время после обработки, ч 4-8-24-48-72-96... |
|
1 |
|
эритема |
|
|
n |
|
эритема |
|
|
средн. |
|
эритема |
|
Приложение 4-а
|
Протокол N __________ |
Дата __________ |
Оценка реакции кожи при повторных воздействиях препарата
|
Кролик |
Концентрация препарата, % |
Дни воздействия и наблюдения |
|
|
|
|
|
|
|
1-2-3-4-5-6-7-8-9-10-n |
|
1 |
|
|
|
... |
|
|
|
п |
|
|
Степень кожной реакции
|
Эритема |
Э |
|
Отек |
О |
|
Трещины |
Т |
|
Некроз |
Н |
|
Шелушение |
Ш |
|
Сухость |
С |
Приложение 5
Оценка интенсивности местно-раздражающего действия
химических веществ на кожу
Оценка степени эритемы
|
Интенсивность эритемы (визуально) |
Оценка эритемы по линейке С.В.Суворова, баллы |
|
Отсутствие эритемы |
0 |
|
Слабая (розовый тон) |
1 |
|
Умеренно выраженная (розово-красный тон) |
2 |
|
Выраженная (красный тон) |
3 |
|
Резко выраженная (ярко красный тон) |
4 |
Оценка интенсивности отека кожи
|
Степень интенсивности отека |
Увеличение толщины кожной складки, мм |
Оценка отека, баллы | |
|
|
кролики |
морские свинки |
|
|
Отсутствие |
0 |
0 |
0 |
|
Слабая |
до 0,5 |
до 0,3 |
1 |
|
Умеренная |
0,6-1,0 |
0,4-0,6 |
2 |
|
Выраженная |
1,1-2,0 |
0,7-1,0 |
3 |
|
Резко выраженная |
более 2,0 |
более 1,0 |
4 |
Приложение 6
|
Протокол N __________ |
Дата __________ |
Исследование реакции глаза на препарат
|
Кролик |
Время (дни) |
Роговица |
Конъюнктива |
Сумма по: |
Суммарный балл | ||||
|
|
|
А |
Б |
А |
Б |
В |
Рог. |
Кон. |
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
Не промыв. |
3 |
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
Промыв. |
4 |
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
n |
4 |
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
Приложение 7
Классификация химических веществ по силе аллергенной активности
(МУ 1.1.578-96)
|
|
Классы aллepгeнной активности | |||||
|
Метод сенсибилизации |
по частоте развития сенсибилизации |
по достоверности отличия средне-групповых показателей опытной и контрольной групп | ||||
|
|
1 |
2 |
3 |
1 |
2 |
3 |
|
Морская свинка (в кожу уха): |
|
|
|
|
|
|
|
200 мкг |
>5 из 10 |
>5 из 10 |
|
|
|
>0,05 |
|
50 мкг |
>5 из 10 |
|
0 |
|
>0,05 |
- |
|
Морская свинка комбинированно |
>5 из 10 |
>5 из 10 |
>5 из 10 |
|
|
>0,05 |
|
Морская свинка - эпикутанно |
>5 из 10 |
>5 из 10 |
>5 из10 |
|
|
>0,05 |
|
Мышь - в кожу основания хвоста |
не учитывается |
|
|
>0,05 | ||
Приложение 8
АНКЕТА
учета побочных явлений при проведении практических испытаний
дезинфицирующего средства
|
N |
Ф.И.О. |
Долж- |
Стаж работы |
Вид работы |
Коли- |
Использование средств защиты |
Состояние до начала работы с дезинфек- |
Субъек- | ||
|
|
|
|
|
|
|
защитные очки |
пер- |
респи- |
|
|
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
|
|
|
|
|
|
|
|
|
|
|
|
Примечания.
1. Использование средств защиты обозначается знаком "+", отсутствие знаком "-".
2. Указать, какой вид респиратора использовали.
3. Указать, какие из следующих побочных явлений появились при работе со средством: слезотечение, першение в горле и носу, кашель, насморк, покраснение, зуд кожи, головная боль, тошнота, головокружение.
Подпись и должность лица,
ответственного за проведение испытаний
Печать учреждения
Библиографические данные и нормативные документы
1. Методические указания к постановке исследований для обоснования санитарных стандартов вредных веществ в воздухе рабочей зоны: МУ 2163-80. М., 1980.
2. Временные методические указания по обоснованию предельно допустимых концентраций (ПДК) загрязняющих веществ в атмосферном воздухе населенных мест: МУ 4681-88. М., 1989.
3. Гигиенические критерии для обоснования необходимости разработки ПДК и ОБУВ (ОДУ) вредных веществ в воздухе рабочей зоны, атмосферном воздухе населенных мест, воде водных объектов: ГН 1.1.701-98. М., 1998.
4. Токсикометрия химических веществ, загрязняющих окружающую среду /Под ред. И.В.Саноцкого и А.А.Каспарова /ГКНТ. М., 1986. 417 с.
5. Методические указания к постановке исследований по изучению раздражающих свойств и обоснованию предельно допустимых концентраций избирательно действующих раздражающих веществ в воздухе рабочей зоны. М., 1980.
6. Требования к постановке экспериментальных исследований по обоснованию предельно допустимых концентраций промышленных химических аллергенов в воздухе рабочей зоны и атмосферы: МУ 1.1.578-96. М., 1997.
7. Методические рекомендации по оценке иммунотоксических свойств фармакологических средств. М., 1992.
8. Методические рекомендации по оценке мутагенной активности химических веществ микроядерным методом. М., 1984.
9. Методические рекомендации по оценке новых пестицидов. Киев, 1988. 37 с.
10. Гигиеническая классификация пестицидов по степени опасности: МР 2001/26. М., 2001.
11. ССБТ. Вредные вещества. Классификация и общие требования безопасности: ГОСТ 12.1.007-76.
12. Измеров Н.Ф., Саноцкий И.В., Сидоров К.К. Параметры токсикометрии промышленных ядов при однократном воздействии: Справочник. М.,1977.
13. Оценка токсичности и опасности препаратов дезинсекции: МУ 15-6/7. М., 1990.
14. Методы определения смываемости с посуды: ГОСТ Р 51021-97. М., 1997.
15. Методические указания по использованию культуры диплоидных клеток человека, рекомендуемых для токсиколого-гигиенических исследований. Утверждены МЗ СССР 18.09.91 N 15-6/21. М., 1991. 20 с.
16. Оценка биологического действия медицинских изделий. Ч.5: Исследования на цитотоксичность: методы in vitro / Госстандарт России. М., 1999.
17. Альтернативные методы исследований (экспресс-методы) для токсиколого-гигиенической оценки материалов, изделий и объектов окружающей среды: Методическое пособие. М., 1999. С.79-89.
18. Методические рекомендации по изучению газообразных стерилизующих агентов в целях гигиенической регламентации и контроля их содержания в изделиях медицинского назначения: МР 28-6/14. М., 1988.
19. Государственная Фармакопея СССР. XI изд. М., 1987. Вып.1. С.183-186.
20. Сборник руководящих методических материалов по токсиколого-гигиеническим исследованиям полимерных материалов и изделий на их основе медицинского назначения. Утверждены МЗ СССР. М., 1987. 85 с.
21. Шандала М.Г., Заева Г.Н., Мальцева М.М., Панкратова Г.П. Методология обоснования гигиенических нормативов дезинфицирующих средств. Гигиена и санитария. 2000. N 3. С.58-61.
22. ССБТ. Общие санитарно-гигиенические требования к воздуху рабочей зоны: ГОСТ 12.1.005-88.
Текст документа сверен по:
официальное издание
М.: Федеральный центр госсанэпиднадзора
Минздрава России, 2002