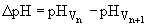
ГОСТ 23268.3-78
Группа Р19
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ВОДЫ МИНЕРАЛЬНЫЕ ПИТЬЕВЫЕ ЛЕЧЕБНЫЕ,
ЛЕЧЕБНО-СТОЛОВЫЕ И ПРИРОДНЫЕ СТОЛОВЫЕ
Методы определения гидрокарбонат-ионов
Drinking medicinal, medicinal-table and natural-table mineral waters.
Methods of determination of hydrocarbonate ions
Дата введения 1980-01-01
ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета СССР по стандартам от 1 сентября 1978 г. N 2408
Ограничение срока действия снято по протоколу N 4-93 Межгосударственного Совета по стандартизации, метрологии и сертификации (ИУС 4-94)
ИЗДАНИЕ с Изменением N 1, утвержденным в апреле 1983 г. (ИУС 8-83)
Настоящий стандарт распространяется на лечебные, лечебно-столовые и природные столовые питьевые минеральные воды и устанавливает методы определения гидрокарбонат-ионов.
(Измененная редакция, Изм. N 1).
1. ОТБОР ПРОБ
1.1. Отбор проб - по ГОСТ 23268.0-91.
1.2. Объем пробы воды для определения гидрокарбонат-ионов должен быть не менее 250 см .
.
2а. ТИТРИМЕТРИЧЕСКИЙ МЕТОД
2а.1. Сущность метода
Метод основан на нейтрализации гидрокарбонат-ионов соляной кислотой в присутствии индикатора метилового оранжевого. Метод позволяет определять от 5 мг гидрокарбонат-ионов в пробе.
2. АППАРАТУРА, МАТЕРИАЛЫ И РЕАКТИВЫ
2.1. Колбы мерные лабораторные по ГОСТ 1770-74, вместимостью 100, 1000 см .
.
Колбы конические стеклянные лабораторные по ГОСТ 25336-82, вместимостью 250 см .
.
Приборы мерные лабораторные стеклянные, вместимостью: пипетки 10, 25, 50 см ; бюретки 25 см
; бюретки 25 см .
.
Капельницы по ГОСТ 25336-82.
Холодильник стеклянный лабораторный по ГОСТ 25336-82.
Вода дистиллированная по ГОСТ 6709-72.
Кислота соляная, фиксанал, 0,1 н. раствор.
Метиловый оранжевый.
Весы технические типа ВЛТ-200.
Все реактивы должны быть квалификации х.ч. или ч.д.а.
3. ПОДГОТОВКА К АНАЛИЗУ
3.1. Приготовление 0,1 н. раствора соляной кислоты
Раствор готовят из фиксанала. Содержимое ампулы для приготовления 0,1 н. раствора соляной кислоты количественно переносят в мерную колбу вместимостью 1000 см и доводят дистиллированной водой до метки.
и доводят дистиллированной водой до метки.
3.2. Приготовление 0,1%-ного раствора метилового оранжевого
0,1 г метилового оранжевого взвешивают с погрешностью не более 0,01 г, растворяют в небольшом объеме дистиллированной воды и доводят объем дистиллированной водой до 100 см .
.
4. ПРОВЕДЕНИЕ АНАЛИЗА
4.1. В коническую колбу вместимостью 250 см отбирают от 25 до 50 см
отбирают от 25 до 50 см анализируемой минеральной воды, объем пробы доводят дистиллированной водой до 100 см
анализируемой минеральной воды, объем пробы доводят дистиллированной водой до 100 см , добавляют 2-3 капли раствора метилового оранжевого и титруют 0,1 н. раствором соляной кислоты до изменения цвета раствора из желтого в розовый. При наличии в исследуемой воде гидрокарбонат-ионов более 300 мг/л после окончания титрования пробу воды кипятят с обратным холодильником в течение 5-7 мин (обратный холодильник можно заменить перевернутой воронкой). В случае изменения цвета раствора в желтый пробу дотитровывают соляной кислотой.
, добавляют 2-3 капли раствора метилового оранжевого и титруют 0,1 н. раствором соляной кислоты до изменения цвета раствора из желтого в розовый. При наличии в исследуемой воде гидрокарбонат-ионов более 300 мг/л после окончания титрования пробу воды кипятят с обратным холодильником в течение 5-7 мин (обратный холодильник можно заменить перевернутой воронкой). В случае изменения цвета раствора в желтый пробу дотитровывают соляной кислотой.
5. ОБРАБОТКА РЕЗУЛЬТАТОВ
Массовую концентрацию гидрокарбонат-ионов (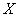 ), мг/дм
), мг/дм , вычисляют по формуле
, вычисляют по формуле
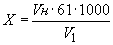 ,
,
где 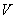 - объем раствора соляной кислоты, израсходованный на титрование, см
- объем раствора соляной кислоты, израсходованный на титрование, см ;
;
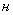 - нормальность раствора соляной кислоты;
- нормальность раствора соляной кислоты;
61 - грамм-эквивалент гидрокарбонат-ионов;
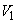 - объем воды, взятый на анализ, см
- объем воды, взятый на анализ, см .
.
За окончательный результат принимают среднее арифметическое значение двух параллельных определений, допускаемые расхождения между которыми не должны превышать 3,0%.
6. ПОТЕНЦИОМЕТРИЧЕСКИЙ МЕТОД
6.1. Сущность метода
Метод основан на установлении конечной точки титрования по наибольшему изменению величины рН, фиксируемому с помощью стеклянного электрода.
Метод применяется при разногласиях, возникающих в оценке качества, и при выполнении химического анализа вод.
6.2. Аппаратура, материалы и реактивы
Прибор для измерения величины рН типа рН-метр-милливольтметр (рН-340, рН-121) или иономер ЭВ-74.
Электрод сравнения хлор-серебряный насыщенный образцовый, 2-го разряда по ГОСТ 17792-72.
Электрод стеклянный типа ЭСЛ.
Мешалка магнитная ММ-3.
Весы технические типа ВЛТ-200.
Приборы мерные лабораторные стеклянные, вместимостью: пипетки 10, 25, 50, 100 см ; бюретки 25 см
; бюретки 25 см .
.
Колбы мерные лабораторные по ГОСТ 1770-74, вместимостью 100, 500, 1000 см .
.
Стаканы лабораторные вместимостью 150 см (диаметр стакана 60-70 мм, высота 70-75 мм).
(диаметр стакана 60-70 мм, высота 70-75 мм).
Бумага фильтровальная по ГОСТ 12026-76.
Кислота соляная, фиксанал, 0,1 н. раствор.
Вода дистиллированная по ГОСТ 6709-72.
6.3. Подготовка к анализу
6.3.1. Приготовление 0,1 н. раствора соляной кислоты - по п.3.1.
6.3.2. Приготовление 0,02 н. раствора соляной кислоты
В мерную колбу вместимостью 500 см отмеривают 100 см
отмеривают 100 см 0,1 н. раствора соляной кислоты, добавляют до метки дистиллированную воду, закрывают колбу пробкой и перемешивают.
0,1 н. раствора соляной кислоты, добавляют до метки дистиллированную воду, закрывают колбу пробкой и перемешивают.
6.4. Проведение анализа
В стакан вместимостью 150 см отмеривают от 1 до 100 см
отмеривают от 1 до 100 см минеральной воды (
минеральной воды (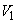 ) с таким расчетом, чтобы в ней содержалось от 5 до 120 мг гидрокарбонат-ионов, доливают дистиллированной водой до 100 см
) с таким расчетом, чтобы в ней содержалось от 5 до 120 мг гидрокарбонат-ионов, доливают дистиллированной водой до 100 см (если отмеренная проба составляла менее 100 см
(если отмеренная проба составляла менее 100 см ). В раствор погружают стеклянный электрод и наконечник электролитического ключа. Титрование ведут 0,1 н. или 0,02 н. (при содержании в пробе менее 10 мг гидрокарбонат-ионов) раствором НСl из обычной бюретки с ценой деления не более 0,1 см
). В раствор погружают стеклянный электрод и наконечник электролитического ключа. Титрование ведут 0,1 н. или 0,02 н. (при содержании в пробе менее 10 мг гидрокарбонат-ионов) раствором НСl из обычной бюретки с ценой деления не более 0,1 см , перемешивая титруемый раствор магнитной мешалкой. Вначале проводят ориентировочное титрование с целью определения примерного положения эквивалентной точки. Для этого раствор титранта прибавляют порциями по 0,5-1,0 см
, перемешивая титруемый раствор магнитной мешалкой. Вначале проводят ориентировочное титрование с целью определения примерного положения эквивалентной точки. Для этого раствор титранта прибавляют порциями по 0,5-1,0 см и после прибавления каждой порции снимают показания прибора (величину рН). Вначале величина рН изменяется незначительно, но вблизи эквивалентной точки наблюдается резкий скачок рН. После скачка рН прибавляют еще 2-3 порции титранта и ориентировочное титрование заканчивают. Замечают объемы титранта (
и после прибавления каждой порции снимают показания прибора (величину рН). Вначале величина рН изменяется незначительно, но вблизи эквивалентной точки наблюдается резкий скачок рН. После скачка рН прибавляют еще 2-3 порции титранта и ориентировочное титрование заканчивают. Замечают объемы титранта (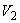 ) и (
) и (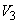 ), при которых наблюдалось максимальное изменение рН (
), при которых наблюдалось максимальное изменение рН (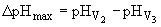 ). Последующее, точное титрование проводят вблизи эквивалентной точки, но, начиная с объема
). Последующее, точное титрование проводят вблизи эквивалентной точки, но, начиная с объема 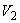 , титрант прибавляют по каплям и снова по максимальному скачку рН определяют объем титранта. Результаты, полученные при точном титровании, оформляют по форме, указанной в приложении.
, титрант прибавляют по каплям и снова по максимальному скачку рН определяют объем титранта. Результаты, полученные при точном титровании, оформляют по форме, указанной в приложении.
6.5. Обработка результатов
Массовую концентрацию гидрокарбонат-ионов вычисляют по формуле, указанной в разд.5.
За окончательный результат принимают среднее арифметическое значение двух параллельных определений, допускаемые расхождения между которыми не должны превышать 1,0-1,5% для вод с содержанием гидрокарбонат-ионов более 100 мг/дм и 2% - для вод, содержащих менее 100 мг/дм
и 2% - для вод, содержащих менее 100 мг/дм гидрокарбонат-ионов.
гидрокарбонат-ионов.
Разд.6 (Введен дополнительно, Изм. N 1).
ПРИЛОЖЕНИЕ
Справочное
Результаты точного титрования потенциометрическим методом
|
Порядковый номер измерения |
Объем титранта |
рН |
|
|
|
|
|
|
ПРИЛОЖЕНИЕ. (Введено дополнительно, Изм. N 1).
Текст документа сверен по:
официальное издание
Государственный контроль качества
минеральной воды и напитков. -
М.: ИПК Издательство стандартов, 2003
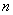
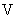 , см
, см