МУК 4.1.1023-01
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Изомерспецифическое определение полихлорированных бифенилов (ПХБ)
в пищевых продуктах
Дата введения 2001-06-15
1. РАЗРАБОТАНЫ Институтом питания РАМН (Эллер К.И., к.х.н., рук. лаборатории; Бессонов В.В., к.х.н., ст.н.с.; Волкович С.В., н.с.; Левин Л.Г., к.м.н., ст.н.с.; Хромченкова Е.П., м.н.с.).
2. РЕКОМЕНДОВАНЫ К УТВЕРЖДЕНИЮ Комиссией по государственному санитарно-эпидемиологическому нормированию при МЗ РФ (протокол N 4 от 19 октября 2000 г.).
3. УТВЕРЖДЕНЫ Главным государственным санитарным врачом Российской Федерации - Первым заместителем министра здравоохранения Российской Федерации 15 марта 2001 г.
4. ВВЕДЕНЫ ВПЕРВЫЕ.
1. Назначение и область применения
Настоящие методические указания устанавливают метод изомерспецифического определения массовых концентраций токсичных полихлорированных бифенилов (ПХБ) в пищевых продуктах с помощью капиллярной газожидкостной хроматографии (КГЖХ) с детектором электронного захвата (ДЭЗ) и предназначены для проведения лабораторных исследований безопасности пищевой продукции и исследования биологического материала (молока, жировой ткани) при оценке нагрузки ПХБ на организм учреждениями госсанэпидслужбы Минздрава РФ, а также для организаций и учреждений, осуществляющих контроль качества и безопасности пищевой продукции в соответствии с СанПиН 2.3.2.560-96* "Гигиенические требования к качеству и безопасности продовольственного сырья и пищевых продуктов" и аккредитованных в установленном порядке.
_________________
* На территории РФ действует СанПиН 2.3.2.1078-01 "Санитарно-эпидемиологические правила и нормативы. Гигиенические требования безопасности и пищевой ценности пищевых продуктов". - Примечание .
2. Общие положения
Полихлорированные бифенилы (ПХБ) - группа стабильных хлорированных ароматических углеводородов, широко использовавшихся в промышленности. Несмотря на повсеместный запрет их использования, смеси наиболее устойчивых ПХБ, отличающихся по степени хлорирования (от 21 до 68% хлора) и составу индивидуальных ПХБ (конгенеров), до настоящего времени обнаруживаются в значимых концентрациях в отходах производств, окружающей среде и биологических объектах. Из 209 возможных конгенеров ПХБ около 50 являются наиболее стабильными и могут накапливаться в различных звеньях пищевой цепи. Химическая структура и принятая нумерация наиболее распространенных и актуальных с гигиенической точки зрения конгенеров ПХБ приведены в табл.1.
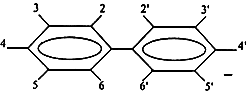
Таблица 1
Химическая структура и принятая нумерация конгенеров ПХБ
|
N индивидуального конгенера ПХБ |
Наименование |
Положение атомов хлора |
|
1 |
2 |
3 |
|
15 |
Дихлорфенил |
4, 4' |
|
18 |
Трихлорбифенил |
2, 2', 5 |
|
22 |
Трихлорбифенил |
2, 3, 4' |
|
28 |
Трихлорбифенил |
2, 4, 4' |
|
31 |
Трихлорбифенил |
2, 4', 5 |
|
33 |
Трихлорбифенил |
2', 3, 4 |
|
40 |
Тетрахлорбифенил |
2, 2', 3, 3' |
|
42 |
Тетрахлорбифенил |
2, 2', 3, 4' |
|
44 |
Тетрахлорбифенил |
2, 2', 3, 5' |
|
49 |
Тетрахлорбифенил |
2, 2', 4, 5' |
|
52 |
Тетрахлорбифенил |
2, 2', 5, 5' |
|
54 |
Тетрахлорбифенил |
2, 2', 6, 6' |
|
66 |
Тетрахлорбифенил |
2, 3', 4, 4' |
|
71 |
Тетрахлорбифенил |
2, 3', 4', 6 |
|
74 |
Тетрахлорбифенил |
2, 4, 4', 5 |
|
76 |
Тетрахлорбифенил |
2', 3, 4, 5 |
|
77 |
Тетрахлорбифенил |
3, 3', 4, 4' |
|
82 |
Пентахлорбифенил |
2, 2', 3, 3', 4 |
|
85 |
Пентахлорбифенил |
2, 2', 3, 4, 4' |
|
86 |
Пентахлорбифенил |
2, 2', 3, 4, 5 |
|
87 |
Пентахлорбифенил |
2, 2', 3, 4, 5' |
|
95 |
Пентахлорбифенил |
2, 2', 3, 5', 6 |
|
97 |
Пентахлорбифенил |
2, 2', 3', 4, 5 |
|
99 |
Пентахлорбифенил |
2, 2', 4, 4', 5 |
|
101 |
Пентахлорбифенил |
2, 2', 4, 5, 5' |
|
105 |
Пентахлорбифенил |
2, 3, 3', 4, 4' |
|
110 |
Пентахлорбифенил |
2, 3, 3', 4', 6 |
|
114 |
Пентахлорбифенил |
2, 3, 4, 4', 5 |
|
118 |
Пентахлорбифенил |
2, 3', 4, 4', 5 |
|
119 |
Пентахлорбифенил |
2, 3', 4, 4', 6 |
|
121 |
Пентахлорбифенил |
2, 3', 4, 5', 6 |
|
128 |
Гексахлорбифенил |
2, 2', 3, 3', 4, 4' |
|
129 |
Гексахлорбифенил |
2, 2', 3, 3', 4, 5 |
|
134 |
Гексахлорбифенил |
2, 2', 3, 3', 5, 6 |
|
136 |
Гексахлорбифенил |
2, 2', 3, 3', 6, 6' |
|
137 |
Гексахлорбифенил |
2, 2', 3, 4, 4', 5 |
|
138 |
Гексахлорбифенил |
2, 2', 3, 4, 4', 5' |
|
141 |
Гексахлорбифенил |
2, 2', 3, 4, 5, 5' |
|
146 |
Гексахлорбифенил |
2, 2', 3, 4', 5, 5' |
|
151 |
Гексахлорбифенил |
2, 2', 3, 5, 5', 6 |
|
153 |
Гексахлорбифенил |
2, 2', 4, 4', 5, 5' |
|
154 |
Гексахлорбифенил |
2, 2', 4, 4', 5, 6' |
|
170 |
Гептахлорбифенил |
2, 2', 3, 3', 4, 4', 5 |
|
171 |
Гептахлорбифенил |
2, 2', 3, 3', 4, 4', 6 |
|
174 |
Гептахлорбифенил |
2, 2', 3, 3', 4, 5, 6' |
|
177 |
Гептахлорбифенил |
2, 2', 3, 3', 4', 5, 6 |
|
180 |
Гептахлорбифенил |
2, 2', 3, 4, 4', 5, 5' |
|
182 |
Гептахлорбифенил |
2, 2', 3, 4, 4', 5, 6' |
|
183 |
Гептахлорбифенил |
2, 2', 3, 4, 4', 5', 6 |
|
185 |
Гептахлорбифенил |
2, 2', 3, 4, 5, 5', 6 |
|
187 |
Гептахлорбифенил |
2, 2', 3, 4', 5, 5', 6 |
|
189 |
Гептахлорбифенил |
2, 3, 3', 4, 4', 5, 5' |
|
191 |
Гептахлорбифенил |
2, 3, 3', 4, 4', 5', 6 |
|
194 |
Октахлорбифенилил |
2, 2', 3, 3', 4, 4', 5, 5' |
|
195 |
Октахлорбифенилил |
2, 2', 3, 3', 4, 4', 5,6 |
|
196 |
Октахлорбифенилил |
2, 2', 3, 3', 4, 4', 5', 6 |
|
199 |
Октахлорбифенилил |
2, 2', 3, 3', 4, 5, 6, 6' |
|
206 |
Нонахлорбифенил |
2, 2', 3, 3', 4, 4', 5, 5', 6 |
|
209 |
Декахлорбифенил |
2, 2', 3, 3', 4, 4', 5, 5', 6, 6' |
В жировой ткани человека и женском молоке накапливаются в основном следующие конгенеры ПХБ: 138, 153, 156, 118, 180, 105, 99, 174, 170, 187, 101, 74, 66, 95, 146, 137, 183. В образцах рыбопродуктов чаще всего встречаются ПХБ: 138, 153, 99, 118, 110, 101, 87, 84, 52, 49, 44 и др.
Многочисленные опыты на животных показали, что долговременное воздействие малых доз ПХБ может индуцировать опухоли, оказывает неблагоприятное влияние на репродуктивную функцию. ПХБ проявляют эмбриотоксические и нейротоксические свойства. Согласно оценке Международного агентства исследований рака (МАИР) ПХБ следует рассматривать как потенциально канцерогенные вещества для человека.
ПХБ характеризуются высокой стабильностью в окружающей среде и способностью аккумулироваться в различных звеньях пищевой цепи. Основным источником поступления ПХБ в организм человека являются пищевые продукты. Показано, что ПХБ могут накапливаться в жировой ткани человека и экскретироваться с женским молоком.
Среднее поступление ПХБ с пищей в развитых индустриальных странах оценивается в 0,005-0,2 мкг/кг/сутки, поступление ПХБ в организм грудных детей с женским молоком - 2-12 мкг/кг/сутки.
В Российской Федерации установлен максимально допустимый уровень содержания суммы ПХБ в рыбе и рыбопродуктах на уровне 2,0 мг/кг и в биологически активных добавках к пище на основе рыбьего жира - на уровне 3,0 мг/кг (СанПиН 2.3.2.560-96 "Гигиенические требования к качеству и безопасности продовольственного сырья и пищевых продуктов" раздел 6.3).
3. Основные характеристики метода
Предел обнаружения метода составляет 0,001 мг/кг (по ПХБ-105) и 0,01-0,015 (для суммы изомеров ПХБ).
Диапазон определяемых массовых концентраций по ПХБ-105 составляет от 0,001 до 100 мг/кг.
При соблюдении всех регламентируемых методикой условий проведения измерений относительная характеристика погрешности (стандартное отклонение сходимости) результата анализа при концентрации суммы ПХБ в 1,0 мг/кг не превышает 0,023 (2,26%). Среднее значение открываемости ПХБ при концентрациях от 0,2 до 20,0 мг/кг составляет от 85 до 88%.
4. Принцип метода
Метод включает следующие этапы:
- гидролиз пищевых продуктов или стабилизированного оксалатом калия молока 5%-ным раствором гидроксида натрия в 96%-ном водном этиловом спирте и экстракцию неомыляемой фракции гексаном;
- очистку фракции ПХБ с помощью колоночной хроматографии (КХ) на флоризиле (активированном силикате магния) или смеси флоризил-оксид алюминия;
- обнаружение, идентификацию и количественное определение индивидуальных ПХБ с помощью КГЖХ с ДЭЗ с использованием метода внутреннего стандарта.
5. Аппаратура и оборудование
|
1. Весы лабораторные общего назначения, с наибольшим пределом взвешивания до 500 г, с пределом допустимой погрешности ±0,038 г |
ГОСТ 24104-80 |
|
2. Весы лабораторные с наибольшим пределом взвешивания до 200 г, с пределом допустимой погрешности +0,0005 г |
ГОСТ 24104-80 |
|
3. Мельница электрическая |
ТУ 46-22-236-76 |
|
4. Аппарат для встряхивания проб АВУ-6С |
ТУ 64-1-2451-78 |
|
5. Центрифуга ОПн-8УХЛ 4.2 |
ТУ 5.375-4261-76 |
|
6. Ротационный испаритель типа ИР-1М |
ТУ 25-11-917-76 |
|
7. Насос вакуумный с электродвигателем или вакуум насос типа ВН-461М |
ГОСТ 14707-82 |
|
ТУ 3-863-73 | |
|
8. Баня силиконовая или глицериновая |
|
|
9. Газовый хроматограф с детектором электронного захвата и инжектором с делением потока "split-splitless injector" для капиллярной колонки |
|
|
10. Капиллярная колонка с жидкой фазой SE-54, или DB-5, или Rtx-5, или НР-5, длина - 30-50 м, внутренний диаметр - 0,2-0,32 мм, толщина пленки жидкой фазы - 2-5 мкм |
|
|
11. Баллон с азотом ос.ч. |
|
|
12. Микрошприцы МШ-10 или аналогичные |
|
|
13. Колбы конические плоскодонные КНКШ-500-29/32, КНКШ-100-29/32, КНКШ-50-29/32 с НШ 29 |
ГОСТ 10394-72 |
|
14. Колбы круглодонные ККШ-1000-29/32, ККШ-500-29/32, ККШ-100-29/32 с НШ-29 |
ГОСТ 10394-72 |
|
15. Воронки делительные ВД-1-1000, ВД-1-500, ВД-1-250 |
|
|
16. Колбы грушевидные ГР 25-14/23, ГР 50-14/23, ГР 100-14/23 |
|
|
17. Цилиндры мерные типа 2-500, 2-100, 2-50, 2-25, 2-10 |
|
|
18. Пипетки мерные типа 4-1-1 на 10, 5, 2, 1 мм |
ГОСТ 20292-74 |
|
19. Колбы мерные 2-200-2, 2-100-2, 2-50-2, 2-25-2 |
|
|
20. Воронка Бюхнера |
|
|
21. Колба Бунзена на 500 см |
|
|
22. Холодильники стеклянные лабораторные типа ХПТ-2-400-29/32, ХШ-1-300-29/32 |
|
|
23. Колонки стеклянные для адсорбционной хроматографии длиной 250 мм с внутренним диаметром 8 мм |
|
|
24. Воронки стеклянные В-56-80, В-36-50, В-36-80 |
6. Реактивы и стандартные растворы
|
1. Фильтры обеззоленные марки ФОМ |
|
|
2. Вода дистиллированная |
|
|
3. Гексан х.ч. |
ТУ 6-094521-77 |
|
или ч. |
ТУ 6-093375-78 |
|
4. Ацетонитрил для жидкостной хроматографии ОП-3 ос.ч. |
ТУ 6-09-14216-78 |
|
или ч. |
ТУ 6-09-3534-82 |
|
5. Спирт этиловый х.ч. |
|
|
или спирт изопропиловый х.ч. |
ТУ 6-09-402-81 |
|
6. Эфир медицинский |
|
|
7. Флоризил 100/200 mesh (силикат магния) для колоночной хроматографии "Supеlco" |
|
|
8. Индивидуальные стандарты ПХБ и стандартные смеси ПХБ |
|
|
9. Конгенеры ПХБ-48, ПХБ-119; ПХБ-128; ПХБ-155; (фирма "Chеmservicе" США), |
|
|
смесь ПХБ арохлор 1254* |
|
|
(см. приложения) |
|
|
10. Натрий серно-кислый (сульфат натрия) безводный, ч.д.а., промытый перегнанным хлороформом и прокаленный при t=150 °С |
7. Подготовка реактивов для проведения анализов
7.1. Очистка растворителей
Дистиллированная вода и органические растворители перегоняются перед анализом с использованием только стеклянной лабораторной посуды в условиях, исключающих контакт с пластиками.
7.2. Очистка и регенерация флоризила
Флоризил промывают под вакуумом на воронке Бюхнера смесью перегнанных гексана с ацетоном (1:1) или гексана с хлороформом (1:1), подсушивают на воздухе в вытяжном шкафу и в сушильном шкафу при t=110 °С, выдерживают в муфельной печи при t=600 °С в течение 4 час. Использованный в ходе анализа флоризил отмывают дистиллированной водой от остатков сульфата натрия, фильтруют, подсушивают, для удаления остатков воды промывают ацетоном, смесью гексана с хлороформом (1:1), фильтруют над вакуумом, подсушивают на воздухе, затем в сушильном шкафу при 110 °С и активируют в муфельной печи при t=600 °С в течение 4 час.
8. Гидролиз образца и экстракция ПХБ
Усредненную и измельченную пробу (1 г) помещают в коническую колбу на 100 мл, заливают 50 мл 5%-ного раствора гидроксида калия в 96%-ном водном этаноле и кипятят с обратным холодильником 30 минут. После охлаждения выливают содержимое колбы в делительную воронку, в которую предварительно было налито 300 мл дистиллированной воды. Экстрагируют гексаном (2х60 мл). Объединенный гексановый экстракт промывают дистиллированной водой (3х40 мл), сушат сульфатом натрия, фильтруют через бумажный фильтр и упаривают на ротационном испарителе до объема около 1 мл.
9. Очистка экстракта с помощью КХ на флоризиле
Упаренный экстракт наносят на хроматографическую колонку с флоризилом (слой флоризила в колонке высотой 4-5 см, предварительно промыт 5 мл гексана), грушевидную колбу из-под экстракта ополаскивают 5 мл смеси гексан-эфир (95:5), которые также наносят на колонку. Колонку элюируют 45 мл смеси гексан-эфир (95:5), элюат собирают в грушевидную колбу на 100 мл и упаривают на ротационном испарителе до объема примерно 1 мл (раствор А). Остаток растворителя отдувают в слабом токе азота. Остаток растворяют в 1 мл гексанового раствора внутреннего стандарта ПХБ-119 с концентрацией 50 нг/мл (раствор В)*.
_____________
* В случае недостаточной очистки с помощью КХ на флоризиле раствор А дополнительно очищают путем жидкость-жидкостного распределения в системе гексан-ацетонитрил: раствор А упаривают в токе азота досуха, добавляют 15 мл гексана, насыщенного ацетонитрилом, и 15 мл ацетонитрила. Смесь переносят в делительную воронку и встряхивают. После разделения слоев верхний гексановый слой отбрасывают, к нижнему ацетонитрильному слою добавляют 100 мл дистиллированной воды. Фракцию ПХБ экстрагируют из водно-ацетонитрильного раствора гексаном (2х20 мл). Гексановый раствор сушат серно-кислым натрием, фильтруют через бумажный фильтр в грушевидную колбу на 100 мм и упаривают на ротационном испарителе до объема примерно 1 мл. Остаток растворителя отдувают в слабом токе азота. Остаток растворяют в 1 мл гексанового раствора внутреннего стандарта ПХБ-119 с концентрацией 50 нг/мл.
10. ГЖХ фракции ПХБ и расчет концентрации индивидуальных ПХБ в образцах
Раствор В анализируют с помощью ГЖХ с детектором электронного захвата.
Условия ГЖХ: кварцевая капиллярная колонка 30 или 50 м, внутренний диаметр 0,32 мм, жидкая фаза - полиметилфенилсилоксан (5% фенила, 1% дивинила) SЕ-54, DB-5, или Rtx-5, или НР-5:
|
температура колонки |
220 °С; |
|
температура испарителя |
240 °С; |
|
температура детектора |
300 °С; |
|
время выхода растворителя |
2,5-3 мин (для колонки 50 м). |
Перед исследованием образцов необходимо провести контроль растворителя (гексана) на наличие пиков посторонних веществ, накладывающихся при ГЖХ на пики анализируемых ПХБ.
Предварительно калибруют колонку, определяют приведенные относительные времена удерживания стандартов ПХБ (ПХБ-48, ПХБ-128, ПХБ-155, рис.1) и основных пиков стандарта арохлора 1254 (рис.2) относительно внутреннего стандарта ПХБ-119 на их соответствие табличным данным (см. табл.2). Идентификация пиков при ГЖХ образца проводят по приведенным относительным временам удерживания (RRT) по таблице. Значения RRТ для индивидуальных конгенеров ПХБ должны воспроизводиться с точностью до 0,001-0,003 (1-3 единиц в третьем знаке после запятой).
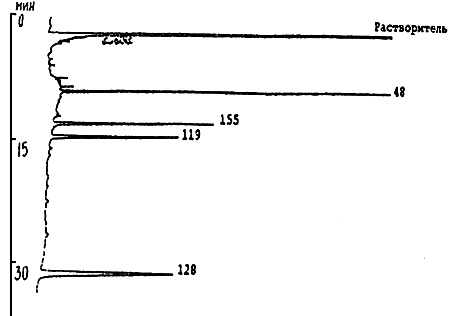
Рис.1. Смесь 1 индивидуальных ПХБ 48, 155, 119, 128

Рис.2. Смесь 2 арохлор 1254 и ПХБ 119
Определение относительного приведенного времени удерживания (RRT) по внутреннему стандарту проводится по формуле:
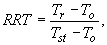
где 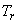 - время выхода пика конгенера;
- время выхода пика конгенера;
 - время выхода пика неудерживаемого компонента (растворителя);
- время выхода пика неудерживаемого компонента (растворителя);
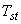 - время выхода внутреннего стандарта (OCN или инд. ПХБ-119).
- время выхода внутреннего стандарта (OCN или инд. ПХБ-119).
Относительные приведенные времена удерживания (RRT) и калибровочные коэффициенты  наиболее распространенных индивидуальных ПХБ по ПХБ-119 и октахлорнафталину (ОСN) при ГЖХ на жидкой фазе SE-54, температура 220 °С приведены в табл.2.
наиболее распространенных индивидуальных ПХБ по ПХБ-119 и октахлорнафталину (ОСN) при ГЖХ на жидкой фазе SE-54, температура 220 °С приведены в табл.2.
Таблица 2
Относительные приведенные времена удерживания (RRT) и калибровочные коэффициенты наиболее распространенных индивидуальных ПХБ по ПХБ 119 и по октахлорнафталину при ГЖХ на жидкой фазе SE-54, температура 220 °С
|
N инд. ПХБ |
RRT по ПХБ 119 |
|
RRT пo октахлорнафталину |
|
1 |
2 |
3 |
4 |
|
18 |
0,322 |
4,07 |
0,047 |
|
15 |
0,328 |
13,45 |
0,047 |
|
54 |
0,402 |
3,46 |
0,058 |
|
31 |
0,426 |
2,15 |
0,062 |
|
28 |
0,434 |
1,73 |
0,063 |
|
33 |
0,464 |
2,77 |
0,067 |
|
22 |
0,486 |
0,98 |
0,071 |
|
52 |
0,532 |
2,98 |
0,077 |
|
49 |
0,549 |
1,83 |
0,079 |
|
48 |
0,559 |
1,42 |
0,082 |
|
44 |
0,611 |
2,33 |
0,088 |
|
42 |
0,628 |
1,45 |
0,091 |
|
71, 41, 64 |
0,665 |
- |
0,097 |
|
40 |
0,699 |
1,62 |
0,101 |
|
74 |
0,765 |
1,76 |
0,111 |
|
76, 70 |
0,781 |
1,94 |
0,114 |
|
66 |
0,802 |
1,84 |
0,117 |
|
95 |
0,809 |
0,80 |
0,117 |
|
121 |
0,809 |
1,51 |
0,117 |
|
155 |
0,873 |
0,93 |
0,127 |
|
101 |
0,930 |
1,77 |
0,135 |
|
99 |
0,959 |
1,95 |
0,139 |
|
119 |
1,000 |
1,00 |
0,146 |
|
97 |
1,070 |
1,89 |
0,155 |
|
86 |
1,075 |
1,44 |
0,156 |
|
87 |
1,101 |
1,07 |
0,159 |
|
85 |
1,137 |
1,57 |
0,165 |
|
136 |
1,161 |
2,79 |
0,168 |
|
77 |
1,173 |
3,30 |
0,170 |
|
154 |
1,175 |
2,12 |
|
|
110 |
1,176 |
1,83 |
0,170 |
|
82 |
1,266 |
1,49 |
0,183 |
|
151 |
1,272 |
1,47 |
0,184 |
|
118 |
1,383 |
1,30 |
0,20 |
|
134 |
1,473 |
1,33 |
0,214 |
|
114 |
1,495 |
1,06 |
0,216 |
|
146 |
1,542 |
1,60 |
0,214 |
|
153 |
1,596 |
1,71 |
0,231 |
|
105 |
1,646 |
1,18 |
0,238 |
|
141 |
1,742 |
0,74 |
0,253 |
|
137 |
1,824 |
0,96 |
0,263 |
|
138 |
1,920 |
1,16 |
0,278 |
|
129 |
2,025 |
1,10 |
0,292 |
|
187 |
2,139 |
0,95 |
0,309 |
|
182 |
2,139 |
0,433 |
0,309 |
|
183 |
2,217 |
1,129 |
0,320 |
|
128 |
2,294 |
0,880 |
0,333 |
|
185 |
2,374 |
0,682 |
0,342 |
|
174 |
2,493 |
1,422 |
0,361 |
|
177 |
2,582 |
1,084 |
0,374 |
|
171 |
2,663 |
0,898 |
0,385 |
|
180 |
2,995 |
0,786 |
0,433 |
|
191 |
3,135 |
0,659 |
0,452 |
|
170 |
3,623 |
1,547 |
0,524 |
|
196 |
3,992 |
0,841 |
0,576 |
|
189 |
4,409 |
0,637 |
0,638 |
|
195 |
4,826 |
3,01 |
0,698 |
|
194 |
5,567 |
0,465 |
0,806 |
Расчет концентрации индивидуальных ПХБ в образцах
Количественное определение ПХБ проводят по отношению площадей пиков ПХБ и внутреннего стандарта с использованием калибровочных коэффициентов, определенных при ГЖХ стандартных смесей ПХБ известного количественного состава (табл.2).
Расчет при использовании метода добавленного внутреннего стандарта проводят по формуле:

где 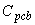 - концентрация конгенера ПXБ в образце, мг/кг (ррm);
- концентрация конгенера ПXБ в образце, мг/кг (ррm);
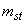 - масса внутреннего стандарта, внесенного в очищенный экстракт образца, мкг;
- масса внутреннего стандарта, внесенного в очищенный экстракт образца, мкг;
 - площадь пика ПХБ на хроматограмме;
- площадь пика ПХБ на хроматограмме;
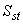 - площадь пика внутреннего стандарта на хроматограмме;
- площадь пика внутреннего стандарта на хроматограмме;
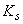 - калибровочный коэффициент ПХБ по внутреннему стандарту (по данным табл.2);
- калибровочный коэффициент ПХБ по внутреннему стандарту (по данным табл.2);
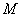 - навеска образца, г.
- навеска образца, г.
За содержание ПХБ в образце принимается суммарное содержание основных 10-15 конгенеров ПХБ.
11. Расчет погрешности измерений
Расчет погрешности измерений проводят в соответствии с требованиями ГОСТа 8.563-96 и ГОСТа 8.207-76. Вычисляют неисключенную систематическую и случайную погрешности по всем этапам измерений и далее в соответствии с ГОСТом 8.207-76 определяют суммарную погрешность измерений. Статистика оценивалась по смеси индивидуальных ПХБ 48, 155 и 128.
Статистические параметры определения суммы полихлорированных бифенилов в рыбе и рыбопродуктах:
|
Статистический параметр |
Внесено суммы ПХБ, мг/кг | ||||
|
0,2 |
1,0 |
2,0 |
10,0 |
20,0 | |
|
Среднее обозначение определения m, мг/кг |
0,171 |
0,859 |
1,73 |
8,74 |
17,6 |
|
Среднее значение открываемости, % от внесенного |
85,3 |
85,9 |
86,5 |
87,4 |
88,0 |
|
Стандартное отклонение сходимости Sr, мг/кг |
0,012 |
0,051 |
0,097 |
0,235 |
0,349 |
|
Относительное стандартное отклонение сходимости, % oт m |
2,37 |
2,26 |
2,12 |
2,35 |
2,34 |
|
Показатель сходимости r, мг/кг (r=2,77 Sr) |
0,033 |
0,125 |
0,265 |
0,651 |
0,967 |
|
Стандартное отклонение воспроизводимости, % от m |
0,019 |
0,094 |
0,119 |
0,475 |
0,054 |
|
Относительное стандартное отклонение воспроизводимости, % от m |
3,84 |
4,37 |
4,22 |
4,51 |
4,39 |
|
Показатель воспроизводимости R, мг/кг (R=2,77 Sr) |
0,053 |
0,26 |
0,33 |
1,31 |
1,81 |
12. Требования к квалификации исполнителей и техники безопасности
Работу по указанной методике может выполнять группа аналитиков, включающая квалифицированных специалистов в области газожидкостной хроматографии и санитарной химии. Исполнители должны быть проинструктированы об основных мерах техники безопасности при работе с веществами 1-2 класса опасности, органическими растворителями (ацетонитрил, гексан и т.д.), а также с основными правилами техники безопасности при работе в химической лаборатории.
Приложения
Для оценки пригодности системы ГЖХ и калибровки колонки предварительно проводят 2 тестовых ГЖХ-анализа стандартных смесей ПХБ:
1. Смесь 1 индивидуальных ПХБ 48, 155, 128 с концентрацией каждого от 50 до 125 нг/мл и внутреннего стандарта 119 с концентрацией 50 нг/мл.*
______________
* При недостаточной чувствительности ГЖХ системы можно применять растворы смесей 1 и 2, а также раствор стандарта 119 с десятикратно более высокими концентрациями: смесь 1 - от 500 до 1250 нг/мл, ПХБ-119 - 500 нг/мл и смесь 2 - 5000 нг/мл по арохлору 1254 и 500 нг/мл по ПХБ-119.
2. Смесь 2, содержащая арохлор 1254 с общей концентрацией около 500 нг/мл и внутреннего стандарта 119 с концентрацией 50 нг/мл.*
______________
* При недостаточной чувствительности ГЖХ системы можно применять растворы смесей 1 и 2, а также раствор стандарта 119 с десятикратно более высокими концентрациями: смесь 1 - от 500 до 1250 нг/мл, ПХБ-119 - 500 нг/мл и смесь 2 - 5000 нг/мл по арохлору 1254 и 500 нг/мл по ПХБ-119.
Тест 1. Вносят в газовый хроматограф 1-2 мкл смеси 1. При этом получают хроматограмму, аналогичную приведенной на рис.1. Рассчитанные относительные приведенные времена удерживания ПХБ 48, 155, 128 по внутреннему стандарту 119 должны соответствовать данным табл.2.
Тест 2. Вносят в газовый хроматограф 1-2 мкл смеси 2. При этом получают хроматограмму, аналогичную приведенной на рис.2. Сравнивают рассчитанные по хроматограмме относительные приведенные времена удерживания ПХБ основных компонентов с данными табл.3.
Таблица 3
Относительные приведенные времена удерживания (RRT) основных конгенеров арохлора 1254 по ПХБ 119 при ГЖХ на жидкой фазе SE-54, температура 220 °С
|
N инд. ПХБ |
RRT по ПХБ 119 |
RRT по октахлорнафталину |
|
52 |
0,532 |
0,077 |
|
44 |
0,611 |
0,088 |
|
41, 64 |
0,665 |
0,097 |
|
70 |
0,781 |
0,114 |
|
66 |
0,802 |
0,117 |
|
95 |
0,809 |
0,117 |
|
91 |
0,837 |
0,122 |
|
84 |
0,891 |
0,13 |
|
101 |
0,928 |
0,135 |
|
99 |
0,959 |
0,14 |
|
119 |
1,000 |
0,146 |
|
97 |
1,069 |
0,155 |
|
87 |
1,102 |
0,160 |
|
85 |
1,136 |
0,165 |
|
110 |
1,176 |
0,170 |
|
82, 151 |
1,268 |
0,185 |
|
123, 118 |
1,388 |
0,202 |
|
146 |
1,542 |
0,214 |
|
153, 132 |
1,602 |
0,233 |
|
105 |
1,646 |
0,238 |
|
141 |
1,742 |
0,253 |
|
138 |
1,922 |
0,279 |
|
128 |
2,298 |
0,334 |
|
171 |
2,663 |
0,385 |
Текст документа сверен по:
официальное издание
М.: Федеральный центр госсанэпиднадзора
Минздрава России, 2001