- USD ЦБ 03.12 30.8099 -0.0387
- EUR ЦБ 03.12 41.4824 -0.0244
|
Краснодар:
|
погода |
Курсы
Индексы
- DJIA 03.12 12019.4 -0.01
- NASD 03.12 2626.93 0.03
- RTS 03.12 1545.57 -0.07
МУК 4.1.699-98
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
ОПРЕДЕЛЕНИЕ ЙОДА В СОЛИ ПОВАРЕННОЙ ПИЩЕВОЙ,
ЙОДИРОВАННОЙ ЙОДАТОМ КАЛИЯ ( )
)
Дата введения: с момента утверждения
1. РАЗРАБОТАНЫ: Институтом питания РАМН (Тутельян В.А., Спиричев В.Б., Переверзева О.Г.) на основе официально принятого международными организациями ВОЗ, ЮНИСЕФ, РАММ, МИ, ICCIDD руководства "Мониторинг программ всеобщего йодирования соли" (М., 1997)
2. УТВЕРЖДЕНЫ И ВВЕДЕНЫ В ДЕЙСТВИЕ Главным государственным санитарным врачом Российской Федерации Г.Г.Онищенко 14 апреля 1998 г.
3. ВВЕДЕНЫ ВПЕРВЫЕ.
1. ОБЛАСТЬ ПРИМЕНЕНИЯ
Необходимость контроля за содержанием йода в йодированной поваренной соли обусловлена существованием интервала допустимого и достаточного потребления этого элемента человеком, составляющего 150-200 мкг/сут.
Методические указания предназначены для предприятий соляной промышленности, учреждений Госсанэпиднадзора и других ведомств, осуществляющих контроль качества и безопасности продовольственного сырья и пищевых продуктов.
2. СУЩНОСТЬ МЕТОДА
Метод основан на взаимодействии йодата калия с йодидом калия в кислой среде (1) титровании выделившегося йода тиосульфатом натрия (2).
3. СРЕДСТВА ИЗМЕРЕНИЙ, ВСПОМОГАТЕЛЬНЫЕ УСТРОЙСТВА, РЕАКТИВЫ
1. Весы лабораторные по ГОСТ 24104-88, 2-го класса с наибольшим пределом взвешивания 200 г и допустимой погрешностью взвешивания не более 0,002 г.
2. Пипетки стеклянные по ГОСТ 29227-91, вместимостью 10 см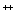 , 5 см
, 5 см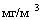 , 1см
, 1см .
.
3. Колбы конические по ГОСТ 25226-82, вместимостью 250 см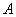 .
.
4. Бюретки по ГОСТ 29251-91, вместимостью 25 см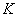 , 5 см
, 5 см .
.
5. Фильтры бумажные диаметром 9 мм.
6. Вода дистилированная по ГОСТ 6709-72.
7. Калий йодистый ( ) по ГОСТ 4232-74.
) по ГОСТ 4232-74.
8. Кислота серная (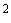 ) по ГОСТ 4204-77.
) по ГОСТ 4204-77.
9. Натрий серноватистокислый пятиводный (тиосульфат натрия, 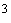 ·
·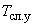 ) по ГОСТ 27068-86 или фиксанал 0,1 г - экв.
) по ГОСТ 27068-86 или фиксанал 0,1 г - экв.
10. Крахмал растворимый по ГОСТ 10163-76.
11. Натрия хлорид, ЧДА, ГОСТ 4233-77.
4. ПРИГОТОВЛЕНИЕ РЕАКТИВОВ
1. 0,005 М тиосульфат натрия (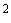 ·
·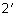 ). 1,24г
). 1,24г 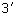 ·
· развести в 1000 мл дистиллированной свежепрокипяченной воды. Т.к. кристаллический тиосульфат при хранении набирает влагу, что требует введения поправки на его титр, то в случае возникновения сомнений рекомендуется использовать фиксанал
развести в 1000 мл дистиллированной свежепрокипяченной воды. Т.к. кристаллический тиосульфат при хранении набирает влагу, что требует введения поправки на его титр, то в случае возникновения сомнений рекомендуется использовать фиксанал  ·
·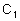 0.1 г - эквивалент, который растворяют в дистиллированной воде, доводя конечный объем до 1000 мл, и полученный раствор разводят в 20 раз (50 мл раствора + 950 мл воды) до конечной концентрации 0,005 М.
0.1 г - эквивалент, который растворяют в дистиллированной воде, доводя конечный объем до 1000 мл, и полученный раствор разводят в 20 раз (50 мл раствора + 950 мл воды) до конечной концентрации 0,005 М.
Полученный раствор хранят в прохладном темном месте. Его объем достаточен для анализа 100-200 проб в зависимости от содержания в них йода. При соблюдении условий хранения раствор стабилен не менее одного месяца.
2. 2 н. серная кислота (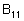 ). 6 мл концентрированной
). 6 мл концентрированной 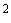 медленно доливают в 90 мл воды, затем доводят раствор водой до конечного объема 100 мл. Полученное количество достаточно для анализа 100 проб. Раствор сохраняет свои свойства неопределенно долгое время.
медленно доливают в 90 мл воды, затем доводят раствор водой до конечного объема 100 мл. Полученное количество достаточно для анализа 100 проб. Раствор сохраняет свои свойства неопределенно долгое время.
Примечание. Во всех случаях кислоту надо наливать в воду, а не наоборот, во избежание чрезмерного повышения температуры смеси и разбрызгивания кислоты. Во время добавления кислоты раствор следует непрерывно перемешивать.
3. 10% йодид калия (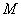 ) свежеприготовленный. 10 г
) свежеприготовленный. 10 г 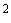 растворяют в 100 мл воды. Хранят в прохладном темном месте. Его количества достаточно для анализа 20 проб.
растворяют в 100 мл воды. Хранят в прохладном темном месте. Его количества достаточно для анализа 20 проб.
4. Насыщенный раствор хлорида натрия (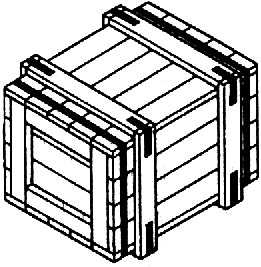 ). В колбу объемом 250 мл с 80 мл воды постепенно добавляют при перемешивании и/или нагревании
). В колбу объемом 250 мл с 80 мл воды постепенно добавляют при перемешивании и/или нагревании 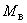 до тех пор, пока не прекратится его растворение. Хранят под пробкой. Раствор сохраняет свои свойства по крайней мере в течение года.
до тех пор, пока не прекратится его растворение. Хранят под пробкой. Раствор сохраняет свои свойства по крайней мере в течение года.
5. Индикаторный раствор крахмала. В колбу объемом 250 мл вносят 1 г растворимого крахмала, добавляют 10 мл воды и нагревают до растворения крахмала. В полученную горячую смесь добавляют 90 мл насыщенного раствора 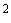 и перемешивают. Полученного объема достаточно для анализа 50 проб. Готовый раствор хранят в прохладном темном месте. Раствор остается стабильным на протяжении месяца.
и перемешивают. Полученного объема достаточно для анализа 50 проб. Готовый раствор хранят в прохладном темном месте. Раствор остается стабильным на протяжении месяца.
Примечание. В день проведения анализа раствор необходимо прогреть (но не кипятить) для ресуспендирования возможного осадка.
5. ПРОВЕДЕНИЕ АНАЛИЗА
Этап 1. Навеску исследуемой пробы массой 10 г растворяют в 100 см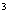 дистиллированной воды в конической колбе объемом 250 см
дистиллированной воды в конической колбе объемом 250 см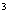 . Если полученный раствор мутный, его необходимо профильтровать.
. Если полученный раствор мутный, его необходимо профильтровать.
Этап 2. К полученному раствору добавляют 1 см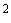 2 н.
2 н. 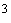 , перемешивают, добавляют 5 мл 10% раствора
, перемешивают, добавляют 5 мл 10% раствора 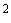 , перемешивают, закрывают колбу пробкой и помещают на 10 мин в темное место.
, перемешивают, закрывают колбу пробкой и помещают на 10 мин в темное место.
Этап 3. К исследуемому раствору, приобретшему темно-желтую окраску, добавляют из бюретки при перемешивании 0,005 М 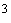 до перехода окраски в светло-желтую. Добавляют в исследуемый раствор примерно 2 мл индикаторного раствора крахмала, от чего смесь должна приобрести темно-синюю окраску, и продолжают титрование до тех пор, пока последняя не исчезнет.
до перехода окраски в светло-желтую. Добавляют в исследуемый раствор примерно 2 мл индикаторного раствора крахмала, от чего смесь должна приобрести темно-синюю окраску, и продолжают титрование до тех пор, пока последняя не исчезнет.
Отмечают объем раствора тиосульфата, пошедший на титрование.
6. ТРЕБОВАНИЯ К БЕЗОПАСНОСТИ
- до начала титрования реакционную смесь следует хранить в темном месте ввиду возможности побочного процесса под воздействием света, который вызывает окисление ионов йодида до йода;
- при использовании не вполне остывшего раствора крахмала точность определений понижается;
- если индикаторный раствор добавлен слишком рано, происходит образование прочного, очень медленно реагирующего комплекса йода с крахмалом, что приводит к завышению результатов анализа;
- реакция должна проходить при умеренной комнатной температуре (ниже 30 °С), поскольку йод характеризуется повышенной летучестью, а индикаторный раствор при нагревании теряет чувствительность.
7. ОБРАБОТКА РЕЗУЛЬТАТОВ
Количество йода в мг на 1кг исследуемой соли вычисляют по формуле:
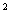 (мг/кг),
(мг/кг),
где 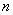 - объем 0,005 М
- объем 0,005 М 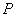 , пошедший на титрование, см
, пошедший на титрование, см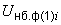 ;
;
10 - навеска соли, взятой на анализ, г;
1000 - пересчет на 1 кг соли;
0,1057- количество йода из иодата калия исследуемого образца соли, соответствующее 1 см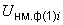 пошедшего на титрование этого образца 0,005 М
пошедшего на титрование этого образца 0,005 М 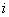 .
.
Примечание. Из уравнений реакций (1) и (2), лежащих в основе данного метода определения йода в соли, обогащенной 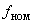 , следует, что из общего количества йода, оттитровываемого тиосульфатом натрия в исследуемой пробе, на долю йода, происходящего из
, следует, что из общего количества йода, оттитровываемого тиосульфатом натрия в исследуемой пробе, на долю йода, происходящего из 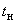 , приходится 1/6 часть, т.е. не 0,6345, а 0,1057 мг.
, приходится 1/6 часть, т.е. не 0,6345, а 0,1057 мг.
Для облегчения расчета количества йода в исследуемой соли можно также пользоваться переводной таблицей (см. Приложение).
Приложение
Таблица для перевода показаний шкалы бюретки в мг/кг соли
Показания шкалы |
мг/кг |
0,0 |
0,0 |
0,1 |
1,1 |
0,2 |
2,1 |
0,3 |
3,2 |
0,4 |
4,2 |
0,5 |
5,3 |
0,6 |
6,3 |
0,7 |
7,4 |
0,8 |
8,5 |
0,9 |
9,5 |
1,0 |
10,6 |
1,1 |
11,6 |
1,2 |
12,7 |
1,3 |
13,8 |
1,4 |
14,8 |
1,5 |
15,9 |
1,6 |
16,9 |
1,7 |
18,0 |
1,8 |
19,0 |
1,9 |
20,1 |
2,0 |
21,2 |
2,1 |
22,2 |
2,2 |
23,3 |
2,3 |
24,3 |
2,4 |
25,4 |
2,5 |
26,5 |
2,6 |
27,5 |
2,7 |
28,6 |
2,8 |
29,6 |
2,9 |
30,7 |
3,0 |
31,7 |
3,1 |
32,8 |
3,2 |
33,9 |
3,3 |
34,9 |
3,4 |
36,0 |
3,5 |
37,0 |
3,6 |
38,1 |
3,7 |
39,1 |
3,8 |
40,2 |
3,9 |
41,3 |
4,0 |
42,3 |
4,1 |
43,4 |
4,2 |
44,4 |
4,3 |
45,5 |
4,4 |
46,6 |
4,5 |
47,6 |
4,6 |
48,7 |
4,7 |
49,7 |
4,8 |
50,8 |
4,9 |
51,9 |
5,0 |
52,9 |
5,1 |
54,0 |
5,2 |
55,0 |
5,3 |
56,1 |
5,4 |
57,1 |
5,5 |
58,2 |
5,6 |
59,2 |
5,7 |
60,3 |
5,8 |
61,4 |
5,9 |
62,4 |
6,0 |
63,5 |
6,1 |
64,5 |
6,2 |
65,6 |
6,3 |
66,7 |
6,4 |
67,7 |
6,5 |
68,8 |
6,6 |
69,8 |
6,7 |
70,9 |
6,8 |
71,9 |
6,9 |
73,0 |
7,0 |
74,1 |
7,1 |
75,1 |
7,2 |
76,2 |
7,3 |
77,2 |
7,4 |
78,3 |
7,5 |
79,4 |
7,6 |
80,4 |
7,7 |
81,5 |
7,8 |
82,5 |
7,9 |
83,6 |
8,0 |
84,6 |
8,1 |
85,7 |
8,2 |
86,8 |
8,3 |
87,8 |
8,4 |
88,9 |
8,5 |
89,9 |
8,6 |
91,0 |
8,7 |
92,0 |
8,8 |
93,1 |
8,9 |
94,2 |
9,0 |
95,2 |
9,1 |
96,3 |
9,2 |
97,3 |
9,3 |
98,4 |
9,4 |
99,5 |
9,5 |
100,5 |
9,6 |
101,6 |
9,7 |
102,6 |
9,8 |
103,7 |
9,9 |
104,7 |
Текст документа сверен по:
М.: "Интерсэн", 1998

 В России подорожала водка с 1 января
В России подорожала водка с 1 января  Создайте свой интернет-магазин на новой платформе ReadyScript
Создайте свой интернет-магазин на новой платформе ReadyScript  Хостинг, домены, VPS/VDS, размещение серверов
Хостинг, домены, VPS/VDS, размещение серверов