- USD ЦБ 03.12 30.8099 -0.0387
- EUR ЦБ 03.12 41.4824 -0.0244
|
Краснодар:
|
погода |
Курсы
Индексы
- DJIA 03.12 12019.4 -0.01
- NASD 03.12 2626.93 0.03
- RTS 03.12 1545.57 -0.07
ГОСТ Р 52550-2006
Группа Р26
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Производство лекарственных средств
ОРГАНИЗАЦИОННО-ТЕХНОЛОГИЧЕСКАЯ ДОКУМЕНТАЦИЯ
Manufacturing of medicinal products.
Organizing and technological documentation
ОКС 11.120.10
ОКП 94 5120
Дата введения 2007-01-01
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. N 184-ФЗ "О техническом регулировании", а правила применения национальных стандартов Российской Федерации - ГОСТ Р 1.0-2004 "Стандартизация в Российской Федерации. Основные положения"
Сведения о стандарте
1 РАЗРАБОТАН Общероссийской общественной организацией "Ассоциация инженеров по контролю микрозагрязнений" (АСИНКОМ)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 458 "Правила производства и контроля качества лекарственных средств"
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 2 июня 2006 г. N 105-ст
4 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячно издаваемых информационных указателях "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
Введение
Обязательными требованиями к производству лекарственных средств являются:
- идентичное, стандартное выполнение всех операций;
- прослеживаемость процесса производства каждой серии продукции;
- обеспечение полного соответствия всех этапов производства, исходных и упаковочных материалов, промежуточной и готовой продукции заданным требованиям.
С этой целью производство лекарственных средств должно основываться на системе документации, регламентирующей организацию и технологию производства, контроль качества и документальное оформление всех выполняемых операций. Любое действие должно выполняться в соответствии с документом. Исключаются следование устным распоряжениям и выполнение действий по собственному усмотрению.
Порядок производства лекарственных средств регламентируется системообразующим стандартом ГОСТ Р 52249. Настоящий стандарт детализирует требования ГОСТ Р 52249 в части ведения организационно-технологической документации.
1 Область применения
Настоящий стандарт устанавливает основные требования к организационно-технологической документации, необходимой для производства лекарственных средств по ГОСТ Р 52249, ее содержанию и порядку ведения.
Стандарт не устанавливает конкретные формы документов, требования к их разработке, согласованию, утверждению, хранению и пр., которые определяются самим предприятием - производителем лекарственных средств (ЛС). Приведенные в приложениях образцы документов носят справочный характер.
Стандарт не распространяется на организационно-распорядительную документацию (приказы, распоряжения, должностные инструкции и пр.).
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ Р 51141-98 Делопроизводство и архивное дело. Термины и определения
ГОСТ Р 52249-2004 Правила производства и контроля качества лекарственных средств
ГОСТ Р 52537-2006 Производство лекарственных средств. Система обеспечения качества. Общие требования
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодно издаваемому информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году. Если ссылочный документ заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться замененным (измененным) документом. Если ссылочный документ отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены следующие термины и определения:
3.1 спецификация (specification): Документ, содержащий требования к материалам и продуктам, используемым или получаемым при производстве, являющийся основой для оценки качества лекарственных средств (ГОСТ Р 52249).
3.2 промышленный регламент, технологическая инструкция и инструкция по упаковке: Документы, определяющие все используемые исходные материалы и операции по производству и упаковке продукции (ГОСТ Р 52249).
Примечания
1 Промышленный регламент охватывает все аспекты технологического процесса, требования к качеству сырья, внутрипроизводственному контролю, контролю качества, безопасности труда, экологической безопасности, утилизации отходов и пр.
2 Допускается использование термина "технологический регламент" вместо термина "промышленный регламент".
3.3 инструкция, методика, процедура (procedure, standard operation procedure): Документы, содержащие указания по выполнению отдельных видов операций; например, по очистке, переодеванию, контролю окружающей среды, отбору проб, проведению испытаний, эксплуатации и техническому обслуживанию оборудования (ГОСТ Р 52249).
Примечание - "Стандартная операционная процедура - СОП" - нерекомендуемый термин.
3.4 протокол на серию (record): Документ, отражающий ход производства каждой серии продукции, в т.ч. разрешение на ее реализацию и все факторы, влияющие на качество готовой продукции (ГОСТ Р 52249).
Примечание - Протокол на серию продукции (досье на серию) включает:
- протокол(ы) на производство серии по ГОСТ Р 52249 (подраздел 4.17);
- протокол(ы) на упаковку серии по ГОСТ Р 52249 (подраздел 4.18);
- протоколы контроля исходных и упаковочных материалов, в том числе разрешение на их применение;
- протокол или другой документ по контролю качества готовой продукции;
- разрешение на реализацию серии продукции;
- протоколы на подготовку оборудования, помещений и пр.;
- другие документы (при необходимости).
Данные о проведении основных технологических операций, исполнителях и пр. могут оформляться в виде маршрутных карт.
3.5 учтенные копии: Копии документов, находящиеся на учете в подразделении, контролирующем ведение документации, и в которые вносятся любые изменения для поддержания их соответствия оригиналу.
3.6 серия (batch, or lot): Определенное количество однородных исходных и упаковочных материалов или однородной продукции, обработанной в ходе одной или нескольких последовательных технологических стадий (ГОСТ Р 52249).
Примечание - При необходимости на определенных стадиях производства серия может быть разделена на подсерии, объединяемые впоследствии в однородную серию продукции. При непрерывном производстве понятие серии должно относиться к определенной части продукции, характеризуемой однородностью.
С точки зрения контроля готовой продукции серия продукции включает в себя совокупность единиц дозированной формы лекарственных средств (лекарственной формы), изготовленных из одного объема исходного материала и прошедших единую последовательность производственных операций или единый цикл стерилизации; при непрерывном производстве - все единицы, произведенные в заданный интервал времени.
3.7 организационно-распорядительный документ: Вид письменного документа, в котором фиксируют решение административных и организационных вопросов, а также вопросов управления, взаимодействия, обеспечения и регулирования деятельности органов власти, учреждений, предприятий, организаций, их подразделений и должностных лиц (ГОСТ Р 51141).
4 Общие положения
4.1 Основные требования к документации:
- исчерпывающий характер, т.е. охват всех выполняемых операций, требований к материалам, продукции, методам испытаний и пр.;
- ясно сформулированное наименование и назначение;
- отсутствие лишней информации и ее необоснованного дублирования;
- ясное изложение текста без неопределенности и двусмысленности;
- логичная структура, системное изложение в соответствии с установленным порядком кодирования (рубрикации, нумерации);
- оформление и утверждение в установленном порядке.
4.2 Система документации в производстве лекарственных средств должна соответствовать разрешительной документации и регистрационному досье, требованиям надзорных органов, нормативным и нормативно-правовым документам.
4.3 Следует предусмотреть порядок ведения документации в системе обеспечения качества, включая порядок ее использования, учета и системы нумерации, кодирования и маркирования, а также оформления и рассмотрения полученных данных и протоколов на серию готовой продукции (далее - серию). На предприятии должна быть разработана инструкция, регламентирующая порядок ведения документации.
4.4 Ведение документации в соответствии с установленными требованиями обеспечивает постоянную воспроизводимость при производстве серий продукции, предотвращает ошибки, возникающие при устном общении, неправильном толковании слов, неполной или утерянной информации, дает возможность проследить историю серии продукции и при необходимости выявить причины отклонений, влияющие на качество, и внести коррективы во избежание повторения отклонений в будущем.
4.5 Документы, как правило, не должны быть рукописными. Данные, которые вносятся в бланки рукописным способом, должны быть выполнены четким, разборчивым почерком, так, чтобы эти записи нельзя было аннулировать.
4.6 Документы должны систематически рассматриваться на предмет соответствия текущим требованиям с внесением изменений (при необходимости) и пересматриваться по истечении срока ее действия.
Внесение изменений в документы должно выполняться одновременно с изменением технологического процесса. Не допускается отклонение от требований документов, если изменения не оформлены в установленном порядке. Внесение изменений должно выполняться во все учтенные копии.
4.7 При совершенствовании производства следует своевременно пересматривать систему документации (вносить изменения, удалять неиспользуемую информацию и пр.).
4.8 Технологическая документация должна быть согласована с отделом контроля качества (ОКК). Ее взаимосвязь с документацией по контролю качества обеспечивается путем перекрестных ссылок.
4.9 При необходимости в документах могут быть приведены требования безопасности в виде отдельных пунктов (разделов), относящихся непосредственно к производству данной продукции. По возможности, следует заменять их ссылками на соответствующие документы, которые должны быть проверены и согласованы лицами, ответственными на предприятии за выполнение требований по охране труда и(или) окружающей среды.
4.10 Основой организационно-технологической документации являются законы, технические регламенты, стандарты, фармакопейные статьи и другие нормативные и нормативно-правовые документы.
4.11 Система организационно-технологической документации работает совместно с системой организационно-распорядительной документации по ГОСТ Р 51141, в которую входят устав предприятия, положения о подразделениях, должностные инструкции и пр.
5 Структура организационно-технологической документации
5.1 Виды организационно-технологических документов приведены в таблице 1.
Таблица 1 - Виды организационно-технологических документов
|
Наименование документа |
Назначение |
|
1 Информация о предприятии, регистрационное досье, лицензия на производство и пр. |
Общая документация предприятия |
|
2 Спецификация |
Документ, содержащий требования к материалам или продукции |
|
3 Промышленный регламент, технологическая инструкция, инструкция по упаковке |
Документы, устанавливающие требования к процессам производства конкретной продукции |
|
4 Инструкция (методика) |
Документ, устанавливающий требования, общие для производств различных видов продукции |
|
5 Протокол на серию |
Документ, отражающий фактические данные о производстве конкретной серии продукции |
|
6 Внутрипроизводственная этикетка |
Документ, идентифицирующий материалы или продукцию, содержащие указание их статуса в производстве |
На предприятии также должны использоваться методики аттестации критического оборудования и процессов, протоколы аттестации, документы проведения аудитов (самоинспекций) и пр.
5.2 Содержание информации о предприятии и регистрационного досье регламентируются ГОСТ Р 52537.
5.3 Спецификации
Спецификации составляются для следующих материалов и продукции:
- исходных, вспомогательных и упаковочных материалов;
- промежуточной продукции (при ее наличии);
- готовой продукции.
В спецификации указываются:
- наименование материала (продукции) со ссылкой на внутренний код предприятия (при необходимости);
- ссылку на фармакопейную статью или другой нормативный документ;
- основные характеристики материала (продукции);
- порядок отбора проб и проведения испытаний (ссылки на методику испытания);
- условия хранения и меры предосторожности (ссылки на инструкцию);
- срок годности (хранения) и периодичность повторных испытаний;
- другие данные.
К спецификации должен прилагаться перечень поставщиков и производителей материалов.
Примечание - К вспомогательным материалам относятся фильтрующие элементы, моющие и дезинфицирующие средства и пр.
Примеры форм спецификаций приведены в приложениях А и В.
5.4 Промышленные регламенты, технологические инструкции и инструкции по упаковке
Данные документы разрабатываются для серийного производства продукции и содержат детальное описание технологического процесса с указанием стадий процесса, выполняемых операций, требований к оборудованию, используемым материалам, методам контроля и пр. [1], [2], [3]. В зависимости от назначения могут также разрабатываться лабораторные, опытно-промышленные и пусковые регламенты. Виды технологических регламентов по производству лекарственных средств приведены в приложении С.
Для каждого размера серии продукции разрабатывается промышленный или иной регламент с технологическими инструкциями, в том числе по фасовке и упаковке, утвержденными в установленном порядке. Требования к технологическим инструкциям приведены в приложении D.
5.5 Инструкции и методики
5.5.1 Общие положения
Инструкции и методики охватывают все сферы производства и контроля качества и регламентируют действия, общие для различных видов продукции. Они не включают требования к производству конкретной продукции, которые изложены в промышленном регламенте [2], [3], [4], [5]. Инструкции и методики могут оформляться в виде стандарта предприятия.
Инструкции и методики регламентируют:
- получение и контроль качества исходных и упаковочных материалов;
- контроль качества промежуточной и готовой продукции;
- работу лабораторий;
- аттестацию критических процессов и оборудования;
- работу складов, обращение материалов, промежуточной и готовой продукции;
- технологическое и инженерное оборудование (системы отопления, вентиляции и кондиционирования воздуха, подготовки воды, пара, технологических жидкостей и газов, сжатого воздуха, чистые помещения, эксплуатация, техническое обслуживание и ремонт оборудования, калибровка приборов и т.д.);
- требования к поведению, гигиене и состоянию здоровья персонала;
- порядок ведения документации и т.д.
Персонал должен знать инструкцию и уметь ответить на любой вопрос, касающийся ее. Инструкции не должны содержать лишние данные, не используемые в работе, так как они могут служить причиной признания несоответствия производства требованиям ГОСТ Р 52249.
Инструкции, включая изменения к ним, должны соответствовать требованиям нормативных документов, промышленных регламентов, технической документации на процессы и оборудование.
Инструкции разрабатываются в следующих случаях:
- организации нового производства;
- реконструкции производства;
- введения нового оборудования и процессов или внесения в них изменений;
- изменения нормативных документов, требующего разработки новой инструкции.
Рекомендуемый перечень инструкций, методик и стандартов предприятия приведен в приложении Е.
5.5.2 Содержание инструкции
Настоящий стандарт устанавливает общие требования к содержанию и форме инструкции. Конкретные требования определяются самим предприятием с учетом того, что инструкция должна носить исчерпывающий характер.
При большом объеме инструкции, например, инструкции по техническому обслуживанию, допускается ссылка на другие документы. В этом случае должен быть организован контроль изменений в документах, на которые сделана ссылка.
Рекомендуется включать в инструкцию следующие разделы:
a) общие данные:
- наименование предприятия;
- наименование подразделения;
- наименование инструкции;
- номер инструкции;
- дата утверждения инструкции;
- дата и номер внесения изменения (при необходимости);
- срок действия инструкции;
- данные по истории инструкции (номер и дату прежнего варианта и номера и даты внесения всех изменений);
b) специальные данные:
- область применения инструкции (при необходимости, указание областей, на которые она не распространяется);
- перечень лиц (должностей, подразделений), на которые распространяется инструкция;
- требования к охране окружающей среды (при необходимости) с указанием мер защиты или со ссылкой на соответствующие документы;
- требования техники безопасности и производственной санитарии с указанием средств индивидуальной защиты;
- перечень документов, связанных с данной инструкцией;
- термины и определения (при необходимости);
- содержание инструкции (для инструкций большого объема);
c) основное содержание инструкции в форме пронумерованной последовательности действий с указанием требуемых материалов, оборудования, приборов и документации;
d) прочие данные, например, периодичность обработки оборудования и помещений и пр.;
e) фамилии, инициалы и должности:
- разработчиков инструкции;
- лиц, согласовавших и утвердивших инструкцию;
f) приложения к инструкции.
Инструкция может иметь титульный лист, на котором указываются:
- наименование предприятия,
- наименование подразделения,
- наименование инструкции,
- номер инструкции,
- дата утверждения инструкции,
- дата и номер внесения изменения (при необходимости),
- срок действия инструкции,
- разработчик инструкции,
- фамилии, инициалы и должности лиц, согласовавших и утвердивших инструкцию.
При наличии в инструкции графиков (рисунков) и таблиц они должны иметь сквозную нумерацию и наименования.
Лица, указанные в перечислении b), должны пройти обучение работе по данной инструкции.
При разработке инструкции рекомендуется готовить учебно-методический материал, который может прилагаться к инструкции.
5.5.3 Форма представления инструкции
Форма представления инструкции определяется самим предприятием. В пределах одного предприятия следует использовать единую форму. Пример формы инструкции приведен в приложении F.
5.5.4 Порядок разработки, согласования и утверждения инструкций
Инструкция разрабатывается компетентным сотрудником. Данный сотрудник может входить или не входить в перечень лиц, на которые будет распространяться инструкция.
Разработка инструкции ведется в следующем порядке:
- получение номера разрабатываемой инструкции в отделе, контролирующем ведение документации;
- разработка проекта инструкции;
- обсуждение инструкции и работа в соответствии с ней в опытном порядке с участием тех, кто будет по ней работать; при этом особое внимание следует уделять полноте инструкции и ясности ее изложения;
- доработка инструкции с учетом предложений и замечаний;
- повторное обсуждение инструкции (при необходимости);
- проверка необходимости изменения других документов в случае утверждения данной инструкции (при внесении изменений в инструкцию - проверка необходимости изменений других разделов данной инструкции или других документов);
- согласование инструкции с соответствующими службами (отделами), в том числе службой контроля качества и подразделением, ответственным за ведение документации;
- утверждение инструкции;
- помещение инструкции в электронную базу данных предприятия (если это предусмотрено);
- изготовление необходимого числа копий инструкции с указанием номера копии инструкции и постановка их на учет;
- обучение персонала сразу же после утверждения инструкции.
5.5.5 Порядок представления и хранения инструкций
Инструкции могут быть представлены в бумажном и(или) в электронном виде.
Доступ к инструкциям в электронной форме должны иметь все лица, на которые они распространяются, соответствующие руководители и сотрудники подразделений.
Оригиналы (контрольные экземпляры) хранятся в отделе обеспечения качества или другом подразделении, ответственном за контроль ведения документации.
Пользователь может иметь только действующие учтенные копии, не допускается нахождение у пользователя проектов документов.
Проекты документов должны иметь гриф "ПРОЕКТ".
Подразделение, контролирующее ведение документации, должно следить за недопущением дублирования инструкций и противоречий в инструкциях, привлекая для этого необходимые подразделения.
5.5.6 Пересмотр и внесение изменений
Инструкции должны периодически пересматриваться по истечении срока их действия, но не реже одного раза в два года. При изменениях в оборудовании или процессе вносятся изменения во все инструкции, имеющие к ним отношение.
Рекомендуется ввести электронную систему контроля ведения документации, предупреждающую об окончании срока действия документа и необходимости его пересмотра или внесения изменений.
5.6 Протокол на серию
5.6.1 При разработке технологической документации необходимо предусматривать порядок регистрации хода выполнения операций и получаемых результатов, а также заверения подписями полученных данных. Для этого на предприятии рекомендуется разрабатывать формы документов с изготовлением, при необходимости, бланков для внесения данных (записей) при выполнении операций.
Содержание протоколов на производство серий и протоколов на упаковку серий должно соответствовать промышленному регламенту, технологическим инструкциям и инструкциям на упаковку.
При необходимости бланки для внесения данных (записей) помещают в инструкции в виде приложений.
5.6.2 Такие бланки должны содержать наименования операций (оборудования, параметров и пр.) и графы для регистрации выполнения операций, состояния оборудования, значений параметров и т.д.
Бланки для внесения данных (записей), при необходимости, должны содержать указания по проведению вычислений (см. приложение G).
Бланки следует составлять таким образом, чтобы можно было сравнивать полученные результаты с нормами, указанными в спецификациях и других документах. Они должны содержать указание о необходимости внесения записей в случае отклонений.
Рекомендуется указывать критерии возможности повторного проведения операций в случае отклонения от установленных норм.
На бланке следует предусматривать места для подписей операторов и других лиц, которые проверяют (контролируют) выполнение критических операций и ставят вторую подпись на бланке, а также место для подписей проверяющего (ответственного) лица структурного подразделения.
5.6.3 Бланки для внесения данных должны быть разработаны таким образом, чтобы ведение записей от руки было сведено к минимуму.
Такие бланки следует использовать, например, на этапе подготовки к работе с оборудованием и материалами. Незаполненные поля предназначены для внесения номеров серий, дат, времени, температуры, идентификационных номеров, номеров помещений, номеров оборудования, проведения калибровки, считываемых исходных данных, результатов расчетов.
Бланки должны заполняться персоналом в реальном времени по мере выполнения требований инструкции (методики). Данные регистрируют в последовательности их получения. Заполненные бланки должны гарантировать, что все необходимые данные собраны и ничего не упущено, и являться свидетельством того, что работа была выполнена в соответствии с инструкцией.
5.6.4 На любом заполняемом бланке должно быть указано наименование организации, номер формы и номер ее пересмотренного варианта (или ссылка на инструкцию, если бланк внесен в приложение), номер инструкции, номер серии продукции, указано число страниц.
Контролируемые операции, оборудование, параметры и пр. устанавливаются соответствующей инструкцией. Должен быть определен порядок исправления данных. Например, данные (записи), проставленные по ошибке, должны быть зачеркнуты, а напротив внесенных правильных данных (записей) должна быть проставлена подпись ответственного лица. Удаление данных (записей) любым способом (с помощью ластика, корректирующей жидкости и др.) не допускается.
5.6.5 Все графы бланков должны быть заполнены. Если графа заполняется по мере необходимости, то в ней может ставиться прочерк или другая отметка, однозначно указывающая на отсутствие данных для заполнения. Должно быть предусмотрено свободное место (поля) для записи отклонений от спецификаций, выявленных по ходу выполнения операций.
Если в процессе производства какое-либо действие выполняется по ссылочному протоколу, то в бланке должно быть предусмотрено место для внесения таких записей и указания номера протокола.
5.6.6 Следует документально оформлять выполнение любых операций таким образом, чтобы можно было проследить весь ход производства и контроля качества лекарственного средства. Заполненные и проверенные ответственным лицом протокол на производство серии и протокол на упаковку серии, подписанные (утвержденные) в установленном порядке, входят в состав протокола на серию продукции.
5.6.7 Перед началом любого технологического процесса следует проверять и оформлять протоколом то, что оборудование и рабочая зона освобождены от предыдущей продукции, документов и материалов, не требующихся для планируемого процесса, и являются чистыми и готовыми к эксплуатации.
Содержание протоколов на производство должно соответствовать требованиям ГОСТ Р 52249 (подраздел 4.17).
Примеры протоколов производства серии, подготовленных в форме отдельных бланков, приведены в приложении G.
5.6.8 На каждую произведенную серию или часть серии готовой продукции (при необходимости) следует составлять протокол на упаковку в соответствии с инструкций по упаковке.
Протокол на упаковку должен содержать номер серии и число единиц нерасфасованной продукции, которое должно быть упаковано, а также номер серии и фактическое число единиц готовой продукции.
5.6.9 Перед началом любой операции по упаковке следует проверять и оформлять протоколом то, что оборудование и рабочая зона освобождены от предыдущей продукции, документов и материалов, не требующихся для планируемых операций по упаковке, и что оборудование является чистым и готовым к эксплуатации.
Содержание протоколов на упаковку должно соответствовать требованиям ГОСТ Р 52249 (подраздел 4.18).
Примерное содержание инструкции на упаковку серии и соответствующих протоколов, подготовленных в форме отдельных бланков, приведены в приложении Н.
5.6.10 Для критического оборудования следует вести журналы, отмечая в них, по мере необходимости, все работы по аттестации, калибровке, техническому обслуживанию, очистке, ремонту оборудования с указанием даты и лиц, выполнивших эти работы.
В журналах также следует регистрировать в хронологическом порядке использование критического оборудования и зоны, где обрабатывалась продукция.
Журналы для мониторинга окружающей среды следует вести, если снятие показаний выполняется на месте (например, показаний температуры, давления, влажности).
В протоколе на серию (досье на серию) должна быть сделана ссылка на соответствующую запись в журнале, если это важно при производстве данной серии.
5.6.11 Набор документов, сопровождающих серию готовой продукции, в том числе промышленный регламент, технологические инструкции и инструкции по фасовке и упаковке, другие инструкции и заполняемые бланки, подлежит проверке отделом обеспечения качества на полноту и правильность оформления. Результаты такой проверки должны быть заверены подписью ответственного лица до выдачи разрешения на реализацию серии продукции.
5.7 Внутрипроизводственные этикетки
Рекомендуется разрабатывать систему внутрипроизводственного этикетирования для маркирования:
- исходных материалов;
- промежуточной и готовой продукции;
- оборудования, помещений и зон;
- технологической одежды и т.д.
Внутрипроизводственные этикетки делятся на два вида:
- идентификационные;
- статусные.
В идентификационной этикетке указываются:
- наименование (код) материала или продукта;
- номер серии;
- дата нанесения этикетки (маркировки);
- подпись.
Статусная этикетка (этикетка статуса) содержит информацию о том, где находится материал (продукция, единица оборудования, помещение и пр.) или какую стадию в производственной цепи он прошел (например, "Находится на карантинном хранении (на контроле)", "Прошел карантинное хранение" и т.д.). На ней также следует указывать наименование (код) материала, номер серии и дату.
Информацию о статусе материала (продукции) рекомендуется выделять цветом этикетки, например:
- красный - "Отклонен";
- желтый - "Находится на карантинном хранении (на контроле)";
- зеленый - "Допущен к использованию".
Данные о статусе единицы оборудования, помещения и пр. наносятся на отдельную этикетку, которая помещается на соответствующее оборудование и пр.
Данные об идентификации материала (продукции) и его статусе могут быть нанесены на одну и ту же этикетку.
Примеры оформления этикеток приведены в приложении I.
6 Ведение документации
Порядок ведения документации должен быть определен специальной инструкцией (стандартом предприятия), регламентирующей порядок разработки, утверждения, распространения, использования документов, внесения в них изменений и пр.
6.1 Первым шагом при разработке организационно-технологической документации, соответствующей требованиям ГОСТ Р 52249, должна быть разработка инструкции по ведению документации (стандарта предприятия), устанавливающей порядок составления, пересмотра, утверждения и использования всех необходимых документов, в том числе инструкций, технологических регламентов производства, технологических инструкций, инструкций по фасовке и упаковке, а также ведения протокола на серию готовой продукции. При необходимости могут регламентироваться требования к содержанию, форме, порядку согласования, утверждения и использования (распространения, применения, изъятия) конкретных видов документов.
6.2 Промышленные регламенты производства, технологические инструкции и инструкции по фасовке и упаковке, как правило, разрабатываются на стадии разработки и постановки продукции на производство и корректируются в ходе практического использования в соответствии с принятым порядком внесения изменений.
6.3 Документы, регламентирующие процесс производства, могут быть изменены в связи с появлением новых данных о производстве лекарственного средства. В каждой новой версии должны быть учтены самые последние данные, используемая в данное время технология, нормативные и фармакопейные требования. Новая версия должна также содержать ссылку на предыдущую редакцию, чтобы обеспечить прослеживаемость производства серии продукции. Обоснования изменений следует оформлять протоколом.
Необходимо разработать инструкции, регламентирующие действия, которые следует предпринимать при изменении исходных материалов, других компонентов лекарственного средства, в том числе упаковочных материалов, технологического оборудования, окружающей среды (или производственной зоны), способа производства или метода испытания или любое другое изменение, которое может повлиять на качество продукции или воспроизводимость процесса. Все изменения, влияющие на качество продукции или воспроизводимость процесса, должны быть оформлены документом и утверждены. Необходимо оценить возможное влияние изменения технических средств, систем, оборудования и параметров процессов на качество продукции, в том числе провести анализ рисков. Следует определить необходимость и объем повторной аттестации.
Продукция, произведенная при измененных технологических процессах, не должна быть реализована без осведомленности о данных изменениях ответственного персонала, в том числе Уполномоченного лица.
6.4 Если изменение в технологической документации не влечет за собой изменений в регистрационном досье (не нарушает соответствия между технологической документацией и регистрационным досье), то процедура внесения изменения может регламентироваться соответствующим документом системы управления документацией предприятия. Такое изменение может являться объектом инспектирования на соответствие требованиям ГОСТ Р 52249.
6.5 Если изменение в технологической документации влечет за собой изменения в регистрационном досье, то внесение изменений регламентируется не только документом системы управления документацией предприятия-производителя, но и процедурой, установленной в соответствующих нормативных документах компетентным органом.
6.6 Контроль за внесением изменений
Оригиналы документов (бумажные копии) хранятся в подразделении, отвечающем за ведение документации.
Для практического использования с оригиналов снимаются копии.
Копии могут быть учтенными и неучтенными.
В подразделении, отвечающем за ведение документации, все учтенные копии регистрируются в учетном листе с указанием подразделения и рабочего места, в которых находятся копии.
При внесении изменений разрабатывается новый экземпляр оригинала документа, в котором проставляется номер и дата внесения изменения. Затем изготавливаются копии документа по числу учтенных копий. На каждой учтенной копии проставляется штамп "УЧТЕННАЯ КОПИЯ" с указанием даты оформления копии и лица, выдавшего копию. Учтенная копия выдается в соответствующее подразделение, при этом прежняя копия изымается. Изъятые копии уничтожаются.
Рекомендуется на каждую учтенную копию проставлять штамп "ДЕЙСТВИТЕЛЬНО ДО ________ 20__г." (указание даты).
Неучтенные копии не могут использоваться для работы.
В инструкции должны быть приведены данные о прежнем варианте инструкции и всех изменениях с указанием их номеров и дат.
6.7 Отмена документов
Документ с истекшим сроком действия или замененный документ должны быть изъяты из обращения.
На предприятии должен быть предусмотрен порядок, исключающий обращение или использование отмененных документов или документов с истекшим сроком годности. Например, это может быть предусмотрено системой кодирования и присвоением другого номера, указанием в коде документа номера изменения, автоматической заменой номера (кода) документа по истечению срока его действия и пр.
6.8 Кодирование (обозначение) документов
Документы должны иметь обозначение (код). Система обозначений определяется самим предприятием.
Пример системы кодирования приведен в приложении J.
Порядок кодирования должен быть оформлен отдельной инструкцией.
Приложение А
(справочное)
Пример формы спецификации на материалы
|
Наименование фирмы |
Спецификация |
Номер |
Стр. ___ из ___ | |||
|
Подразделение: Отдел контроля качества |
Дата введения |
Номер редакции ____ | ||||
|
Название инструкции/методики |
||||||
|
Наименование |
Материалы | |||||
|
ТУ |
| |||||
|
Поставщики |
(перечень одобренных поставщиков) | |||||
|
Упаковка и условия хранения |
плотно закрытый контейнер, комнатная температура | |||||
|
Метод отбора проб |
| |||||
|
Наименование показателя |
Результат |
Метод оценки показателя | ||||
|
Внешний вид |
Например: белый кристаллический порошок или белые плоские кристаллы |
Ссылка на методику | ||||
|
Состав (формула) |
Ссылка на методику | |||||
|
Содержание |
не менее ....% и не более ....% по отношению к сухому веществу |
Ссылка на методику | ||||
|
Определение количественных характеристик |
Ссылка на методику | |||||
|
| ||||||
|
Разработал Ф.И.О., |
Согласовал Ф.И.О., |
Утвердил Ф.И.О., | ||||
Приложение В
(справочное)
Пример формы спецификации на промежуточную и готовую продукцию
|
Наименование предприятия |
Спецификация |
номер |
Стр. ____ из ____ стр. | |||||
|
Подразделение: Отдел контроля качества |
Дата введения |
Версия | ||||||
|
Название ______________________________ таблетки, 50 мг | ||||||||
|
| ||||||||
|
N |
Параметры |
Нормы по ФС |
Ссылки на методики | |||||
|
1 |
Описание |
|
||||||
|
2 |
Состав |
|
| |||||
|
3 |
Подлинность |
|
| |||||
|
4 |
Растворение |
|
| |||||
|
5 |
Посторонние примеси |
|
| |||||
|
6 |
Количественное определение |
|
| |||||
|
7 |
Упаковка |
|
||||||
|
8 |
Маркировка |
|
| |||||
|
9 |
Хранение |
|
| |||||
|
10 |
Срок годности |
|
| |||||
|
| ||||||||
|
Штриховой код | ||||||||
|
Отбор проб | ||||||||
|
| ||||||||
|
Разработал Ф.И.О., |
Согласовал Ф.И.О., |
Утвердил Ф.И.О., | ||||||
Приложение С
(справочное)
Виды технологических регламентов по производству
лекарственных средств
С.1 В зависимости от назначения технологические регламенты подразделяются на лабораторные, опытно-промышленные, пусковые и промышленные [1].
С.2 Порядок разработки, экспертизы, согласования и утверждения любого технологического регламента должен предусматривать соответствующий уровень компетенции и квалификации ответственных лиц, утверждающих или согласующих его.
С.3 Лабораторный регламент разрабатывается в соответствии с теми же правилами, что и промышленный регламент, содержит те же разделы и устанавливает методы изготовления продукции и условия, обеспечивающие воспроизводимость технологических процессов в лабораторных условиях со стабильными выходами, правила техники безопасности. Допускается взамен раздела "Технико-экономические нормативы" (ТЭН) внесение в таблицу экспериментальных данных по ТЭН.
С.4 Опытно-промышленный регламент на новую продукцию разрабатывается одновременно с фармакопейной статьей на лекарственное средство и является неотъемлемой частью комплекта технической документации.
Опытно-промышленный регламент на новый вид продукции или технологический процесс, осуществляемый на серийно работающих мощностях промышленного предприятия, должен иметь двойное утверждение организации-разработчика и предприятия-производителя.
С.5 Пусковой и промышленный регламенты утверждаются руководителем фармацевтического предприятия после согласования с организацией-разработчиком технологических процессов, проектной организацией (в случае использования новых/реконструируемых площадей или оборудования) и экспертной организацией по стандартизации требований к закрепленной группе продукции.
С.6 В комплект документов технологического регламента должно входить заключение о результатах научно-технической экспертизы на соответствие требованиям действующих межотраслевых нормативных документов, правил и норм техники безопасности и промышленной санитарии, а также на соответствие организации производства и контроля качества лекарственных средств требованиям ГОСТ Р 52249.
С.7 Промышленные регламенты для взрывоопасных производств, подконтрольных соответствующим надзорным органам в части промышленной и экологической безопасности производств, а также соблюдения санитарно-гигиенических норм должны быть дополнительно согласованы с данными органами.
С.8 В комплект документов промышленного регламента на вновь осваиваемую продукцию должны быть внесены протоколы испытаний производства и протоколы аттестации в соответствии с требованиями ГОСТ Р 52249.
С.9 Квалификация ответственных лиц, утверждающих и согласующих технологический регламент, в том числе руководителя предприятия, должна быть подтверждена соответствующими документами об образовании или повышении квалификации в соответствующей области деятельности.
С.10 Серийный выпуск продукции осуществляется в соответствии с пусковым и промышленным регламентом.
Примечание - Срок действия пускового регламента не должен превышать, как правило, более трех лет.
Регламенты следует регулярно пересматривать с периодичностью один раз в пять лет.
С.11 Разработка, использование и пересмотр технологических регламентов осуществляются в соответствии с инструкцией (стандартом предприятия), регламентирующей порядок ведения документации, утвержденной на предприятии, на основании действующих нормативно-правовых документов.
С.12 Соблюдение требований технологического регламента является обязательным, поскольку он является нормативным документом для производства конкретного лекарственного средства конкретным производителем.
С.13 В соответствии с требованиями ГОСТ Р 52249 технологический регламент должен быть разработан и утвержден для каждого вида (формы) лекарственного средства и определенного размера серии, как правило, с учетом мощности используемого технологического оборудования.
Требования одного технологического регламента могут распространяться на разные дозировки одного наименования лекарственного средства строго определенной лекарственной формы, выпускаемые по одной фармакопейной статье на однотипном оборудовании.
Данное положение полностью согласуется с требованиями общепринятой международной практики производства лекарственных средств.
С.14 Не допускается произвольное изменение объема серии продукции в рамках одного технологического регламента. Любое изменение должно быть обосновано, оформлено ведомостью изменений и зарегистрировано как отдельный промышленный регламент. Не допускается составление и утверждение групповых регламентов даже в производстве с простыми технологическими процессами на однотипном оборудовании.
С.15 Рекомендуется включать в состав технологического регламента следующие разделы:
- характеристика готового продукта;
- химическая схема производства;
- технологическая схема производства;
- аппаратурная схема производства и спецификация оборудования;
- характеристика полупродуктов, исходных и упаковочных материалов;
- изложение технологических процессов;
- материальный баланс;
- переработка и обезвреживание отходов производства;
- контроль производства;
- безопасная эксплуатация производства;
- охрана окружающей среды;
- перечень производственных инструкций;
- технико-экономические нормативы;
- информационные материалы.
С.16 По разделу "Характеристика готового продукта" в соответствии с ГОСТ Р 52249 данные о готовой продукции должны содержать:
- наименование и код продукции в соответствии с требованиями спецификации (нормативного документа), регистрационный номер;
- описание лекарственной формы, ее дозировку и размер серии, состав препарата со ссылкой на соответствующий документ;
- методики отбора образцов и проведения испытаний со ссылкой на соответствующий документ (например, фармакопейную статью), количественные и качественные характеристики, условия хранения и меры предосторожности при применении препарата;
- перечень активных фармацевтических субстанций, ингредиентов и других материалов с точным наименованием и указанием марки, сорта в соответствии с принятой спецификацией (нормативным документом), с указанием их кодов и всех ингредиентов, которые могут преобразовываться в ходе технологического процесса. При этом регламентированные требования спецификаций (нормативных документов) приводятся обязательно;
- установленный выход готовой продукции с указанием допустимых пределов, подтвержденных соответствующими расчетами, согласованными при разработке технологического регламента с экспертной организацией, а также выход на отдельных стадиях производства.
Данные сведения должны подтверждаться в разделах "Характеристика полупродуктов, исходных и упаковочных материалов" и "Материальный баланс".
С.17 Раздел "Характеристика полупродуктов, исходных и упаковочных материалов" должен содержать:
- наименование (в алфавитном порядке) и массу (или другой количественный параметр) каждого ингредиента на каждую дозированную форму;
- полный перечень компонентов с указанием их наименований или кодов и специфических требований, отражающих показатели качества со ссылками на соответствующие нормативные документы;
- описание упаковочно-укупорочных материалов, в том числе образцов или копий всех упаковочных и других видов материалов для маркирования, датированных и подписанных лицом, ответственным за их утверждение.
С.18 Раздел "Аппаратурная схема производства и спецификация оборудования" должен содержать подробное изложение основного технологического и вспомогательного оборудования, которое может оказывать существенное влияние на качество продукции.
Наименования оборудования и приборов приводятся в соответствии с действующими нормативными документами, техническим паспортом и спецификацией поставщика (изготовителя).
Характеристика оборудования должна содержать информацию о материале рабочей зоны оборудования, контактирующей с продуктом в процессе работы, и средствах измерения (датчиках), поверхности которых непосредственно контактируют с продуктом. Соответствие оборудования установленным требованиям должно быть подтверждено сертификатом соответствия либо декларацией соответствия (протоколами испытаний, аттестаций и пр.).
С.19 Раздел "Изложение технологического процесса" помимо точного изложения порядка выполнения технологических операций должен содержать описание технологии и способов упаковки и маркирования.
В заключительной части раздела на каждой стадии производства указываются возможные отклонения от технологического процесса, приводящие к браку или возникновению аварийных ситуаций, а также меры их предупреждения.
С.20 Раздел "Материальный баланс" должен содержать полную информацию о теоретическом значении выхода продукции на каждой стадии производства с указанием максимального и минимального показателей выхода, при превышении которых требуется проведение расследования в соответствии с порядком, установленным на предприятии.
С.21 В разделе "Контроль производства" содержится перечень важнейших контрольных точек производства, требующих соблюдения установленного технологического режима в целях обеспечения стабильного качества выпускаемой продукции. Любое изменение контрольных точек следует оформлять как изменение регламента. Например, необходимо указывать предельное количество остаточного материала (сырья, полуфабриката от предыдущей серии), добавляемого к последующей серии, порядок их предварительной подготовки и контроль, а также сроки использования.
С.22 Раздел "Безопасная эксплуатация производства" должен содержать характеристики опасностей производства, исчерпывающий перечень сведений, подтверждающих безопасность готового продукта, сырья, полупродуктов и субстанций с указанием соответствующих нормативов, методы их контроля, а также заключение специализированных компетентных организаций о возможности обеспечения безопасных условий ведения всех технологических процессов.
Раздел должен содержать утвержденные методы и способы подготовки к работе помещений, оборудования и персонала, порядок получения разрешения на использование, а также наименования веществ и рецептуры для санитарной обработки.
С.23 В разделе "Перечень производственных инструкций" указываются обозначения (коды) и наименования инструкций, содержащих:
- данные о месте нахождения производства и основного оборудования;
- требования к подготовке основного оборудования (очистке, сборке, калибровке, поверке, стерилизации и другим операциям);
- подробное изложение стадий технологического процесса, в том числе требования к контролю материалов, предварительной обработке, последовательности внесения материалов, времени перемешивания, температуре и др.;
- описание всех видов внутрипроизводственного контроля с указанием допустимых пределов контроля и ответственных лиц;
- условия хранения нерасфасованной продукции, требования к упаковке, маркированию, специальные условия хранения (при необходимости);
- специальные меры предосторожности.
С.24 Не рекомендуется внесение изменений в обязательные разделы регламента без оформления и регистрации ведомости изменений или нового регламента, если таких существенных изменений более трех.
Приложение D
(справочное)
Технологические инструкции и инструкции по фасовке и упаковке
D.1 Для каждого размера серии производимого лекарственного средства необходимо иметь утвержденный технологический регламент с технологическими инструкциями, в том числе по фасовке и упаковке.
Технологические инструкции, разработанные в соответствии с ГОСТ Р 52249, должны полностью соответствовать технологическому регламенту и содержать следующее:
- данные о месте ведения процесса и используемом оборудовании;
- порядок проведения подготовки необходимого оборудования или ссылки на инструкции (методики) (например, очистки, монтажа, калибровки, стерилизации);
- подробно изложенные правила, порядок и режимы выполнения каждого действия (например, проверки сырья, предварительной обработки, порядка загрузки сырья, времени смешивания, температурные режимы);
- описание действий по любому внутрипроизводственному контролю с указанием предельных значений контролируемых параметров;
- при необходимости требования к хранению нерасфасованной продукции, в том числе требования к производственной таре, маркированию и специальным условиям хранения, где это требуется;
- особые меры предосторожности;
- порядок заполнения первичной технологической документации в ходе выполнения работ.
D.2 Инструкции по фасовке и упаковке должны соответствовать технологическому регламенту, содержать следующие сведения или ссылки на инструкции, содержащие следующие сведения:
- наименование лекарственного средства;
- описание его лекарственной формы и содержание действующего вещества;
- количество лекарственного средства в упаковке, выраженное в штуках, единицах массы или объема, либо других единицах измерения с указанием, при необходимости, допустимых отклонений;
- полный перечень всех упаковочных материалов, требуемых для серии определенного размера, в том числе количество, размеры и типы материалов с указанием кода на каждый упаковочный материал согласно спецификациям;
- при необходимости образец или копию соответствующих маркированных упаковочных материалов с наличием свободного места для отметки номера серии и срока годности продукции;
- особые меры предосторожности, в том числе указание о тщательной проверке зоны оборудования с целью подтверждения очистки зоны перед началом работы;
- описание процесса фасовки и упаковки, в том числе основных и вспомогательных операций и используемого оборудования;
- подробное описание технологического контроля со ссылками на методику отбора проб (образцов) и допустимыми предельными значениями контролируемых параметров.
D.3 Последовательность разделов технологических инструкций должна соответствовать порядку выполнения основных производственных операций.
Первый раздел должен включать информацию о подготовке производства, а именно: очистке, подготовке оборудования, исходных материалах и т.д. Вместо полного описания всех процедур и контроля, выполняемого в процессе подготовки производства, рекомендуется приводить ссылки на соответствующие инструкции (методики).
D.4 В технологической инструкции следует приводить данные о помещениях (внутренний код) и используемом оборудовании; причем каждая единица оборудования должна иметь наименование, тип и индивидуальный номер, чтобы обеспечить прослеживаемость производства каждой серии продукции. В инструкциях приводится указание о необходимости идентификации оборудования в процессе его использования этикетками с номером серии и видом продукции.
D.5 В инструкции рекомендуется указывать все вещества, используемые в технологическом процессе, код для каждого из них (при наличии), а также требуемое количество для производства серии и ссылки на инструкции по взвешиванию или отмериванию. Кроме того, следует указывать номера серий, ссылки на спецификации и методики испытаний, даты выдачи разрешения на использование и(или) номер документа, подтверждающего качество.
Примечание - Эти данные приводятся на основании соответствующих документов по контролю качества.
Необходимо привести также сведения об ожидаемом выходе готовой продукции с указанием допустимых пределов.
Для каждого ингредиента могут быть указаны допускаемые верхние и нижние предельные значения действительного количества вещества по отношению к номинальному количеству в технологическом регламенте производства на серию в зависимости от количественного содержания.
Пределы приемлемости от 95% до 105% номинального количества для действующих веществ и пределы от 90% до 110% номинального количества для вспомогательных веществ не требуют дополнительного обоснования.
D.6 Могут допускаться более широкие пределы приемлемости, которые должны быть обоснованы доказательством, что серии с составом, близким к значениям предлагаемых нижних и верхних пределов приемлемости, продолжают соответствовать спецификациям на готовую продукцию.
Если количество используемого действующего вещества рассчитывается из действительного количественного содержания вещества в данной серии ("факторизация"), то это должно быть указано. Если для того, чтобы общая масса серии готовой продукции была равна массе, предусмотренной в производственной рецептуре на серию, используются другие вещества, то это также должно быть указано.
В инструкциях по фасовке и упаковке необходимо указать количество полученной нерасфасованной продукции и материалы, необходимые для ее упаковки с указанием номера серии и(или) документа, подтверждающего их качество.
D.7 Следует приводить схему технологического процесса с указанием последовательности основных операций, точек введения исходных материалов в процесс и по ходу процесса, в которых проводится отбор проб (образцов) и технологический контроль. На такой схеме рекомендуется выделять критические процессы.
Операции, не специфичные для производства конкретной продукции, например, связанные с подготовкой оборудования, в технологической инструкции не приводятся.
Следует также привести поэтапные указания по выполнению каждой стадии и операции технологического процесса. Указания для каждой стадии следует нумеровать и начинать с новой страницы для того, чтобы иметь возможность выдавать исполнителям именно те части документов, которые необходимы для выполнения запланированных операций.
D.8 В технологических инструкциях и инструкциях по фасовке и упаковке необходимо описать каждое действие на данной стадии, последовательность действий и технологические параметры процесса (например, проверку исходных материалов, порядок загрузки исходных материалов, время смешивания, температурные режимы и другое). Следует также привести все точки контроля в процессе производства со ссылками на методику, в соответствии с которыми проводится данный контроль.
Раздел "Контроль процесса упаковки" должен включать в себя проверку:
- общего вида упаковки;
- соответствия упаковочного материала упаковываемой продукции;
- правильности маркирования;
- правильности работы устройств контроля на линии упаковки и т.д.
Необходимо указать, что изъятые на какой-либо стадии образцы продукции не должны использоваться в текущем технологическом процессе.
D.9 При необходимости следует указывать дату (время) начала и окончания отдельных стадий производства либо их продолжительность, если они строго регламентированы для данной продукции. Должен быть приведен порядок получения, передачи и сдачи продукции с указанием сопроводительной документации.
Необходимо также регламентировать действия персонала при возникновении отклонений от заданных параметров или нарушении стандартного хода выполнения технологических операций.
Описание каждой стадии технологического процесса должно заканчиваться сведениями об ожидаемом выходе продукции с указанием допустимых пределов. При необходимости следует привести требования составления баланса на данной стадии.
В инструкциях по фасовке и упаковке должно быть указано, что оставшиеся маркированные упаковочные материалы подлежат уничтожению со ссылкой на инструкцию по уничтожению, а возврат на склад упаковочных материалов, на которых не был проставлен номер серии, проводится согласно соответствующей инструкции с оформлением протокола возврата.
Инструкции по упаковке должны завершаться указанием о подведении баланса между количеством нерасфасованной продукции, упаковочных материалов и полученной готовой продукции. Выполнение каждой операции должно подтверждаться подписью исполнителя и контролирующего лица.
В заключении технологической инструкции и инструкции по фасовке и упаковке следует привести ссылки на инструкцию по удалению отходов и очистке помещений и оборудования, а также образцы этикеток, которыми маркируют произведенную продукцию на период ожидания результатов контроля готовой продукции. Следует указать статус продукции "Находится на карантинном хранении", а также условия ее хранения, в том числе тару, способы маркирования и другие специальные условия.
D.10 В качестве приложений инструкции должны содержать формы или иметь ссылки на прилагаемые протоколы, в которых фиксируются данные или информация в целях документального подтверждения выполнения технологических операций в соответствии с инструкцией. По критическим технологическим операциям в формах наряду с описанием подобных операций следует предусматривать место для подписи руководителя производства и контролирующего лица.
Приложение Е
(справочное)
Рекомендуемый перечень инструкций, методик и стандартов предприятия
1 Инструкция (стандарт предприятия) по разработке, утверждению, распространению, использованию документов, внесению в них изменений и пр.
2 Инструкция по взвешиванию и выдаче сырья.
3 Инструкция по эксплуатации оборудования.
4 Инструкция по внутризаводской маркировке.
5 Инструкция по предотвращению перекрестного загрязнения.
6 Инструкция по производству различной продукции в одной зоне.
7 Инструкция по возвращению на склад остатков сырья и материалов.
8 Инструкция по переработке забракованной продукции.
9 Инструкция по формированию досье на серию готовой продукции.
10 Инструкция по учету отклонений и выполнению корректирующих действий в процессе производства.
11 Инструкция по отзыву продукции с рынка и работе с рекламациями.
12 Инструкция по уничтожению забракованной, возвращенной и отозванной продукции.
13 Инструкция по учету движения промаркированных упаковочных материалов.
14 Инструкция по уничтожению упаковочных и маркированных материалов.
15 Инструкция по оценке здоровья персонала.
16 Инструкция по личной гигиене персонала.
17 Инструкция по переодеванию и ношению одежды.
18 Инструкция по обработке одежды.
19 Инструкция по входу в чистые помещения.
20 Инструкция по очистке, уборке, дезинфекции помещений.
21 Инструкция по удалению остатков дезинфицирующих средств с обработанных поверхностей.
22 Инструкция по очистке и санитарной обработке трубопроводов.
23 Инструкция по борьбе с паразитами, насекомыми и животными.
24 Инструкция по обучению персонала.
25 Методики по аттестации процессов и оборудования.
26 Инструкция по техническому обслуживанию оборудования.
27 Инструкция по очистке оборудования.
28 Инструкция по стерилизации оборудования.
29 Инструкция по очистке упаковочных линий.
30 Инструкция по монтажу.
31 Инструкция по аудиту поставщиков.
32 Инструкция по приемке исходных материалов.
33 Инструкция по приемке упаковочных материалов.
34 Инструкция по карантинному хранению.
35 Инструкция по хранению исходных и упаковочных материалов.
36 Инструкция по идентификации исходных и упаковочных материалов.
37 Инструкция по обращению с животными.
38 Инструкция по контролю окружающей среды.
Приложение F
(справочное)
Пример формы инструкции (методики)
|
Наименование предприятия |
||||||||||||||||||
|
Инструкция |
||||||||||||||||||
|
наименование |
||||||||||||||||||
|
N |
Версия |
Дата |
||||||||||||||||
|
Подразделение |
||||||||||||||||||
|
Отдел |
||||||||||||||||||
|
Разработана |
||||||||||||||||||
|
Назначение | ||||||||||||||||||
|
Место и время применения | ||||||||||||||||||
|
Исполнитель | ||||||||||||||||||
|
Лицо, контролирующее выполнение инструкции | ||||||||||||||||||
|
Материалы и оборудование Приводится точный перечень материалов и оборудования, необходимых для выполнения инструкции. | ||||||||||||||||||
|
Утверждена (подпись) | ||||||||||||||||||
|
Дата введения в действие |
Взамен |
|||||||||||||||||
|
стр. |
из |
|||||||||||||||||
Приложение G
(справочное)
Примеры форм протоколов производства серии
Протокол 1
|
Наименование ЛС | |||||||||||||||||||
|
Код |
Номер серии |
Объем серии |
|||||||||||||||||
|
Контроль подготовки производства |
|||||||||||||||||||
|
(до начала работы): |
|||||||||||||||||||
|
|
Код оборудования |
Проверено ________________ |
Начальник смены |
Контролирующее лицо ОКК | |||||||||||||||
|
Да (+) |
Нет (-) |
Да (+) |
Нет (-) | ||||||||||||||||
|
1 |
|
Санитарная подготовка помещения проведена |
|||||||||||||||||
|
2 |
Вытяжная система проверена |
||||||||||||||||||
|
3 |
Система подачи воздуха проверена |
||||||||||||||||||
|
4 |
Наличие очищенной воды в сборнике проверено |
||||||||||||||||||
|
5 |
Подача сжатого воздуха проверена |
||||||||||||||||||
|
6 |
22 |
Реактор |
|
||||||||||||||||
|
7 |
23 |
Реактор |
|
||||||||||||||||
|
8 |
24 |
Реактор |
|
||||||||||||||||
|
9 |
6/1 |
Реактор |
|
||||||||||||||||
|
10 |
6/2 |
Реактор |
|||||||||||||||||
|
11 |
11/1 |
Сборник |
|||||||||||||||||
|
12 |
11/2 |
Сборник |
|||||||||||||||||
|
13 |
13 |
Весы ПТ-10 очищены и откалиброваны |
|||||||||||||||||
|
14 |
14 |
Весы ПВ-30 очищены и откалиброваны |
|||||||||||||||||
|
15 |
Оборудование маркировано |
||||||||||||||||||
|
16 |
|
Инвентарь очищен |
|||||||||||||||||
|
Начальник смены |
|||||||||||||||||||
|
Дата |
Подпись |
||||||||||||||||||
|
Контролирующее лицо |
|||||||||||||||||||
|
Дата |
Подпись |
||||||||||||||||||
|
Замечания: | |||||||||||||||||||
|
Протокол проверил | |||||||||||||||||||
|
Должность, подпись |
Дата | ||||||||||||||||||
Продолжение (обратная сторона) протокола 1
|
Наименование ЛС | ||||||||
|
Код |
Номер серии |
Объем серии | ||||||
|
Ежесменный осмотр зоны приготовления (начальник смены) | ||||||||
|
Дата |
Смена |
Время |
Подпись | |||||
|
|
|
|
| |||||
|
|
|
|
| |||||
|
|
|
|
| |||||
|
|
|
|
| |||||
|
|
|
|
| |||||
|
|
|
|
| |||||
|
|
|
|
| |||||
|
|
|
|
||||||
|
|
|
|
| |||||
|
|
|
|
| |||||
|
|
|
|
| |||||
|
Очистка зоны приготовления по окончании процесса (начальник смены) | ||||||||
|
Дата |
Смена |
Время |
Подпись | |||||
|
|
||||||||
|
Замечания: | ||||||||
|
Протокол проверил | ||||||||
|
Должность, подпись |
Дата | |||||||
Протокол 2
|
Наименование ЛС | |||||||||||||
|
Код |
Номер серии |
Объем серии | |||||||||||
|
Расчет компонентов | |||||||||||||
|
Наименование сырья |
Код |
Номер серии |
Номер аналитического листка |
Содержание основного вещества |
Формула для расчета, расчет требуемого количества | ||||||||
|
|
|
| |||||||||||
|
|
|
| |||||||||||
|
|
|
| |||||||||||
|
|
|
| |||||||||||
|
|
|
| |||||||||||
|
|
|
| |||||||||||
|
|
|
| |||||||||||
|
|
|
||||||||||||
|
Расчет выполнил | |||||||||||||
|
Должность, подпись |
Дата |
||||||||||||
|
Расчет выполнил | |||||||||||||
|
Должность, подпись |
Дата |
||||||||||||
|
Замечания: | |||||||||||||
|
Протокол проверил | |||||||||||||
|
Должность, подпись |
Дата | ||||||||||||
Протокол 3
|
Наименование ЛС | ||||||||||||
|
Код |
Номер серии |
Объем серии | ||||||||||
|
Взвешивание компонентов | ||||||||||||
|
Наименование сырья |
Единица |
Требуемое количество |
Номер серии |
Взвешенное количество |
Подпись | |||||||
|
|
Масса тары |
Брутто |
Нетто |
испол- |
контроли- | |||||||
|
|
| |||||||||||
|
|
| |||||||||||
|
|
| |||||||||||
|
|
| |||||||||||
|
|
| |||||||||||
|
|
| |||||||||||
|
|
||||||||||||
|
|
||||||||||||
|
| ||||||||||||
|
| ||||||||||||
|
| ||||||||||||
|
| ||||||||||||
|
|
||||||||||||
|
| ||||||||||||
|
Замечания: | ||||||||||||
|
Протокол проверил | ||||||||||||
|
Должность, подпись |
Дата | |||||||||||
Протокол 4
|
Наименование ЛС | |||||||||||
|
Код |
Номер серии |
Объем серии | |||||||||
|
Отбор проб (контролирующее лицо ОКК в присутствии начальника смены) | |||||||||||
|
Дата/время |
Номер предъявительского извещения |
Количество пробы, мл (г) |
Подпись | ||||||||
|
начальник смены |
контролирующее лицо ОКК | ||||||||||
|
Результаты испытаний (лицо ОКК) | |||||||||||
|
Номер протокола испытаний |
"Дальнейшее производство разрешено" |
"Дальнейшее производство | |||||||||
|
| |||||||||||
|
Фильтрование раствора Х | |||||||||||
|
Подать раствор из реактора 6/1,2 в сборник 11/1,2, давление азота не более 2 ATM | |||||||||||
|
Дата/смена |
Время |
Давление по манометру |
Выполнил (аппаратчик) |
Проверил | |||||||
|
|
начало |
конец |
|
|
| ||||||
|
|
|||||||||||
|
Заменить фильтровальный элемент на патронных фильтрах 12/1,2, подать раствор из сборника 11/1,2, давление азота не более 2 ATM | |||||||||||
|
Дата/смена |
Время |
Давление по манометру |
Выполнил (аппаратчик) |
Проверил | |||||||
|
|
начало |
конец |
|
|
| ||||||
|
|
|||||||||||
|
Замечания: | |||||||||||
|
Протокол проверил | |||||||||||
|
Должность, подпись |
Дата | ||||||||||
Протокол 5
|
Должность, |
|
|
|||||||||||||
|
Код |
Номер серии |
Объем серии | |||||||||||||
|
Корректировка N | |||||||||||||||
|
Номер протокола испытаний |
Несоответствующий показатель |
Описание корректирующих действий | |||||||||||||
|
|
|||||||||||||||
|
|
|||||||||||||||
|
|
|||||||||||||||
|
Расчет компонентов | |||||||||||||||
|
Наименование сырья |
Код |
Номер серии |
Номер аналитического листка |
Содержание основного вещества |
Формула для расчета, расчет требуемого количества | ||||||||||
|
|
|
| |||||||||||||
|
|
|
| |||||||||||||
|
|
|
| |||||||||||||
|
|
|
| |||||||||||||
|
|
|
| |||||||||||||
|
|
|
| |||||||||||||
|
|
| ||||||||||||||
|
Корректирующие действия |
|
||||||||||||||
|
Расчет проверил |
Должность, подпись |
||||||||||||||
|
Замечания: | |||||||||||||||
|
Протокол проверил | |||||||||||||||
|
Должность, подпись |
Дата | ||||||||||||||
Продолжение (обратная сторона) протокола 5
|
Взвешивание компонентов | ||||||||||||||||||||||||||
|
Наименование сырья |
Единица измерения |
Требуемое количество |
Номер серии |
Взвешенное количество |
Подпись исполнителя | |||||||||||||||||||||
|
|
|
Масса тары |
Брутто |
Нетто |
||||||||||||||||||||||
|
При взвешивании присутствовал | ||||||||||||||||||||||||||
|
Контролирующее лицо ОКК |
Дата |
Подпись | ||||||||||||||||||||||||
|
| ||||||||||||||||||||||||||
|
Указание аппаратчику (действия, параметры процесса) |
Фактические параметры процесса |
Подпись исполнителя | ||||||||||||||||||||||||
|
Проконтролировал | ||||||||||||||||||||||||||
|
Начальник смены |
Дата |
Подпись |
||||||||||||||||||||||||
|
Отбор проб | ||||||||||||||||||||||||||
|
Дата/время |
Номер предъявительского извещения |
Количество пробы, мл (г) |
Подпись | |||||||||||||||||||||||
|
Начальник смены |
Контролирующее лицо ОКК | |||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||
|
Результаты испытаний (контролирующее лицо ОКК) | ||||||||||||||||||||||||||
|
Номер протокола испытаний |
"Дальнейшее производство разрешено" |
"Дальнейшее производство запрещено" | ||||||||||||||||||||||||
|
Подпись |
Подпись | |||||||||||||||||||||||||
|
Замечания: | ||||||||||||||||||||||||||
|
Протокол проверил | ||||||||||||||||||||||||||
|
Должность, подпись |
Дата |
|||||||||||||||||||||||||
Форма
извещения о предъявлении продукции на испытания
(предъявительского извещения)
|
Наименование предприятия | ||||||||||||||||||
|
Цех |
||||||||||||||||||
|
Начальнику |
||||||||||||||||||
|
Извещение N | ||||||||||||||||||
|
Наименование продукции |
||||||||||||||||||
|
Стадия технологического процесса |
||||||||||||||||||
|
Номер серии |
||||||||||||||||||
|
Количество (шт., кг и т.д.) |
||||||||||||||||||
|
Предъявленная продукция наработана |
||||||||||||||||||
|
согласно нормативным документам |
||||||||||||||||||
|
Продукцию предъявил |
||||||||||||||||||
|
должность, Ф.И.О., подпись |
||||||||||||||||||
|
Дата |
Время |
|||||||||||||||||
|
Проба отработана согласно инструкции |
||||||||||||||||||
|
Масса (объем) пробы |
||||||||||||||||||
|
Дата отбора пробы |
Время |
|||||||||||||||||
|
Фамилия контролирующего лица |
Подпись |
|||||||||||||||||
|
Протокол проверил | ||||||||||||||||||
|
Должность, подпись |
Дата |
|||||||||||||||||
Приложение Н
(справочное)
Пример инструкции по упаковке и протоколов упаковки.
Инструкция по упаковке флаконов в индивидуальную тару
1 Цель
Предоставление необходимых сведений для выполнения процесса упаковки в индивидуальную пачку ручным способом.
2 Область применения
Участок упаковки.
3 Персонал
Исполнитель: оператор.
Процесс контролируют мастер и контролирующее лицо ОКК.
4 Оборудование и инвентарь
Тележки транспортные.
Стол накопительный.
Емкость для сбора бракованных пачек.
Емкость для сбора бракованных листков-вкладышей.
Емкость для сбора бракованных флаконов.
5 Сырье и материалы
Флаконы анкетированные.
Пачки картонные промаркированные.
Инструкции по медицинскому применению (листки-вкладыши).
6 Порядок проведения
6.1 Подготовительные работы
Мастер в зоне комплектации должен скомплектовать материалы в соответствии с "Заданием на упаковку" (см. протокол 1). Получить необходимое число инструкций и пачек на складе упаковочных материалов согласно инструкции "Порядок получения упаковочных материалов со склада". Выкатить с помощью оператора из зоны карантина в зону комплектации задания тележки с анкетированными флаконами, пересчитать, сделать отметку в протоколе "Комплектация задания" (см. протокол 1).
Контролирующее лицо отдела контроля качества должно проверить комплектацию задания; число единиц, идентичность кода, идентичность маркировки с отметкой в протоколе "Комплектация задания" (см. протокол 1).
Мастер и контролирующее лицо отдела контроля качества должны проконтролировать очистку зоны упаковывания в индивидуальную пачку согласно инструкции "Очистка зоны упаковки" с записью в "Листе контроля очистки" (см. протокол 2). Необходимо убедиться, что рабочая зона, оборудование и инвентарь являются свободными от любых использовавшихся ранее лекарственных средств, материалов, документов.
Мастер должен промаркировать зону упаковки идентификационной этикеткой.
Оператор под контролем мастера должен выкатить из зоны комплектации задания в зону упаковки тележки с анкетированными флаконами.
Мастер должен выдать оператору подготовленные на задание:
- инструкции по медицинскому применению (листки-вкладыши);
- промаркированные картонные пачки.
Заполнить и выдать "Протокол упаковки в пачку" (см. протокол 3) и "Задание на упаковку".
Выданные оператору инструкции по медицинскому применению (листки-вкладыши) и пачки поместить отдельно друг от друга в свободные лотки.
6.2 Основные работы
Оператор должен снять лоток с флаконами с тележки и поставить на накопительный стол. Рядом поставить пустой лоток. Сесть за накопительный стол напротив лотков с флаконами, справа от себя поставить лоток с листками-вкладышами, слева - лоток с пачками.
Сложить инструкцию по размеру пачки. Сложить пачку по намеченным сгибам, вложить листок-вкладыш в пачку. Вложить флакон в пачку, пачку закрыть. Упакованную пачку поставить в свободный лоток.
Заполненный пачками лоток поставить на свободную тележку.
Внимание! Оператор в процессе упаковки обязан проверять:
- идентичность инструкций по медицинскому применению (листков-вкладышей) и пачек, сравнивая их с образцами упаковочных материалов в "Задании на упаковку";
- идентичность маркировки флаконов и пачек, сравнивая со штампом в "Задании на упаковку". Материалы, не соответствующие образцам, отбраковывать;
- качество упаковываемых материалов. Помятые инструкции по медицинскому применению (листки-вкладыши) и пачки, а также имеющие типографский брак (пробелы в тексте, размытости, смещения штрих-кода и т.д.), необходимо отбраковывать. Флаконы с нарушенной герметичностью упаковки либо имеющие дефект в нанесении этикетки (плохое качество наклейки, размытый штамп, неправильное расположение этикетки) также необходимо отбраковывать.
Обнаруженный брак следует собирать по наименованиям в идентично промаркированные емкости для сбора брака.
Мастеру и контролирующему лицу отдела контроля качества с установленной периодичностью (например один раз в час) следует проверять качество упаковки с записью в протоколе упаковки (см. протокол 3), а именно:
- идентичность пачки (согласно заданию на упаковку);
- наличие и идентичность инструкции по медицинскому применению (листка-вкладыша) в пачке;
- наличие флакона;
- качество складывания пачки;
- отсутствие брака у печатных упаковочных материалов и флаконов.
Заключительные работы
Мастер должен подсчитать:
- число упакованных в пачку флаконов;
- число бракованных инструкций по медицинскому применению (листков-вкладышей), пачек, флаконов;
- число оставшихся инструкций по медицинскому применению (листков-вкладышей), пачек, флаконов.
Примечание - Подсчет инструкций по медицинскому применению (листков-вкладышей) и пачек может проводиться путем взвешивания.
Внести данные в протокол расхода упаковочных материалов (см. протокол 4). Составить баланс расхода материалов.
Подсчитать отклонения в балансе. Сравнить с допустимым отклонением. Если отклонение превышает допустимое, то провести повторный подсчет.
Подсчитать фактический выход продукции. Теоретический выход продукции на стадии упаковки в индивидуальную пачку составляет 99,6%. Подсчитать отклонение от теоретического выхода, сравнить с допустимым. Допустимое отклонение составляет 0,3%. Данные внести в протокол расхода.
Уничтожить промаркированные неиспользованные и бракованные пачки и бракованные флаконы согласно инструкции "Уничтожение неиспользованных или бракованных упаковочных материалов с переменной информацией".
Вернуть на склад упаковочных материалов неиспользованные и бракованные инструкции по медицинскому применению (листки-вкладыши) в соответствии с инструкцией "Возврат неиспользованных или бракованных упаковочных материалов без переменной информации".
Оператор должен перевезти тележки с упакованной в пачку продукцией в зону карантина для последующего упаковывания в термоусадочную пленку. Каждую тележку промаркировать идентификационной этикеткой.
Оператор должен провести очистку зоны упаковки в соответствии с инструкцией "Очистка зоны упаковки".
Мастер должен проконтролировать очистку, сделать запись в листе контроля очистки (см. протокол 2).
Все протоколы сдать технологу цеха.
Протокол 1
|
Наименование ЛС | |||||||||||||||
|
Код |
Номер серии |
Объем серии | |||||||||||||
|
Задание на упаковку | |||||||||||||||
|
Штамп |
Код инструкции |
Код пачки | |||||||||||||
|
Серия |
Образец |
Образец | |||||||||||||
|
Годен до |
Приклеить образец инструкции |
Приклеить образец пачки | |||||||||||||
|
Начальник цеха |
Дата |
Подпись |
|||||||||||||
|
Начальник ОКК |
Дата |
Подпись |
|||||||||||||
|
Комплектация задания | |||||||||||||||
|
Наименование исходного сырья и вспомогательных веществ |
Задание на комплектацию (планируемое) |
Комплектация задания (склад цеха) | |||||||||||||
|
Код продукта |
Количество |
Серия (по анал. листу) |
Количество | ||||||||||||
|
|
|||||||||||||||
|
|
|||||||||||||||
|
|
|||||||||||||||
|
Начальник цеха |
Дата |
Подпись |
|||||||||||||
|
Контролирующее лицо ОКК |
Дата |
Подпись |
|||||||||||||
|
Замечания: | |||||||||||||||
|
Протокол проверил | |||||||||||||||
|
Должность, подпись |
Дата |
||||||||||||||
Протокол 2
|
Наименование ЛС | |||||||||||||
|
Код |
Номер серии |
Объем серии | |||||||||||
|
Лист контроля очистки зоны упаковки в индивидуальную пачку | |||||||||||||
|
N |
Проверено |
Мастер |
Контролирующее лицо ОКК | ||||||||||
|
1 |
Листки-вкладыши предыдущего ЛС удалены |
| |||||||||||
|
2 |
Пачки предыдущей серии |
| |||||||||||
|
3 |
Не упакованные в пачку флаконы предыдущей серии удалены |
| |||||||||||
|
4 |
Упакованные в пачку флаконы предыдущей серии удалены |
|
| ||||||||||
|
5 |
Документация предыдущей серии удалена |
|
| ||||||||||
|
6 |
Транспортные тележки, лотки удалены |
|
| ||||||||||
|
7 |
Накопительные столы очищены |
| |||||||||||
|
8 |
Емкости для сбора брака очищены |
|
| ||||||||||
|
9 |
Пол в зоне линии очищен |
|
| ||||||||||
|
Мастер |
Дата |
Подпись |
|||||||||||
|
Контролирующее лицо ОКК |
Дата |
Подпись |
|||||||||||
|
Очистка зоны упаковки (после окончания процесса) | |||||||||||||
|
Дата, смена |
Время |
Подпись мастера | |||||||||||
|
|
|||||||||||||
|
Замечания: | |||||||||||||
|
Протокол проверил | |||||||||||||
|
Должность, подпись |
Дата |
||||||||||||
Протокол 3
|
Наименование ЛС | ||||||||||||||
|
Код |
Номер серии |
Объем серии | ||||||||||||
|
Протокол упаковки флаконов в индивидуальную пачку | ||||||||||||||
|
Дата/смена |
Время |
Фамилия оператора | ||||||||||||
|
|
начало |
окончание |
| |||||||||||
|
|
||||||||||||||
|
Контроль процесса упаковывания (мастер, контролирующее лицо ОКК) | ||||||||||||||
|
1 проверка |
2 проверка |
3 проверка |
4 проверка | |||||||||||
|
Ф.И.О. проверяющего |
мастер |
контро- |
мастер |
контро- |
мастер |
контро- |
мастер |
контро- | ||||||
|
1 |
Время |
|||||||||||||
|
2 |
Идентичность пачки |
|||||||||||||
|
3 |
Наличие и идентичность листка-вкладыша |
|||||||||||||
|
4 |
Наличие флакона |
|||||||||||||
|
5 |
Качество складывания пачки |
|||||||||||||
|
6 |
Отсутствие брака |
|||||||||||||
|
Подпись |
||||||||||||||
|
Замечания: | ||||||||||||||
|
Протокол проверил | ||||||||||||||
|
Должность, подпись |
Дата |
|||||||||||||
Протокол 4
|
Наименование ЛС | |||||||||||
|
Код |
Номер серии |
Объем серии | |||||||||
|
Расход упаковочных материалов на серию | |||||||||||
|
Наименование |
Флаконы, шт. |
Пачка, шт. |
Инструкция по медицинскому применению (листок-вкладыш), шт. | ||||||||
|
Код |
|
|
| ||||||||
|
Упаковано в пачку |
|
|
| ||||||||
|
Всего |
|
| |||||||||
|
Количество до упаковывания |
|
|
| ||||||||
|
Отклонение, % |
|
|
| ||||||||
|
Допустимое отклонение, % |
0,2 |
2 |
2 | ||||||||
|
Выход продукции | |||||||||||
|
Теоретический выход, шт. |
Фактический выход, шт. |
Отклонение, % |
Допустимое отклонение, % | ||||||||
|
|
|
|
0,3 | ||||||||
|
Подсчет произвел | |||||||||||
|
Мастер |
Дата |
Подпись |
|||||||||
|
Контролирующее лицо ОКК |
Дата |
Подпись |
|||||||||
|
Замечания: | |||||||||||
|
Протокол проверил | |||||||||||
|
Должность, подпись |
Дата |
||||||||||
Продолжение (обратная сторона) протокола 4
|
Подсчет упаковочных материалов методом взвешивания | |||||||||
|
Наименование |
Брак |
Остаток в цехе | |||||||
|
Масса = |
Масса = | ||||||||
|
Масса = |
Масса = | ||||||||
|
Масса = |
Масса = | ||||||||
|
Подсчет произвел | |||||||||
|
Мастер |
Дата |
Подпись |
|||||||
|
Замечания: | |||||||||
|
Протокол проверил | |||||||||
|
Должность, подпись |
Дата |
||||||||
Приложение I
(справочное)
Примеры внутрипроизводственных этикеток.
Этикетка контроля качества ОКК
|
Предприятие |
КОНТРОЛЬ КАЧЕСТВА |
||||
|
| |||||
|
Субстанция |
|||||
|
Поставщик |
|||||
|
Код |
|||||
|
Серия N |
Анализ N |
||||
|
Оценка |
|||||
|
Дата |
Подпись |
||||
|
| |||||
Этикетка взвешивания
|
Этикетка взвешивания | |||||||||||||
|
Предприятие | |||||||||||||
|
Субстанция |
Годен до | ||||||||||||
|
Дата поступления | |||||||||||||
|
Код |
Масса партии, г | ||||||||||||
|
Производитель |
Число мест | ||||||||||||
|
Партия N |
Брутто | ||||||||||||
|
|
Тара | ||||||||||||
|
|
Нетто | ||||||||||||
|
Дата взвеши- |
Остаток |
Расход |
Общий остаток |
Выдал Ф.И.О., |
Принял, взвесил | ||||||||
|
|
Место, номер, вид тары |
Число в таре |
Взве- |
Остаток |
|
| |||||||
|
|
|
|
|
|
|
|
| ||||||
|
|
|
|
|
|
|
|
|
| |||||
|
|
|
|
|
|
|
|
|
| |||||
|
|
|
|
|
|
|
| |||||||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
| |||||
|
|
|
|
|
|
|
|
|
| |||||
|
|
|
|
|
|
|
|
|
| |||||
|
|
|
|
|
|
|
|
|
| |||||
|
|
|||||||||||||
|
|
|||||||||||||
|
|
|||||||||||||
Этикетка статуса оборудования
|
Предприятие |
Производство | |||||||
|
Участок | ||||||||
|
Статус оборудования | ||||||||
|
Наименование | ||||||||
|
Номер |
Дата | |||||||
|
Использовалось для |
Можно использовать для | |||||||
|
Наименование продукции |
Наименование продукции | |||||||
|
Серия |
Серия | |||||||
|
Подпись контролирующего лица ОКК |
||||||||
Этикетка оценки качества
|
Предприятие |
КОНТРОЛЬ КАЧЕСТВА ОКК | |||||||||
|
Лекарственное средство |
Форма | |||||||||
|
Стадия процесса | ||||||||||
|
Серия N |
Срок годности | |||||||||
|
Оценка контроля качества |
||||||||||
|
Анализ N |
Дата |
Подпись | ||||||||
Приложение J
(справочное)
Пример системы кодирования
Система кодирования документов может иметь алфавитно-цифровое обозначение.
Пример схемы кодирования документов.
|
Вид документа |
Подразделение |
Вид оборудования |
Операция |
|
И |
Ц5У2 |
ТП |
О |
Вид документа:
- И - инструкция;
- С - спецификация;
- М - методика;
- ПР - промышленный регламент;
- ПС - протокол серии.
Подразделение:
- Ц5У2 - цех 5, участок 2.
Вид оборудования:
- ТП - таблет-пресс.
Операция:
- очистка ежедневная - О1.
Таким образом, кодированное обозначение данной инструкции имеет вид: И-Ц5У2-ТП-О1.
Библиография
|
[1] ОСТ 64-02-003-2002 |
Продукция медицинской промышленности. Технологические регламенты производства. - М.: ГипроНИИмедпром, 2002 | |
|
[2] СТБ 1433-2004 |
Производство лекарственных средств. Технологическая документация. - Минск, Госстандарт, 2004 | |
|
[3] Руководство 42-01-2003 |
Лекарственные средства. Технологический процесс. Документация. - Киев, Морион, 2003 | |
|
[4] |
A WHO guide to good manufacturing practice (GMP) requirements. Part 1: Standard operating procedures and master formulae - Geneva: World Health Organization, 1997 | |
|
[5] |
Кодекс Федеральных правил США, титул 21 для лекарственных средств и пищевых продуктов | |
Текст документа сверен по:
официальное издание
М.: Стандартинформ, 2006

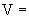 0,4 м
0,4 м очищен
очищен  Светлана Бессараб: все социальные обязательства государства будут выполнены
Светлана Бессараб: все социальные обязательства государства будут выполнены  Создайте свой интернет-магазин на новой платформе ReadyScript
Создайте свой интернет-магазин на новой платформе ReadyScript  Хостинг, домены, VPS/VDS, размещение серверов
Хостинг, домены, VPS/VDS, размещение серверов