- USD ЦБ 03.12 30.8099 -0.0387
- EUR ЦБ 03.12 41.4824 -0.0244
|
Краснодар:
|
погода |
Курсы
Индексы
- DJIA 03.12 12019.4 -0.01
- NASD 03.12 2626.93 0.03
- RTS 03.12 1545.57 -0.07
ГОСТ 23268.9-78
Группа Р19
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ВОДЫ МИНЕРАЛЬНЫЕ ПИТЬЕВЫЕ ЛЕЧЕБНЫЕ,
ЛЕЧЕБНО-СТОЛОВЫЕ И ПРИРОДНЫЕ СТОЛОВЫЕ
Методы определения нитрат-ионов
Drinking medicinal, medicinal-table and natural-table mineral waters.
Methods of determination of nitrate-ions
Дата введения 1980-01-01
ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета СССР по стандартам от 1 сентября 1978 г. N 2413
Ограничение срока действия снято по протоколу N 4-93 Межгосударственного Совета по стандартизации, метрологии и сертификации (ИУС 4-94)
ИЗДАНИЕ с Изменением N 1, утвержденным в декабре 1979 г. (ИУС 2-80).
Настоящий стандарт распространяется на лечебные, лечебно-столовые и природные столовые питьевые минеральные воды и устанавливает колориметрические и потенциометрические методы определения нитрат-ионов.
1. ОТБОР ПРОБ
1.1. Отбор проб - по ГОСТ 23268.0-91.
1.2. Объем пробы воды для определения нитрат-ионов должен быть не менее 50 см .
.
1.3. Анализы выполняют в день вскрытия пробы.
2. КОЛОРИМЕТРИЧЕСКИЙ МЕТОД ОПРЕДЕЛЕНИЯ С ДИФЕНИЛАМИНОМ
Метод предназначен для быстрого определения предельно допустимого содержания нитрат-ионов в минеральных водах.
2.1. Сущность метода
Метод основан на окислении дифениламина нитрат-ионами с образованием окрашенного в синий цвет хиноидного производного дифенилбензидина. Метод позволяет определять нитрат-ионы от 0,001 до 0,005 мг в пробе.
2.2. Аппаратура, материалы и реактивы
Весы технические типа ВЛТ-200.
Весы аналитические лабораторные.
Посуда мерная стеклянная лабораторная по ГОСТ 1770-74, вместимостью: колбы 50, 100, 500, 1000 см ; цилиндры 10 см
; цилиндры 10 см .
.
Приборы мерные лабораторные стеклянные вместимостью: пипетки 1, 2, 5 и 10 см ; бюретки 2 см
; бюретки 2 см .
.
Стаканы стеклянные лабораторные по ГОСТ 25336-82.
Пробирки стеклянные по ГОСТ 25336-82.
Палочки стеклянные.
Термометры ртутные стеклянные лабораторные жидкостные по ГОСТ 28498-90.
Вода дистиллированная по ГОСТ 6709-72.
Натрий хлористый по ГОСТ 4233-77.
Калий азотнокислый по ГОСТ 4217-77.
Дифениламин по НТД.
Кислота серная по ГОСТ 4204-77.
Все реактивы должны быть квалификации х.ч. или ч.д.а.
2.3. Подготовка к анализу
2.3.1. Приготовление основного стандартного раствора азотнокислого калия
Основной стандартный раствор готовят из азотнокислого калия по ГОСТ 4212-76.
1 мл раствора содержит 1 мг нитрат-ионов.
2.3.2. Приготовление рабочего стандартного раствора азотнокислого калия (раствор N 1)
10 см основного стандартного раствора азотнокислого калия вносят в мерную колбу вместимостью 1000 см
основного стандартного раствора азотнокислого калия вносят в мерную колбу вместимостью 1000 см и объем раствора доводят дистиллированной водой до метки. Раствор готовят в день проведения анализа.
и объем раствора доводят дистиллированной водой до метки. Раствор готовят в день проведения анализа.
1 см раствора содержит 0,01 мг нитрат-ионов.
раствора содержит 0,01 мг нитрат-ионов.
2.3.3. Приготовление рабочих стандартных растворов азотнокислого калия (растворы N 2, 3 и 4)
В мерные колбы вместимостью 50 см отмеривают 5,0; 10,0 и 25,0 см
отмеривают 5,0; 10,0 и 25,0 см рабочего стандартного раствора N 1 и объем раствора доводят дистиллированной водой до метки. Растворы готовят в день проведения анализа.
рабочего стандартного раствора N 1 и объем раствора доводят дистиллированной водой до метки. Растворы готовят в день проведения анализа.
1 см раствора N 2 содержит 0,001 мг, раствора N 3 - 0,002 мг, раствора N 4 - 0,005 мг нитрат-ионов.
раствора N 2 содержит 0,001 мг, раствора N 3 - 0,002 мг, раствора N 4 - 0,005 мг нитрат-ионов.
2.3.4. Приготовление основного раствора дифениламинового реактива (раствор N 5)
0,1 г дифениламина взвешивают с погрешностью не более ±0,0002 г, помещают в мерную колбу вместимостью 100 см , осторожно растворяют в серной кислоте и доводят объем раствора этой же кислотой до метки.
, осторожно растворяют в серной кислоте и доводят объем раствора этой же кислотой до метки.
Серная кислота не должна содержать окислителей, придающих раствору дифениламина синюю окраску. Допустимо лишь слабо-голубое окрашивание. Для освобождения от окислителей 150-200 см серной кислоты нагревают до выделения густых белых паров.
серной кислоты нагревают до выделения густых белых паров.
2.3.5. Приготовление рабочего раствора дифениламинового реактива (раствор N 6)
В мерную колбу вместимостью 100 см приливают 38 см
приливают 38 см дистиллированной воды, добавляют 5 см
дистиллированной воды, добавляют 5 см раствора N 5, объем раствора осторожно доводят концентрированной серной кислотой до метки, перемешивают и отстаивают от 3 до 5 сут. Реактив должен быть бесцветным.
раствора N 5, объем раствора осторожно доводят концентрированной серной кислотой до метки, перемешивают и отстаивают от 3 до 5 сут. Реактив должен быть бесцветным.
2.3.6. Приготовление 10%-ного раствора хлористого натрия
10 г хлористого натрия растворяют в 90 см дистиллированной воды
дистиллированной воды
2.3.7. Подготовка пробы
В мерную колбу вместимостью 100 см отмеривают 10 см
отмеривают 10 см анализируемой воды и объем раствора доводят до метки дистиллированной водой, не содержащей нитрат- и нитрит-ионов.
анализируемой воды и объем раствора доводят до метки дистиллированной водой, не содержащей нитрат- и нитрит-ионов.
2.4. Проведение анализа
В сухую пробирку вносят 1 см подготовленной пробы. Одновременно готовят эталонные растворы с содержанием нитрат-ионов 0,0; 1,0; 2,0 и 5,0 мг/дм
подготовленной пробы. Одновременно готовят эталонные растворы с содержанием нитрат-ионов 0,0; 1,0; 2,0 и 5,0 мг/дм , для чего в такие же пробирки вносят соответственно по 1 см
, для чего в такие же пробирки вносят соответственно по 1 см растворов N 2, 3, 4.
растворов N 2, 3, 4.
К содержимому пробирок прибавляют из микробюретки по 0,1 см 10%-ного раствора хлористого натрия, осторожно приливают по 2,5 см
10%-ного раствора хлористого натрия, осторожно приливают по 2,5 см дифениламинового реактива (раствор N 6), перемешивают стеклянной палочкой и помещают в стакан с водой при температуре от 18 °С до 22 °С. Через 2,5 ч сравнивают интенсивность цвета анализируемого раствора с интенсивностью цвета эталонных растворов.
дифениламинового реактива (раствор N 6), перемешивают стеклянной палочкой и помещают в стакан с водой при температуре от 18 °С до 22 °С. Через 2,5 ч сравнивают интенсивность цвета анализируемого раствора с интенсивностью цвета эталонных растворов.
2.5. Обработка результатов
Массовую концентрацию нитрат-ионов (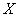 ), мг/дм
), мг/дм , вычисляют по формуле
, вычисляют по формуле
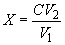 ,
,
где 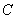 - массовая концентрация нитрат-ионов, определенных по шкале эталонных растворов, мг/дм
- массовая концентрация нитрат-ионов, определенных по шкале эталонных растворов, мг/дм ;
;
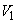 - объем анализируемой воды, взятой для разведения, см
- объем анализируемой воды, взятой для разведения, см ;
;
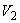 - объем, до которого разбавлена проба, см
- объем, до которого разбавлена проба, см .
.
3. КОЛОРИМЕТРИЧЕСКИЙ МЕТОД ОПРЕДЕЛЕНИЯ
С ФЕНОЛДИСУЛЬФОНОВОЙ КИСЛОТОЙ
При разногласиях в оценке качества минеральной питьевой лечебной, лечебно-столовой и природной столовой воды применяют колориметрический метод определения с фенолдисульфоновой кислотой.
3.1. Сущность метода
Метод основан на образовании желтого соединения в результате реакции нитрат-ионов с фенолдисульфоновой кислотой. Метод позволяет определять от 0,005 до 5 мг нитрат-ионов в пробе.
3.2. Аппаратура, материалы и реактивы
Посуда мерная стеклянная лабораторная по ГОСТ 1770-74, вместимостью: колбы 50, 100, 500, 1000 см ; цилиндры 50, 100 см
; цилиндры 50, 100 см .
.
Колбы стеклянные конические по ГОСТ 25336-82, вместимостью 100 и 150 см .
.
Приборы мерные лабораторные стеклянные вместимостью: пипетки 2, 5, 10, 50 см ; бюретки 5, 10, 25 см
; бюретки 5, 10, 25 см .
.
Цилиндры колориметрические вместимостью 50 см .
.
Посуда лабораторная фарфоровая по ГОСТ 9147-80 - чашки выпарные.
Палочки стеклянные.
Фильтры стеклянные по ГОСТ 25336-82.
Стаканы стеклянные лабораторные по ГОСТ 25336-82.
Холодильник стеклянный лабораторный по ГОСТ 25336-82.
Шкаф сушильный лабораторный с терморегулятором.
Баня водяная.
Весы лабораторные аналитические.
Весы технические типа ВЛТ-200.
Бумага индикаторная универсальная.
Плитка электрическая по ГОСТ 14919-83.
Натрий хлористый по ГОСТ 4233-77.
Фенол по НТД.
Кислота серная по ГОСТ 4204-77.
Аммиак водный по ГОСТ 3760-79.
Серебро сернокислое.
Метиловый оранжевый.
Калия гидроокись.
Соль динатриевая этилендиамин -  - тетрауксусной кислоты, 2-водная (трилон Б) по ГОСТ 10652-73.
- тетрауксусной кислоты, 2-водная (трилон Б) по ГОСТ 10652-73.
Калий азотнокислый по ГОСТ 4217-77.
Все реактивы должны быть квалификации х.ч. или ч.д.а.
3.3. Подготовка к анализу
3.3.1. Приготовление раствора фенолдисульфоновой кислоты
25 г кристаллического бесцветного фенола взвешивают с погрешностью не более 0,01 г, помещают в колбу вместимостью 200 см , осторожно приливают 150 см
, осторожно приливают 150 см концентрированной серной кислоты и нагревают 6 ч на кипящей водяной бане с обратным холодильником. Полученную фенолдисульфоновую кислоту хранят в склянке из темного стекла с притертой пробкой.
концентрированной серной кислоты и нагревают 6 ч на кипящей водяной бане с обратным холодильником. Полученную фенолдисульфоновую кислоту хранят в склянке из темного стекла с притертой пробкой.
3.3.2. Приготовление раствора трилона Б (комплексона III)
50 г комплексона III взвешивают с погрешностью не более 0,01 г и смешивают в фарфоровой чашке с 20 см дистиллированной воды. Полученную массу растворяют в 50 см
дистиллированной воды. Полученную массу растворяют в 50 см концентрированного раствора аммиака.
концентрированного раствора аммиака.
3.3.3. Основной стандартный раствор азотнокислого калия приготавливают по п.2.3.1.
3.3.4. Приготовление рабочего стандартного раствора азотнокислого калия
100 см основного стандартного раствора помещают в мерную колбу вместимостью 1000 см
основного стандартного раствора помещают в мерную колбу вместимостью 1000 см и доводят дистиллированной водой до метки.
и доводят дистиллированной водой до метки.
1 см раствора содержит 0,1 мг нитрат-ионов.
раствора содержит 0,1 мг нитрат-ионов.
3.3.5. Приготовление эталонных растворов азотнокислого калия
В фарфоровые чашки вносят 0,00; 0,25; 0,50; 1,00; 2,50; 5,00; 7,50; 10,00; 15,00; 20,00 и 25,00 см рабочего стандартного раствора, выпаривают досуха на водяной бане, и после охлаждения к сухому остатку приливают по 2 см
рабочего стандартного раствора, выпаривают досуха на водяной бане, и после охлаждения к сухому остатку приливают по 2 см раствора фенолдисульфоновой кислоты, тщательно растирая стеклянной палочкой до получения однородной массы, осторожно растворяют в 20 см
раствора фенолдисульфоновой кислоты, тщательно растирая стеклянной палочкой до получения однородной массы, осторожно растворяют в 20 см дистиллированной воды, затем помешивая добавляют 7 см
дистиллированной воды, затем помешивая добавляют 7 см концентрированного раствора аммиака. Каждый из полученных растворов количественно переносят в колориметрические цилиндры вместимостью 50 см
концентрированного раствора аммиака. Каждый из полученных растворов количественно переносят в колориметрические цилиндры вместимостью 50 см , и содержимое каждого цилиндра доводят до метки дистиллированной водой и перемешивают.
, и содержимое каждого цилиндра доводят до метки дистиллированной водой и перемешивают.
Полученные растворы содержат соответственно 0,0; 0,5; 1,0; 2,0; 5,0; 10,0; 15,0; 20,0; 30,0; 40,0 и 50,0 мг/дм нитрат-ионов. Эталонные растворы пригодны для использования в течение месяца при хранении в закрытых сосудах в темном месте.
нитрат-ионов. Эталонные растворы пригодны для использования в течение месяца при хранении в закрытых сосудах в темном месте.
Допускается приготовление неполной шкалы эталонных растворов в пределах предполагаемых значений нитрат-ионов для анализируемой воды.
3.3.6. Приготовление раствора сернокислого серебра
4,40 г сернокислого серебра взвешивают с погрешностью не более 0,01 г, помещают в мерную колбу вместимостью 1000 см , растворяют в дистиллированной воде и объем раствора доводят дистиллированной водой до метки.
, растворяют в дистиллированной воде и объем раствора доводят дистиллированной водой до метки.
1 см раствора сернокислого серебра соответствует 1 мг хлорид-ионов.
раствора сернокислого серебра соответствует 1 мг хлорид-ионов.
3.3.7. Приготовление 0,1 н. раствора серной кислоты
Раствор готовят из фиксанала. Содержимое ампулы для приготовления 0,1 н. раствора серной кислоты количественно переносят в мерную колбу вместимостью 1000 см и объем раствора доводят дистиллированной водой до метки.
и объем раствора доводят дистиллированной водой до метки.
3.4. Проведение анализа
Определению мешают хлорид-ионы, влияние которых устраняют по ходу анализа. В коническую колбу вместимостью 250 см вводят от 10 до 100 см
вводят от 10 до 100 см анализируемой воды с таким расчетом, чтобы в ней содержалось не более 5 мг нитрат-ионов. К пробе приливают 0,1 н. раствор серной кислоты до тех пор, пока рН, контролируемый по индикаторной бумаге, не достигнет 4.
анализируемой воды с таким расчетом, чтобы в ней содержалось не более 5 мг нитрат-ионов. К пробе приливают 0,1 н. раствор серной кислоты до тех пор, пока рН, контролируемый по индикаторной бумаге, не достигнет 4.
Добавляют раствор сернокислого серебра в количестве, эквивалентом содержанию хлорид-ионов, которые определяют из отдельной пробы по ГОСТ 23268.17-78. Содержимое колбы слегка подогревают и выпавший осадок хлористого серебра отфильтровывают. Прозрачный фильтрат количественно переносят в фарфоровую чашку и выпаривают досуха на водяной бане. После охлаждения к сухому остатку приливают 2 см раствора фенолдисульфоновой кислоты, тщательно растирают стеклянной палочкой до получения однородной массы, осторожно растворяют в 20 см
раствора фенолдисульфоновой кислоты, тщательно растирают стеклянной палочкой до получения однородной массы, осторожно растворяют в 20 см дистиллированной воды и при помешивании добавляют 7 см
дистиллированной воды и при помешивании добавляют 7 см концентрированного раствора аммиака. В случае выпадения осадка гидроокисей металлов прибавляют по каплям аммиачный раствор комплексона III до полного растворения осадка. Прозрачный раствор количественно переносят в колориметрический цилиндр вместимостью 50 см
концентрированного раствора аммиака. В случае выпадения осадка гидроокисей металлов прибавляют по каплям аммиачный раствор комплексона III до полного растворения осадка. Прозрачный раствор количественно переносят в колориметрический цилиндр вместимостью 50 см , объем раствора доводят дистиллированной водой до метки и содержимое перемешивают. Интенсивность цвета анализируемого раствора сравнивают с интенсивностью цвета эталонных растворов.
, объем раствора доводят дистиллированной водой до метки и содержимое перемешивают. Интенсивность цвета анализируемого раствора сравнивают с интенсивностью цвета эталонных растворов.
3.5. Обработка результатов
Массовую концентрацию нитрат-ионов (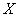 ), мг/дм
), мг/дм , вычисляют по формуле
, вычисляют по формуле
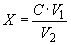 ,
,
где 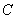 - нитрат-ионы, определенные по шкале эталонных растворов, мг/дм
- нитрат-ионы, определенные по шкале эталонных растворов, мг/дм ;
;
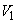 - объем колориметрируемой пробы, см
- объем колориметрируемой пробы, см ;
;
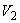 - объем воды, взятый для анализа, см
- объем воды, взятый для анализа, см .
.
За окончательный результат принимают среднее арифметическое значение двух параллельных определений, допускаемые расхождения между которыми не должны превышать 0,5 мг/дм .
.
4. ПОТЕНЦИОМЕТРИЧЕСКИЙ МЕТОД ОПРЕДЕЛЕНИЯ НИТРАТ-ИОНОВ
4.1. Сущность метода
Метод основан на прямом определении нитрат-ионов с использованием ионоселективного электрода.
Метод позволяет определять нитрат-ионы в минеральных водах любой минерализации при содержании их от 10 до 70 мг/дм с относительной ошибкой 10%.
с относительной ошибкой 10%.
4.2. Аппаратура, материалы и реактивы
Прибор для измерения величины потенциала, типа рН-метр - милливольтметр (рН-340; рН-121) или иономер ЭВ-74.
Электрод сравнения хлорсеребряный насыщенный образцовый, 2-го разряда по ГОСТ 17792-72.
Нитратселективный электрод "Квант".
Весы лабораторные аналитические.
Весы технические типа ВЛТ-200.
Шкаф сушильный.
Секундомер.
Бумага фильтровальная по ГОСТ 12026-76.
Приборы мерные лабораторные стеклянные вместимостью: бюретки 50 см ; пипетки 1,25 см
; пипетки 1,25 см .
.
Посуда мерная лабораторная стеклянная по ГОСТ 1770-74, вместимостью: цилиндры 50 см (исполнения 2 или 4) и 1000 см
(исполнения 2 или 4) и 1000 см ; колбы 100, 1000 см
; колбы 100, 1000 см .
.
Стаканчики для взвешивания (бюксы) по ГОСТ 25336-82.
Стаканы и колбы стеклянные лабораторные по ГОСТ 25336-82, вместимостью: стаканы 50 и 1000 см ; колбы конические 1000 см
; колбы конические 1000 см .
.
Воронки стеклянные по ГОСТ 25336-82.
Натрий хлористый по ГОСТ 4233-77.
Квасцы алюмокалиевые по ГОСТ 4329-77.
Калий азотнокислый по ГОСТ 4217-77.
Вода дистиллированная по ГОСТ 6709-72.
Все реактивы должны быть квалификации х.ч. или ч.д.а.
4.3. Подготовка к анализу
4.3.1. Приготовление основного стандартного раствора азотнокислого калия
Азотнокислый калий высушивают в сушильном шкафу при температуре (105±5) °С до постоянной массы.
10,1107 г азотнокислого калия взвешивают на аналитических весах с погрешностью не более ±0,0002 г. Навеску помещают в мерную колбу вместимостью 1000 см , растворяют в дистиллированной воде и объем раствора доводят дистиллированной водой до метки.
, растворяют в дистиллированной воде и объем раствора доводят дистиллированной водой до метки.
1 см раствора содержит 1·10
раствора содержит 1·10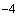 г·молей азотнокислого калия.
г·молей азотнокислого калия.
4.3.2. Приготовление рабочих стандартных растворов
В мерные колбы вместимостью 100 см каждая приливают при помощи бюретки вместимостью 50 см
каждая приливают при помощи бюретки вместимостью 50 см основной стандартный раствор в количестве 1; 10; 20; 30; 40; 50 см
основной стандартный раствор в количестве 1; 10; 20; 30; 40; 50 см и объемы растворов доводят дистиллированной водой до метки.
и объемы растворов доводят дистиллированной водой до метки.
1 см раствора содержит соответственно: 1·10
раствора содержит соответственно: 1·10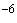 (раствор N 1); 1·10
(раствор N 1); 1·10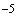 ( )(раствор N 2); 2·10
( )(раствор N 2); 2·10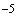 (раствор N 3); 3·10
(раствор N 3); 3·10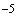 (раствор N 4); 4·10
(раствор N 4); 4·10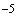 (раствор N 5); 5·10
(раствор N 5); 5·10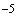 (раствор N 6) г·молей азотнокислого калия.
(раствор N 6) г·молей азотнокислого калия.
Рабочие стандартные растворы готовят в день построения градуировочного графика.
4.3.3. Приготовление буферного раствора (10%-ный раствор алюмокалиевых квасцов)
100,00 г алюмокалиевых квасцов АlК (SO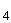 )
)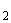 ·12Н
·12Н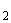 О взвешивают на технических весах с погрешностью не более ±0,01 г. Навеску помещают в коническую колбу и растворяют в 900 см
О взвешивают на технических весах с погрешностью не более ±0,01 г. Навеску помещают в коническую колбу и растворяют в 900 см дистиллированной воды. Для ускорения растворения раствор слегка подогревают.
дистиллированной воды. Для ускорения растворения раствор слегка подогревают.
4.3.4. Приготовление раствора хлористого натрия
Готовят раствор с массовой концентрацией хлорид-ионов, равной массовой концентрации их в исследуемой воде. Массовую концентрацию хлорид-ионов в исследуемой воде определяют по ГОСТ 23268.17-78. Массу навески рассчитывают исходя из массовой концентрации хлорид-ионов в исследуемой воде.
Хлористый натрий взвешивают на технических весах с погрешностью не более ±0,01 г. Навеску помещают в мерную колбу вместимостью 1000 см , растворяют в дистиллированной воде и объем раствора доводят до метки дистиллированной водой.
, растворяют в дистиллированной воде и объем раствора доводят до метки дистиллированной водой.
4.3.5. Подготовка прибора к испытаниям
Новый измерительный нитратселективный электрод выдерживают в основном стандартном растворе азотнокислого калия не менее 12 ч. Перед началом работы его присоединяют к клемме прибора для измерения величины потенциала "Изм.", промывают дистиллированной водой, а остатки воды с электрода удаляют фильтровальной бумагой. В качестве электрода сравнения используют хлорсеребряный электрод.
По окончании работы нитратселективный электрод и наконечник электролитического ключа обмывают дистиллированной водой.
Между анализами нитратселективный электрод хранят в стаканчике с рабочим стандартным раствором N 1, а наконечник элктролитического ключа - в стаканчике с дистиллированной водой.
4.4. Проведение анализа
На характер градуировочного графика влияют ионная сила раствора и присутствующие в воде хлорид-ионы в количестве более 500 мг/дм . Влияние ионной силы устраняют добавлением буферного раствора. Влияние хлорид-ионов при массовой концентрации их от 500 до 2000 мг/дм
. Влияние ионной силы устраняют добавлением буферного раствора. Влияние хлорид-ионов при массовой концентрации их от 500 до 2000 мг/дм устраняют введением в стандартные растворы при построении градуировочного графика хлористого натрия в количестве, равном его массовой концентрации в исследуемой воде. Массовую концентрацию хлорид-ионов в воде определяют по ГОСТ 23268.17-78.
устраняют введением в стандартные растворы при построении градуировочного графика хлористого натрия в количестве, равном его массовой концентрации в исследуемой воде. Массовую концентрацию хлорид-ионов в воде определяют по ГОСТ 23268.17-78.
4.4.1. Определение нитрат-ионов в водах, содержащих менее 500 мг/дм хлорид-ионов
хлорид-ионов
В мерный цилиндр с притертой пробкой вместимостью 50 см отмеривают пипетками вместимостью 25 см
отмеривают пипетками вместимостью 25 см исследуемой воды и 25 см
исследуемой воды и 25 см буферного раствора. Раствор перемешивают. Подготовленную пробу используют для трех параллельных измерений. Для этого в стаканчик вместимостью 50 см
буферного раствора. Раствор перемешивают. Подготовленную пробу используют для трех параллельных измерений. Для этого в стаканчик вместимостью 50 см отливают около
отливают около 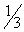 полученного раствора, погружают в него нитратселективный электрод и наконечник электролитического ключа. Потенциал электрода измеряют при помощи прибора для измерения величины потенциала. Показания прибора снимают через 30 с после погружения электрода.
полученного раствора, погружают в него нитратселективный электрод и наконечник электролитического ключа. Потенциал электрода измеряют при помощи прибора для измерения величины потенциала. Показания прибора снимают через 30 с после погружения электрода.
4.4.1.1. Построение градуировочного графика
В мерные цилиндры с притертой пробкой вместимостью 50 см вносят при помощи пипетки вместимостью 1 см
вносят при помощи пипетки вместимостью 1 см соответственно по 0,5 см
соответственно по 0,5 см рабочих стандартных растворов N 1-6, затем в каждый цилиндр приливают пипеткой вместимостью 25 см
рабочих стандартных растворов N 1-6, затем в каждый цилиндр приливают пипеткой вместимостью 25 см по 25 см
по 25 см дистиллированной воды. Полученные эталонные растворы содержат соответственно нитрат-ионов 2·10
дистиллированной воды. Полученные эталонные растворы содержат соответственно нитрат-ионов 2·10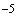 г·моля/дм
г·моля/дм (1,24 мг/дм
(1,24 мг/дм ); 2·10
); 2·10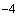 г·моля/дм
г·моля/дм (12,40 мг/дм
(12,40 мг/дм ); 4·10
); 4·10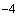 г·моля/дм
г·моля/дм (24,80 мг/дм
(24,80 мг/дм ); 6·10
); 6·10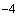 г·моля/дм
г·моля/дм (37,20 мг/дм
(37,20 мг/дм ); 8·10
); 8·10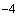 г·моля/дм
г·моля/дм (49,60 мг/дм
(49,60 мг/дм ); 1·10
); 1·10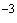 г·моля/дм
г·моля/дм (62,00 мг/дм
(62,00 мг/дм ). Затем к эталонным растворам добавляют пипеткой вместимостью 25 см
). Затем к эталонным растворам добавляют пипеткой вместимостью 25 см по 25 см
по 25 см буферного раствора. Растворы перемешивают и измеряют в них потенциалы по п.4.1 в порядке возрастания массовой концентрации нитрат-ионов в эталонных растворах.
буферного раствора. Растворы перемешивают и измеряют в них потенциалы по п.4.1 в порядке возрастания массовой концентрации нитрат-ионов в эталонных растворах.
На основе полученных данных строят градуировочный график зависимости потенциала электрода, 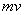 , от массовой концентрации нитрат-ионов. Для его построения на миллиметровой бумаге по оси абсцисс откладывают отрицательные логарифмы значений массовых концентраций нитрат-ионов в эталонных растворах, выраженные в г·молях/дм
, от массовой концентрации нитрат-ионов. Для его построения на миллиметровой бумаге по оси абсцисс откладывают отрицательные логарифмы значений массовых концентраций нитрат-ионов в эталонных растворах, выраженные в г·молях/дм , а по оси ординат - величины измеренных потенциалов.
, а по оси ординат - величины измеренных потенциалов.
Логарифмы значений массовых концентраций нитрат-ионов, г·моль/дм , приведены в табл.1. Градуировочный график проверяют ежедневно по двум эталонным растворам с массовой концентрацией нитрат-ионов 24,80 и 49,60 мг/дм
, приведены в табл.1. Градуировочный график проверяют ежедневно по двум эталонным растворам с массовой концентрацией нитрат-ионов 24,80 и 49,60 мг/дм .
.
Таблица 1
Соотношение между 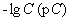 и массовой концентрацией нитрат-ионов
и массовой концентрацией нитрат-ионов
|
|
|
|
|
2,70 |
2,0·10 |
124,0 |
|
2,75 |
1,8·10 |
111,6 |
|
2,80 |
1,6·10 |
99,2 |
|
2,85 |
1,4·10 |
86,8 |
|
2,90 |
1,3·10 |
80,6 |
|
2,95 |
1,1·10 |
68,2 |
|
3,00 |
1,0·10 |
62,0 |
|
3,05 |
9,0·10 |
55,8 |
|
3,10 |
8,0·10 |
49,6 |
|
3,15 |
7,0·10 |
43,4 |
|
3,20 |
6,3·10 |
39,1 |
|
3,25 |
5,6·10 |
34,7 |
|
3,30 |
5,0·10 |
31,0 |
|
3,35 |
4,5·10 |
27,9 |
|
3,40 |
4,0·10 |
24,8 |
|
3,45 |
3,5·10 |
21,7 |
|
3,50 |
3,2·10 |
19,8 |
|
3,55 |
2,8·10 |
17,4 |
|
3,60 |
2,5·10 |
15,5 |
|
3,65 |
2,2·10 |
13,6 |
|
3,70 |
2,0·10 |
12,4 |
|
3,75 |
1,8·10 |
11,2 |
|
3,80 |
1,6·10 |
9,9 |
|
3,85 |
1,4·10 |
8,7 |
|
3,90 |
1,3·10 |
8,1 |
|
3,95 |
1,1·10 |
6,8 |
|
4,00 |
1,0·10 |
6,2 |
|
4,05 |
9,0·10 |
5,6 |
|
4,10 |
8,0·10 |
5,0 |
|
4,15 |
7,0·10 |
4,3 |
|
4,20 |
6,3·10 |
3,9 |
|
4,25 |
5,6·10 |
3,5 |
|
4,30 |
5,0·10 |
3,1 |
|
4,35 |
4,5·10 |
2,8 |
|
4,40 |
4,0·10 |
2,5 |
|
4,45 |
3,5·10 |
2,2 |
|
4,50 |
3,2·10 |
2,0 |
|
4,55 |
2,8·10 |
1,7 |
|
4,60 |
2,5·10 |
1,6 |
|
4,65 |
2,2·10 |
1,4 |
|
4,70 |
2,0·10 |
1,2 |
|
4,75 |
1,8·10 |
1,1 |
|
4,80 |
1,6·10 |
1,0 |
4.4.2. Определение нитрат-ионов в водах, содержащих более 500 мг/дм хлорид-ионов
хлорид-ионов
Исследуемую воду с массовой концентрацией хлорид-ионов от 500 до 2000 мг/дм наливают в стаканчик вместимостью 50 см
наливают в стаканчик вместимостью 50 см , погружают в нее нитратселективный электрод и наконечник электролитического ключа. Минеральную воду с массовой концентрацией хлорид-ионов более 2000 мг/дм
, погружают в нее нитратселективный электрод и наконечник электролитического ключа. Минеральную воду с массовой концентрацией хлорид-ионов более 2000 мг/дм перед анализом разбавляют дистиллированной водой до массовой концентрации в ней хлорид-ионов не более 2000 мг/дм
перед анализом разбавляют дистиллированной водой до массовой концентрации в ней хлорид-ионов не более 2000 мг/дм .
.
Потенциал электрода измеряют при помощи прибора для измерения потенциала. Показания прибора снимают через 30 с после погружения электрода. Проводят три параллельных измерения.
4.4.2.1. Построение градуировочного графика
В мерные цилиндры с притертой пробкой вместимостью 50 см вносят при помощи пипетки вместимостью 1 см
вносят при помощи пипетки вместимостью 1 см соответственно по 1 см
соответственно по 1 см рабочих стандартных растворов N 1-6, затем в каждый цилиндр приливают до метки раствор хлористого натрия, массовая концентрация хлорид-ионов в котором равна массовой концентрации их в исследуемой воде. Растворы перемешивают. Полученные эталонные растворы содержат соответственно нитрат-ионов 2·10
рабочих стандартных растворов N 1-6, затем в каждый цилиндр приливают до метки раствор хлористого натрия, массовая концентрация хлорид-ионов в котором равна массовой концентрации их в исследуемой воде. Растворы перемешивают. Полученные эталонные растворы содержат соответственно нитрат-ионов 2·10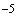 г·моля/дм
г·моля/дм (1,24 мг/дм
(1,24 мг/дм ); 2·10
); 2·10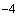 г·моля/дм
г·моля/дм (12,40 мг/дм
(12,40 мг/дм ); 4·10
); 4·10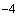 г·моля/дм
г·моля/дм (24,80 мг/дм
(24,80 мг/дм ); 6·10
); 6·10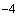 г·моля/дм
г·моля/дм (37,20 мг/дм
(37,20 мг/дм ); 8·10
); 8·10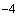 г·моля/дм
г·моля/дм (49,60 мг/дм
(49,60 мг/дм ) и 1·10
) и 1·10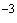 г·моля/дм
г·моля/дм (62,0 мг/дм
(62,0 мг/дм ).
).
В полученных эталонных растворах потенциал электрода измеряют по п.4.4.1. Буферные растворы при этом не добавляют. Измерения проводят в порядке возрастания массовой концентрации нитрат-ионов в эталонных растворах. На основании полученных данных строят градуировочный график по п.4.4.1.1.
4.5. Обработка результатов
Отрицательный логарифм значения массовой концентрации нитрат-ионов (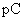 ) находят по градуировочному графику, используя среднее арифметическое значение трех параллельных измерений потенциала, проведенных из одной пробы. Массовую концентрацию нитрат-ионов находят по табл.1.
) находят по градуировочному графику, используя среднее арифметическое значение трех параллельных измерений потенциала, проведенных из одной пробы. Массовую концентрацию нитрат-ионов находят по табл.1.
При составлении таблицы использована зависимость
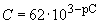 ,
,
где 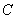 - массовая концентрация нитрат-ионов, г·моль/дм
- массовая концентрация нитрат-ионов, г·моль/дм ;
;
62 - г·моль нитрат-ионов;
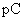 - отрицательный логарифм массовой концентрации нитрат-ионов, выраженный в г·моль/дм
- отрицательный логарифм массовой концентрации нитрат-ионов, выраженный в г·моль/дм .
.
Если при подготовке пробы к анализу минеральную воду разбавляют дистиллированной водой, то содержание нитрат-ионов (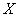 ), мг/дм
), мг/дм , вычисляют по формуле
, вычисляют по формуле
 ,
,
где 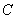 - содержание нитрат-ионов в разбавленной пробе, мг/дм
- содержание нитрат-ионов в разбавленной пробе, мг/дм ;
;
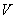 - объем разбавленного раствора, см
- объем разбавленного раствора, см ;
;
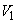 - объем минеральной воды, взятый на анализ, см
- объем минеральной воды, взятый на анализ, см .
.
За окончательный результат принимают среднее арифметическое значение двух параллельных измерений, расхождения между которыми не должны превышать 2,5 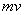 .
.
Раздел 4. (Введен дополнительно, Изм. N 1).
Текст документа сверен по:
официальное издание
Государственный контроль качества
минеральной воды и напитков. -
М.: ИПК Издательство стандартов, 2003


 Создайте свой интернет-магазин на новой платформе ReadyScript
Создайте свой интернет-магазин на новой платформе ReadyScript  Хостинг, домены, VPS/VDS, размещение серверов
Хостинг, домены, VPS/VDS, размещение серверов