- USD ЦБ 03.12 30.8099 -0.0387
- EUR ЦБ 03.12 41.4824 -0.0244
|
Краснодар:
|
погода |
Курсы
Индексы
- DJIA 03.12 12019.4 -0.01
- NASD 03.12 2626.93 0.03
- RTS 03.12 1545.57 -0.07
РД 52.24.403-95
РУКОВОДЯЩИЙ ДОКУМЕНТ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ МАССОВОЙ КОНЦЕНТРАЦИИ
КАЛЬЦИЯ В ВОДАХ ТИТРИМЕТРИЧЕСКИМ МЕТОДОМ С ТРИЛОНОМ Б
Дата введения 1995-01-01
Предисловие
1 РАЗРАБОТАН Гидрохимическим институтом, Малым научно-производственным предприятием "Акватест"
2 РАЗРАБОТЧИКИ Ю.Я.Винников, канд хим. наук, Л.В.Боева, канд. хим. наук, А.А.Назарова, канд. хим. наук
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Начальником ГУЭМЗ Росгидромета Цатуровым Ю.С. 21.07.94
4 ОДОБРЕН Секцией по методам химического и радиологического мониторинга природной среды ЦКПМ Росгидромета 21.06.94, протокол N 1
5 СВИДЕТЕЛЬСТВО ОБ АТТЕСТАЦИИ МВИ Выдано Гидрохимическим институтом в 1994 г. N 55
6 ЗАРЕГИСТРИРОВАН ЦКБ ГМП в 1995 г. N 403
7 ВЗАМЕН РД 52.24.55-86, РД 62.24.55-94
Введение
В естественных условиях содержание растворенного кальция и изменение его концентрации обусловлено главным образом равновесием углекислых солей и двуокиси углерода.
Основными источниками поступления кальция в поверхностные воды являются процессы химического выветривания и растворения минералов, прежде всего известняков, доломитов, гипса, кальцийсодержащих силикатов и других осадочных и метаморфических пород. Растворению способствуют микробиальные процессы разложения органических веществ, сопровождающиеся понижением рН. Большие количества кальция выносятся со сточными водами силикатной, металлургической, стекольной, химической промышленности и стоками с сельскохозяйственных угодий, особенно при использовании кальцийсодержащих минеральных удобрений.
В водных объектах кальций в заметных количествах может выпадать в осадок в виде CaSO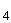 и СаСО
и СаСО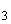 при испарении воды, а также в условиях активизации фотосинтеза, сопровождающегося повышением рН воды. Характерной особенностью кальция является его склонность образовывать в поверхностных водах довольно устойчивые пересыщенные растворы СаСО
при испарении воды, а также в условиях активизации фотосинтеза, сопровождающегося повышением рН воды. Характерной особенностью кальция является его склонность образовывать в поверхностных водах довольно устойчивые пересыщенные растворы СаСО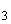 . Ионная форма кальция характерна только для маломинерализованных вод. При увеличении минерализации ионы кальция образуют нейтральные (CaSO
. Ионная форма кальция характерна только для маломинерализованных вод. При увеличении минерализации ионы кальция образуют нейтральные (CaSO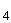 и СаСО
и СаСО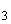 ) или заряженные (СаНСО
) или заряженные (СаНСО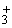 ) ионные пары. Довольно устойчивые комплексные соединения кальций образует с содержащимися в воде органическими веществами.
) ионные пары. Довольно устойчивые комплексные соединения кальций образует с содержащимися в воде органическими веществами.
В речных и озерных водах содержание кальция в большинстве случаев находится в пределах 10-100 мг/дм . При контакте вод с кальцийсодержащими минералами (известняк, доломит, гипс и др.) содержание кальция может повышаться до нескольких сотен миллиграммов в кубическом дециметре.
. При контакте вод с кальцийсодержащими минералами (известняк, доломит, гипс и др.) содержание кальция может повышаться до нескольких сотен миллиграммов в кубическом дециметре.
ПДК кальция в воде водных объектов рыбохозяйственного назначения составляет 180 мг/дм , для водных объектов хозяйственно-питьевого назначения ПДК не установлена.
, для водных объектов хозяйственно-питьевого назначения ПДК не установлена.
1 Назначение и область применения методики
Настоящий руководящий документ устанавливает титриметрическую методику выполнения измерений массовой концентрации кальция в пробах поверхностных вод суши и очищенных сточных вод в диапазоне 1,0-100 мг/дм . При анализе проб воды с массовой концентрацией кальция, превышающей 100 мг/дм
. При анализе проб воды с массовой концентрацией кальция, превышающей 100 мг/дм , соответственно уменьшают аликвоту пробы, отбираемую для выполнения измерений.
, соответственно уменьшают аликвоту пробы, отбираемую для выполнения измерений.
2 Нормы погрешности и значения характеристик погрешности измерения
В соответствии с ГОСТ 27384 норма погрешности при выполнении измерений кальция в природных водах в диапазоне массовых концентраций 0,5-50,0 мг/дм составляют ±10%, свыше 50 мг/дм
составляют ±10%, свыше 50 мг/дм - ±5%.
- ±5%.
В сточных водах норма погрешности составляет ±10% в диапазоне массовых концентраций кальция 5,0-100,0 мг/дм и ±5% -свыше 100 мг/дм
и ±5% -свыше 100 мг/дм .
.
Установленные для настоящей методики значения характеристик погрешности и ее составляющих приведены в таблице 1.
Таблица 1 - Значения характеристик погрешности и ее составляющих (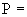 0,95)
0,95)
|
Диапазон измеряемых концентраций кальция, |
Характеристики составляющих погрешности, мг/дм |
Характеристика погрешности, мг/дм | |
|
случайной, |
систематической |
||
|
1,0-100,0 |
0,1+0,020 |
0,053 |
0,2+0,044 |
При выполнении измерений в пробах с массовой концентрацией кальция свыше 100 мг/дм при соответствующем уменьшении объема анализируемой пробы погрешность измерения не превышает значений, рассчитанных по приведенной в таблице 1 зависимости.
при соответствующем уменьшении объема анализируемой пробы погрешность измерения не превышает значений, рассчитанных по приведенной в таблице 1 зависимости.
3 Метод измерений
Определение основано на способности ионов кальция образовывать с трилоном Б малодиссоциированное, устойчивое в щелочной среде соединение. Конечная точка титрования определяется по изменению окраски индикатора (мурексида) из розовой в красно-фиолетовую. Для увеличения четкости перехода окраски предпочтительнее использовать смешанный индикатор (мурексид + нафтоловый зеленый Б). При этом в конечной точке титрования окраска изменяется от грязно-зеленой до синей.
Магний в условиях анализа осаждается в виде гидроксида и не мешает определению.
Определению мешают ионы железа (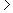 10 мг/дм
10 мг/дм ), кобальта, никеля (
), кобальта, никеля (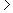 0,1 мг/дм
0,1 мг/дм ), алюминия (
), алюминия (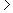 10 мг/дм
10 мг/дм ), меди (
), меди (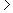 0,05 мг/дм
0,05 мг/дм ), вызывая нечеткое изменение окраски в точке эквивалентности. Другие катионы, например, свинец, кадмий, марганец (II), цинк, стронций, барий могут частично титроваться вместе с кальцием и магнием и повышать расход трилона Б. Результаты определения могут также быть искажены в присутствии значительных количеств анионов (НСО
), вызывая нечеткое изменение окраски в точке эквивалентности. Другие катионы, например, свинец, кадмий, марганец (II), цинк, стронций, барий могут частично титроваться вместе с кальцием и магнием и повышать расход трилона Б. Результаты определения могут также быть искажены в присутствии значительных количеств анионов (НСО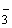 , СО
, СО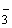 , РО
, РО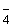 , SiO
, SiO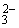 ). Для уменьшения их влияния пробу следует титровать сразу после добавления щелочи.
). Для уменьшения их влияния пробу следует титровать сразу после добавления щелочи.
Мешающее влияние катионов металлов устраняют добавлением соответствующих маскирующих реагентов.
Мешающее влияние взвешенных и коллоидных веществ устраняется фильтрованием пробы, цветности - пропусканием пробы через активный уголь.
4 Средства измерений, вспомогательные устройства, реактивы, материалы
4.1 Средства измерений, вспомогательные устройства
4.1.1 Весы аналитические 2 класса точности по ГОСТ 24104.
4.1.2 Весы технические лабораторные 4 класса точности по ГОСТ 24104 с пределом взвешивания 200 г.
4.1.3 Шкаф сушильный общелабораторного назначения по ГОСТ 13474.
4.1.4 Плитка электрическая по ГОСТ 14919.
|
4.1.5 Колба мерная не ниже 2 класса точности по ГОСТ 1770 вместимостью: |
500 см |
|||
|
4.1.6 Пипетки градуированные не ниже 2 класса точности по ГОСТ 29227 вместимостью: |
||||
|
1 см |
||||
|
2 см |
||||
|
5 см |
||||
|
4.1.7 Пипетки с одной меткой не ниже 2 класса точности по ГОСТ 29169 вместимостью: |
||||
|
10 см |
||||
|
25 см |
||||
|
50 см |
||||
|
100 см |
||||
|
4.1.8 Бюретка не ниже 2 класса точности по ГОСТ 29251 вместимостью |
25 см |
|||
|
4.1.9 Микробюретка не ниже 2 класса точности по ГОСТ 29251 вместимостью |
2 см |
|||
|
4.1.10 Цилиндры мерные по ГОСТ 1770 вместимостью: |
||||
|
25 см |
||||
|
100 см |
||||
|
500 см |
||||
|
1000 см |
||||
|
4.1.11 Колбы конические по ГОСТ 25336 вместимостью |
250 см |
|||
|
4.1.12 Колба коническая термостойкая по ГОСТ 25336 вместимостью |
500 см |
|||
|
4.1.13 Стаканы химические по ГОСТ 25336 вместимостью: |
||||
|
100 см |
||||
|
250 см |
||||
|
1000 см |
||||
|
4.1.14 Стаканчики для взвешивания (бюксы) по ГОСТ 25336 |
- 2 |
|||
|
4.1.15 Ступка фарфоровая по ГОСТ 9147 |
- 1 |
|||
|
4.1.16 Колонка хроматографическая диаметром 1,5-2,0 и длиной 25-30 см |
- 1 |
|||
Допускается использование других типов средств измерений, посуды и вспомогательного оборудования, в том числе импортных, с характеристиками не хуже, чем у приведенных в разделе 4.1.
4.2 Реактивы и материалы
4.2.1 Динатриевая соль этилендиамин -N,N,N,N-тетрауксусной кислоты, дигидрат (трилон Б, комплексон III) по ГОСТ 10652, ч.д.а.
4.2.2 Цинк гранулированный по ГОСТ 989, ч.д.а.
4.2.3 Хлорид аммония по ГОСТ 3773, ч.д.а.
4.2.4 Аммиак водный по ГОСТ 3760, ч.д.а.
4.2.5 Хлорид натрия по ГОСТ 4233, ч.д.а.
4.2.6 Гидроксид натрия по ГОСТ 4328, ч.д.а. или ч.
4.2.7 Сульфид натрия по ГОСТ 2053, ч.д.а. или диэтилдитиокарбамат натрия по ГОСТ 8864, ч.д.а.
4.2.8 Соляная кислота по ГОСТ 3118, ч.д.а.
4.2.9 Пурпурат аммония (мурексид) по ТУ 6-09-1657, ч.д.а.
4.2.10 Нафтоловый зеленый Б.
4.2.11 Эриохром черный Т (хромоген черный).
4.2.12 Гидроксиламина гидрохлорид по ГОСТ 5456, ч.д.а.
4.2.13 Уголь активный.
4.2.14 Вода дистиллированная по ГОСТ 6709.
4.2.15 Универсальная индикаторная бумага (рН 1-10) по ТУ 6-09-1181.
4.2.16 Фильтры мембранные "Владипор МФА-МА", 0,45 мкм, по ТУ 6-05-1903 или другого типа, равноценные по характеристикам, или фильтры бумажные обеззоленные "синяя лента" по ТУ 6-09-1678.
Допускается использование реактивов, изготовленных по другой нормативно-технической документации, в том числе импортных, с квалификацией не ниже указанной в 4.2.
5 Отбор и хранение проб
Отбор проб производят в соответствии с ГОСТ 17.1.5.05. При наличии значительного количества взвесей воду фильтруют через мембранный фильтр 0,45 мкм или бумажный фильтр. Пробы хранят в стеклянной или полиэтиленовой посуде не более 6 мес.
Если в период хранения в пробе выпал осадок карбоната кальция, непосредственно перед анализом его растворяют прибавлением 1 см концентрированной соляной кислоты, предварительно отсифонировав прозрачный слой над осадком. Затем отсифонированный раствор и жидкость с растворенным осадком соединяют вместе и нейтрализуют 20% раствором гидроксида натрия, добавляя его по каплям и контролируя рН по индикаторной бумаге. Далее выполняют определение, как описано в разделе 7.
концентрированной соляной кислоты, предварительно отсифонировав прозрачный слой над осадком. Затем отсифонированный раствор и жидкость с растворенным осадком соединяют вместе и нейтрализуют 20% раствором гидроксида натрия, добавляя его по каплям и контролируя рН по индикаторной бумаге. Далее выполняют определение, как описано в разделе 7.
6 Подготовка к выполнению измерений
6.1 Приготовление растворов и реактивов
6.1.1 Раствор трилона Б с концентрацией 0,02 моль/дм эквивалента
эквивалента
3,72 г трилона Б растворяют в 1 дм дистиллированной воды. Точную концентрацию раствора устанавливают по стандартному раствору хлорида цинка, как описано в 6.2.
дистиллированной воды. Точную концентрацию раствора устанавливают по стандартному раствору хлорида цинка, как описано в 6.2.
Раствор хранят в полиэтиленовой посуде, проверяют его концентрацию не реже 1 раза в месяц.
6.1.2 Раствор хлорида цинка с концентрацией 0,02 моль/дм эквивалента
эквивалента
Отвешивают на технических весах около 0,35 г металлического цинка, смачивают его небольшим количеством концентрированной соляной кислоты и сейчас же промывают дистиллированной водой. Цинк сушат в сушильном шкафу при 105 °С в течение 1 ч, затем охлаждают и взвешивают на аналитических весах.
Навеску цинка помещают в мерную колбу вместимостью 500 см , в которую предварительно вносят 10-15 см
, в которую предварительно вносят 10-15 см дважды дистиллированной воды и 1,5 см
дважды дистиллированной воды и 1,5 см концентрированной соляной кислоты. Цинк растворяют. После растворения цинка объем раствора доводят до метки на колбе дистиллированной водой.
концентрированной соляной кислоты. Цинк растворяют. После растворения цинка объем раствора доводят до метки на колбе дистиллированной водой.
Рассчитывают концентрацию эквивалента раствора хлорида цинка 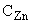 (1/2 ZnCl
(1/2 ZnCl ), моль/дм
), моль/дм , по формуле
, по формуле
 , (1)
, (1)
где 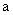 - навеска металлического цинка, г;
- навеска металлического цинка, г;
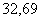 - молярная масса эквивалента Zn
- молярная масса эквивалента Zn , г/моль;
, г/моль;
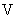 - объем мерной колбы, дм
- объем мерной колбы, дм .
.
6.1.3 Буферный раствор NH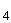 Cl+NH
Cl+NH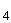 OH
OH
7,0 г хлорида аммония растворяют в мерной колбе вместимостью 500 см в 100 см
в 100 см дистиллированной воды и добавляют 75 см
дистиллированной воды и добавляют 75 см концентрированного раствора аммиака. Объем раствора доводят до метки на колбе дистиллированной водой и тщательно перемешивают.
концентрированного раствора аммиака. Объем раствора доводят до метки на колбе дистиллированной водой и тщательно перемешивают.
Буферный раствор хранят в стеклянной или полиэтиленовой посуде не более 2 мес.
6.1.4 Индикатор эриохром черный Т
0,5 г эриохрома черного Т тщательно растирают в ступке с 50 г хлорида натрия. Используют при определении точной концентрации раствора трилона Б.
6.1.5 Индикатор мурексид
0,2 г мурексида и 0,5 г нафтолового зеленого Б (или 0,2 г только мурексида) тщательно растирают в ступке со 100 г хлорида натрия. Хранят в склянке из темного стекла.
6.1.6 Раствор гидроксида натрия, 20%
20 г NaOH растворяют в 80 см дистиллированной воды.
дистиллированной воды.
6.1.7 Раствор гидроксида натрия, 8%
40 г NaOH растворяют в 460 см дистиллированной воды.
дистиллированной воды.
6.1.8 Раствор гидроксида натрия, 0,4%
2 г NaOH растворяют в 500 см дистиллированной воды.
дистиллированной воды.
Растворы гидроксида натрия устойчивы при хранении в плотно закрытой полиэтиленовой посуде.
6.1.9 Раствор сульфида натрия
2 г сульфида натрия растворяют в 50 см дистиллированной воды. Хранят в плотно закрытой полиэтиленовой посуде не более недели.
дистиллированной воды. Хранят в плотно закрытой полиэтиленовой посуде не более недели.
6.1.10 Раствор диэтилдитиокарбамата натрия
5 г диэтилдитиокарбамата натрия растворяют в 50 см дистиллированной воды. Хранят не более 2 недель.
дистиллированной воды. Хранят не более 2 недель.
6.1.11 Раствор гидрохлорида гидроксиламина
5 г гидрохлорида гидроксиламина растворяют в 100 см дистиллированной воды.
дистиллированной воды.
6.1.12 Раствор соляной кислоты, 1:3
200 см концентрированной соляной кислоты смешивают с 600 см
концентрированной соляной кислоты смешивают с 600 см дистиллированной воды.
дистиллированной воды.
6.1.13 Активный уголь
Порцию активного угля, достаточную для заполнения колонки, помещают в коническую колбу, добавляют 100-150 см раствора соляной кислоты (1:3) и кипятят 2-3 ч. Если раствор кислоты окрашивается, повторяют операцию до тех пор, пока он не останется бесцветным.
раствора соляной кислоты (1:3) и кипятят 2-3 ч. Если раствор кислоты окрашивается, повторяют операцию до тех пор, пока он не останется бесцветным.
Уголь отмывают дистиллированной водой до нейтральной реакции по универсальной индикаторной бумаге, добавляют 100-150 см 8% раствора гидроксида натрия и выдерживают 8-10 ч. Если появляется окраска, операцию повторяют.
8% раствора гидроксида натрия и выдерживают 8-10 ч. Если появляется окраска, операцию повторяют.
Очищенный уголь отмывают дистиллированной водой до нейтральной реакции. Хранят в склянке с дистиллированной водой.
После пропускания каждой пробы воды уголь в колонке регенерируют промыванием 0,4% раствором гидроксида натрия до исчезновения окраски последнего, затем дистиллированной до нейтральной реакции.
6.2 Установление точной концентрации раствора трилона Б
В коническую колбу вместимостью 250 см вносят 10 см
вносят 10 см раствора хлорида цинка (6.1.2), добавляют дистиллированной воды приблизительно до 100 см
раствора хлорида цинка (6.1.2), добавляют дистиллированной воды приблизительно до 100 см , 5 см
, 5 см буферного раствора и 10-15 мг индикатора эриохрома черного Т. Содержимое конической колбы тщательно перемешивают и титруют из бюретки раствором трилона Б до перехода окраски из красной в голубую.
буферного раствора и 10-15 мг индикатора эриохрома черного Т. Содержимое конической колбы тщательно перемешивают и титруют из бюретки раствором трилона Б до перехода окраски из красной в голубую.
Концентрацию раствора трилона Б рассчитывают по формуле:
 , (2)
, (2)
где: 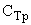 - концентрация раствора трилона Б, моль/дм
- концентрация раствора трилона Б, моль/дм эквивалента;
эквивалента;
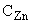 - концентрация раствора хлорида цинка, моль/дм
- концентрация раствора хлорида цинка, моль/дм эквивалента;
эквивалента;
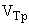 - объем раствора трилона Б, пошедшего на титрование, см
- объем раствора трилона Б, пошедшего на титрование, см ;
;
 - объем раствора хлорида цинка, см
- объем раствора хлорида цинка, см .
.
7 Выполнение измерений
7.1 Выбор условий титрования
Объем пробы воды для определения кальция выбирают исходя из известной величины общей жесткости или по результатам оценочного титрования.
Если жесткость составляет менее 4 ммоль/дм эквивалента, то для анализа берут 100 см
эквивалента, то для анализа берут 100 см , 4-8 ммоль/дм
, 4-8 ммоль/дм эквивалента - 50 см
эквивалента - 50 см и более 8 ммоль/дм
и более 8 ммоль/дм эквивалента - 25 см
эквивалента - 25 см пробы воды.
пробы воды.
Для оценочного титрования берут 10 см воды, добавляют 0,2 см
воды, добавляют 0,2 см 8% раствора гидроксида натрия, 10-15 мг индикатора мурексида и титруют раствором трилона Б со смешанным индикатором до перехода окраски из грязно-зеленой в синюю, а при использовании только мурексида - из розовой в красно-фиолетовую. По величине израсходованного на титрование объема раствора трилона Б выбирают из таблицы 2 соответствующий объем пробы воды.
8% раствора гидроксида натрия, 10-15 мг индикатора мурексида и титруют раствором трилона Б со смешанным индикатором до перехода окраски из грязно-зеленой в синюю, а при использовании только мурексида - из розовой в красно-фиолетовую. По величине израсходованного на титрование объема раствора трилона Б выбирают из таблицы 2 соответствующий объем пробы воды.
Таблица 2 - Объем пробы воды, рекомендуемый для выполнения измерений массовой концентрации кальция по результатам оценочного титрования
|
Объем израсходованного раствора трилона Б, см |
|
2-4 |
4-8 |
|
|
Рекомендуемый объем пробы, см |
100 |
50 |
25 |
10 |
В зависимости от содержания кальция титрование проводят из микробюретки или из бюретки. Если по результатам оценочного титрования объем трилона Б меньше 0,2 см или жесткость меньше 0,4 ммоль/дм
или жесткость меньше 0,4 ммоль/дм эквивалента используют микробюретку, в противном случае - бюретку.
эквивалента используют микробюретку, в противном случае - бюретку.
7.2 Титрование
В коническую колбу отмеривают пипеткой требуемый объем пробы, доводят, если необходимо, до 100 см дистиллированной водой, добавляют 2 см
дистиллированной водой, добавляют 2 см 8%-ного раствора гидроксида натрия, 0,1-0,2 г индикатора мурексида и титруют раствором трилона Б со смешанным индикатором до перехода окраски из грязно-зеленой в синюю, а при использовании только мурексида - из розовой в красно-фиолетовую. Повторяют титрование и, если расхождение между параллельными титрованиями не превышает приведенных в таблице 3, за результат принимают среднее значение объема трилона Б. В противном случае повторяют титрование до получения допустимого расхождения результатов.
8%-ного раствора гидроксида натрия, 0,1-0,2 г индикатора мурексида и титруют раствором трилона Б со смешанным индикатором до перехода окраски из грязно-зеленой в синюю, а при использовании только мурексида - из розовой в красно-фиолетовую. Повторяют титрование и, если расхождение между параллельными титрованиями не превышает приведенных в таблице 3, за результат принимают среднее значение объема трилона Б. В противном случае повторяют титрование до получения допустимого расхождения результатов.
Таблица 3 - Допустимые расхождения между параллельными титрованиями в зависимости от объема раствора трилона Б
|
Объем израсходованного раствора трилона Б, см |
|
2-5 |
5-10 |
10-15 |
|
|
Допустимое расхождение объемов трилона Б, см |
0,04 |
0,05 |
0,1 |
0,2 |
0,3 |
7.3 Устранение мешающих влияний
Для устранения мешающего влияния катионов металлов к пробе перед титрованием прибавляют 0,5 см раствора сульфида или диэтилдитиокарбамата натрия и 0,5 см раствора гидрохлорида гидроксиламина.
раствора сульфида или диэтилдитиокарбамата натрия и 0,5 см раствора гидрохлорида гидроксиламина.
Если проба воды заметно окрашена за счет присутствия веществ природного или антропогенного происхождения, затрудняется фиксация конечной точки титрования. В этом случае пробу перед выполнением анализа следует пропустить со скоростью 3-5 см /мин через хроматографическую колонку (4.1.12), заполненную активным углем (высота слоя 15-20 см). Первые 25-30 см
/мин через хроматографическую колонку (4.1.12), заполненную активным углем (высота слоя 15-20 см). Первые 25-30 см пробы, прошедшей через колонку, отбрасывают.
пробы, прошедшей через колонку, отбрасывают.
Как правило, окрашенные соединения антропогенного происхождения сорбируются активным углем практически полностью, в то время как природного (гумусовые вещества) - лишь частично. При высокой и не устраняемой цветности пробы, обусловленной гумусовыми веществами, определение конечной точки титрования значительно облегчается использованием для сравнения перетитрованной пробы этой же воды (пробы-свидетеля).
8 Вычисление результатов измерений
Массовую концентрацию кальция в анализируемой пробе воды находят по формулам:
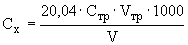 или
или 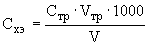 , (3)
, (3)
где 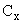 или
или 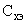 - массовая концентрация кальция в воде, мг/дм
- массовая концентрация кальция в воде, мг/дм или ммоль/дм
или ммоль/дм эквивалента соответственно;
эквивалента соответственно;
 - концентрация раствора трилона Б, моль/дм
- концентрация раствора трилона Б, моль/дм эквивалента;
эквивалента;
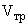 - объем раствора трилона Б, пошедшего на титрование пробы, см
- объем раствора трилона Б, пошедшего на титрование пробы, см ;
;
 - объем пробы воды, взятый для определения, см
- объем пробы воды, взятый для определения, см .
.
 -молярная масса эквивалента Са
-молярная масса эквивалента Са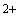 , г/моль.
, г/моль.
Результат измерения в документах, предусматривающих его использование, представляют в виде:
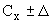 , мг/дм
, мг/дм (
(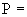 0,95), (4)
0,95), (4)
где  - характеристика погрешности измерения для данной массовой концентрации кальция (таблица 1).
- характеристика погрешности измерения для данной массовой концентрации кальция (таблица 1).
Численные значения результата измерения должны оканчиваться цифрой того же разряда, что и значения характеристики погрешности.
9 Контроль погрешности измерений
Оперативный контроль погрешности проводят с использованием метода добавок совместно с методом разбавления пробы. Периодичность контроля - не менее одной контрольной на 15-20 рабочих проб за период, в течение которого условия проведения анализа неизменны.
Измеряют массовую концентрацию кальция в исходной пробе (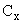 ), в пробе, разбавленной в
), в пробе, разбавленной в 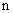 раз (
раз (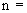 1,5-2,5) (
1,5-2,5) (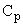 ) и в пробе, разбавленной в
) и в пробе, разбавленной в 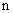 раз с введенной добавкой (
раз с введенной добавкой (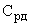 ). Величина добавки (
). Величина добавки (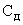 ) должна составлять 40-60% от концентрации кальция в исходной пробе.
) должна составлять 40-60% от концентрации кальция в исходной пробе.
Результат контроля признают удовлетворительным, если:
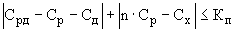 (5)
(5)
Норматив контроля погрешности (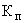 ) рассчитывают по формуле:
) рассчитывают по формуле:
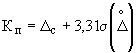 (
(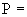 0,95), (6)
0,95), (6)
где 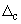 и
и 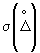 - характеристики систематической и случайной составляющих погрешности измерений массовой концентрации кальция в исходной пробе
- характеристики систематической и случайной составляющих погрешности измерений массовой концентрации кальция в исходной пробе 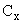 (таблица 1).
(таблица 1).
При превышении норматива измерение повторяют. При повторном превышении указанного норматива выясняют причины, приводящие к неудовлетворительным результатам, и устраняют их.
10 Требования безопасности
10.1 При выполнении измерений массовой концентрации кальция в пробах природных и очищенных сточных вод соблюдают требования безопасности, установленные в "Правилах по технике безопасности при производстве наблюдений и работ на сети Госкомгидромета", Л., Гидрометеоиздат, 1983, или в "Типовой инструкции по технике безопасности для гидрохимических лабораторий служб Роскомвода", М, 1995.
10.2 По степени воздействия на организм вредные вещества, используемые при выполнении измерений, относятся ко 2, 3 классам опасности по ГОСТ 12.1.007.
10.3 Содержание используемых вредных веществ в воздухе рабочей зоны не должно превышать установленных предельно допустимых концентраций в соответствии с ГОСТ 12.1.005.
11 Требования к квалификации операторов
К выполнению измерений и обработке их результатов допускаются лица со средним профессиональным образованием или без профессионального образования, но имеющие стаж работы в лаборатории не менее года и освоившие методику анализа.
12 Затраты времени на проведение анализа
На приготовление растворов и реактивов в расчете на 100 определений - 1,0 чел.-ч.
На проведение определения и вычисление результатов серии из 10 проб - 3,5 чел.-ч.
Затраты времени на подготовку посуды включены в затраты времени на проведение анализа.
Текст документа сверен по:
/ Федеральная служба России по гидрометеорологии
и мониторингу окружающей среды. -
Ростов-на-Дону: Гидрохимический институт, 1995

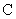 , мг/дм
, мг/дм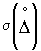
 2
2 
 Создайте свой интернет-магазин на новой платформе ReadyScript
Создайте свой интернет-магазин на новой платформе ReadyScript  Хостинг, домены, VPS/VDS, размещение серверов
Хостинг, домены, VPS/VDS, размещение серверов